24/09/2025
En el vertiginoso mundo de la Fórmula 1 y las categorías de alta competición, a menudo centramos nuestra atención en la aerodinámica, la potencia del motor o la habilidad del piloto. Sin embargo, existe un componente fundamental, el único punto de contacto entre un monoplaza de 1000 caballos de fuerza y el asfalto: el neumático. Y en el corazón de ese neumático, a nivel molecular, se encuentra un héroe anónimo cuya estructura química define los límites de la física en cada vuelta: el 1,3-butadieno. Comprender su estructura híbrida no es solo un ejercicio de química, es desvelar uno de los secretos mejor guardados que permite a los coches de carreras desafiar la gravedad en las curvas y transmitir una potencia brutal al suelo.

¿Qué es Exactamente el 1,3-Butadieno?
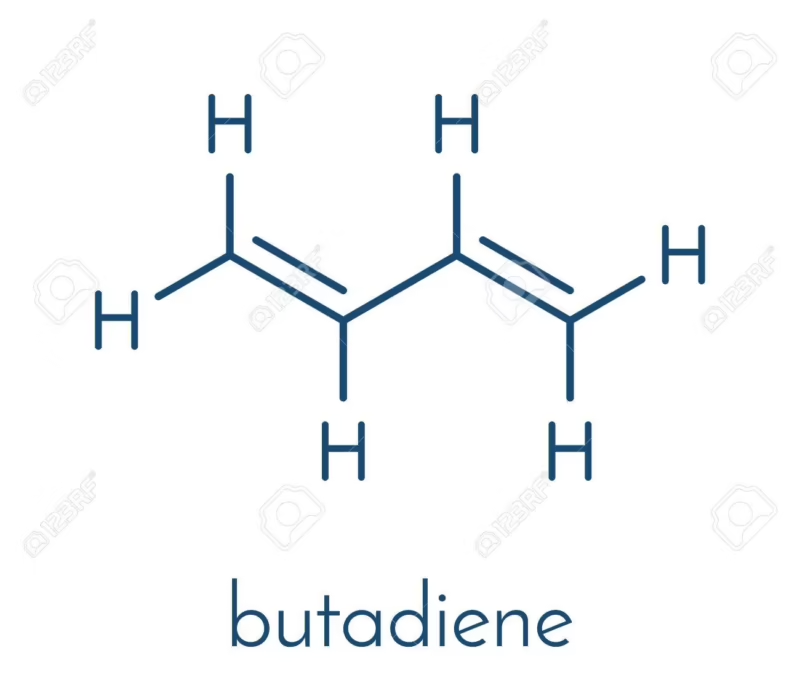
Antes de sumergirnos en orbitales y electrones, pongámoslo en un lenguaje que resuena en el paddock. El 1,3-butadieno es un hidrocarburo simple, un gas incoloro en su estado natural. Su fórmula química es C₄H₆, lo que nos dice que está compuesto por cuatro átomos de carbono y seis de hidrógeno. Lo que lo hace tan especial y tan crucial para el motorsport es la forma en que esos átomos de carbono están enlazados entre sí. Se trata de una cadena de cuatro carbonos donde existen dos dobles enlaces, específicamente entre el primer y segundo carbono, y entre el tercer y cuarto carbono. De ahí su nombre: 'buta' por los cuatro carbonos, 'dieno' por los dos dobles enlaces, y '1,3' para indicar sus posiciones.
Esta configuración de dobles enlaces alternados con un enlace simple es lo que los químicos llaman un sistema conjugado, y es la piedra angular de su increíble versatilidad y rendimiento.
La Clave Está en la Hibridación: La Estructura Molecular
Aquí es donde la magia ocurre y donde respondemos a la pregunta central. Para que los átomos de carbono puedan formar los enlaces que vemos en el 1,3-butadieno, adoptan una configuración electrónica especial conocida como hibridación sp². Cada uno de los cuatro átomos de carbono utiliza tres de sus orbitales para formar tres enlaces fuertes y estables, llamados enlaces sigma (σ). Estos enlaces forman el esqueleto plano de la molécula.
Sin embargo, a cada átomo de carbono le sobra un orbital atómico, un orbital 'p', que se posiciona de forma perpendicular al plano de la molécula, como si fueran pequeñas velas de barco por encima y por debajo de la cadena de carbonos. Y aquí viene lo fascinante: en lugar de que los orbitales 'p' del carbono 1 y 2 interactúen solo entre sí, y los del 3 y 4 hagan lo mismo por su cuenta, los cuatro orbitales 'p' se solapan entre sí. Crean una especie de 'nube' electrónica deslocalizada que se extiende a lo largo de toda la molécula.
Orbitales Moleculares: La Verdadera Estructura
Esta interacción de los cuatro orbitales 'p' da lugar a la formación de cuatro orbitales moleculares π (pi). Pensemos en ellos como los diferentes 'niveles de energía' que los cuatro electrones π (uno de cada carbono) pueden ocupar. Estos niveles se dividen en dos categorías:
- Orbitales de Enlace (π₁ y π₂): Tienen menor energía que los orbitales 'p' atómicos originales. Son estabilizadores, ya que al ser ocupados por electrones, la molécula se vuelve más estable.
- Orbitales de Antienlace (π₃* y π₄*): Tienen mayor energía. Si fueran ocupados por electrones, desestabilizarían la molécula.
En el 1,3-butadieno, los cuatro electrones π disponibles llenan los dos orbitales de enlace (π₁ y π₂) de menor energía. El orbital π₂ es el más alto en energía que está ocupado, por lo que se le conoce como HOMO (Highest Occupied Molecular Orbital). Como los electrones se encuentran en estos orbitales de enlace estabilizadores y deslocalizados, la molécula de conjugación es excepcionalmente estable y, a la vez, reactiva de una manera muy controlable. Esta reactividad controlada es la puerta de entrada a su uso en el mundo del motor.
Del Laboratorio a la Pista: La Magia de la Polimerización
La molécula de 1,3-butadieno por sí sola no sirve de mucho en un circuito. Su verdadero poder se desata a través de un proceso llamado polimerización. Este proceso consiste en unir miles y miles de moléculas individuales de 1,3-butadieno (monómeros) para formar cadenas larguísimas y entrelazadas, creando un polímero: el caucho sintético.
La estructura de dobles enlaces conjugados del 1,3-butadieno es perfecta para este proceso. Permite que las moléculas se unan entre sí de formas muy específicas, dando lugar a diferentes tipos de cauchos sintéticos con propiedades ajustadas a la carta. Los dos más importantes en el automovilismo son:
- Caucho de Polibutadieno (PBR): Formado exclusivamente por monómeros de 1,3-butadieno. Es conocido por su altísima resistencia a la abrasión y su excelente flexibilidad a bajas temperaturas.
- Caucho Estireno-Butadieno (SBR): Es un copolímero, donde se combinan monómeros de 1,3-butadieno con otro monómero llamado estireno. Este caucho es famoso por proporcionar un agarre (grip) excepcional.
Los ingenieros de neumáticos de equipos como Ferrari, Red Bull o Mercedes no eligen un tipo de caucho, sino que crean complejas mezclas de PBR, SBR, caucho natural y otros aditivos (como negro de humo y sílice) para diseñar los compuestos de neumáticos blandos, medios y duros. La proporción de 1,3-butadieno en la mezcla es un factor determinante en el rendimiento final.
Tabla Comparativa: Propiedades Clave para el Motorsport
| Característica | Caucho de Polibutadieno (PBR) | Caucho Estireno-Butadieno (SBR) | Relevancia en Pista |
|---|---|---|---|
| Resistencia a la Abrasión | Muy Alta | Buena | Define la durabilidad del neumático y la degradación. Clave para los compuestos duros. |
| Agarre (Grip) | Moderado | Excelente | Factor decisivo para el tiempo por vuelta, especialmente en clasificación y compuestos blandos. |
| Flexibilidad a Baja Temperatura | Excelente | Buena | Importante para que el neumático entre en su ventana de temperatura óptima rápidamente. |
| Generación de Calor (Histeresis) | Baja | Alta | Un neumático con alta histeresis genera más calor y más agarre, pero también se degrada más rápido. |
El Impacto Directo en una Vuelta de Clasificación
Imaginemos un F1 atacando la curva Eau Rouge en Spa-Francorchamps. Cuando el piloto gira, las fuerzas G laterales son inmensas. El neumático se deforma brutalmente. Las largas cadenas de polímeros basadas en 1,3-butadieno se estiran y se retuercen. Gracias a la estructura molecular, el caucho puede deformarse para maximizar la superficie de contacto con el asfalto (la huella del neumático) y luego volver a su forma original. En este proceso de deformación y recuperación, parte de la energía se disipa en forma de calor. Este fenómeno, llamado histeresis, es la fuente fundamental de la adherencia mecánica. La estructura derivada del 1,3-butadieno es excepcionalmente buena para generar esta histeresis, permitiendo que el neumático se 'clave' literalmente en las micro-irregularidades del asfalto.
Por lo tanto, la próxima vez que veas un piloto marcar un tiempo de pole por milésimas de segundo, recuerda que parte de esa velocidad no viene del motor, sino de la forma en que miles de millones de moléculas de 1,3-butadieno se organizaron para crear un polímero capaz de generar un agarre sobrehumano.
Preguntas Frecuentes (FAQ)
¿Por qué se usa caucho sintético y no natural en la F1?
Aunque el caucho natural se utiliza en las mezclas, el caucho sintético derivado del 1,3-butadieno ofrece una ventaja crucial: la consistencia y la capacidad de diseño. Los ingenieros pueden ajustar las propiedades del caucho sintético a nivel molecular para lograr niveles de agarre, durabilidad y rangos de temperatura específicos, algo mucho más difícil de conseguir con el caucho natural puro.
¿La estructura del 1,3-butadieno afecta la degradación del neumático?
Absolutamente. La forma en que las cadenas de polímero se enlazan y su resistencia inherente a la rotura bajo estrés (resistencia a la tracción y abrasión) dependen directamente de la estructura del monómero original. Una estructura molecular robusta, como la que se logra con el polibutadieno, conduce a un neumático que se desgasta de manera más predecible y lenta, un factor clave en la estrategia de carrera.
¿Todos los neumáticos de competición usan 1,3-butadieno?
Es un componente fundamental en la gran mayoría de los neumáticos de alto rendimiento, no solo en la Fórmula 1, sino también en categorías como el WRC, IndyCar o las carreras de resistencia. Su capacidad para proporcionar una combinación ganadora de agarre, resistencia y flexibilidad lo convierte en el pilar de la tecnología moderna de neumáticos de competición.
En conclusión, la estructura híbrida del 1,3-butadieno, con su sistema de electrones π deslocalizados, no es solo un concepto abstracto de un libro de texto. Es el plano molecular que da vida al componente más crítico de un coche de carreras. Es la ciencia invisible que separa una victoria gloriosa de una salida de pista, demostrando que en el motorsport, las carreras se ganan tanto en el laboratorio de química como en el asfalto del circuito.
Si quieres conocer otros artículos parecidos a 1,3-Butadieno: El Corazón del Neumático de F1 puedes visitar la categoría Automovilismo.