24/08/2019
En el vasto universo de la química orgánica, existen compuestos que, por su estructura y reactividad, se convierten en piezas clave para la síntesis de moléculas más complejas. Uno de estos protagonistas es el 1,3-Ciclohexadieno, un hidrocarburo cíclico que despierta el interés de químicos y estudiantes por igual. A simple vista, su fórmula C6H8 puede parecer sencilla, pero esconde una arquitectura molecular que le confiere propiedades únicas y un rol fundamental en reacciones emblemáticas como la de Diels-Alder. A lo largo de este artículo, desglosaremos en detalle su estructura, sus propiedades físicas y químicas, sus métodos de síntesis y su comparación con otros compuestos relacionados.
Estructura Molecular y Propiedades Físicas
Para entender al 1,3-Ciclohexadieno, primero debemos descifrar su nombre. "Ciclo" nos indica que se trata de una estructura en anillo. "Hexa" se refiere a que este anillo está formado por seis átomos de carbono. Finalmente, "dieno" revela la presencia de dos dobles enlaces, y los números "1,3" especifican sus posiciones. Así, tenemos un anillo de seis carbonos con dobles enlaces entre el carbono 1 y 2, y entre el carbono 3 y 4. Esta disposición de dobles enlaces alternados (separados por un enlace simple) se conoce como un sistema de dienos conjugados, lo cual es la clave de su estabilidad y reactividad particular.
A temperatura ambiente, este compuesto se presenta como un líquido incoloro, volátil y con un olor característico. Es un compuesto inflamable, lo que exige precauciones en su manejo. Su naturaleza insaturada, es decir, la presencia de dobles enlaces, lo hace significativamente más reactivo que su análogo saturado, el ciclohexano.
Tabla de Propiedades Clave
| Propiedad | Valor |
|---|---|
| Fórmula Molecular | C6H8 |
| Apariencia | Líquido incoloro |
| Naturaleza | Hidrocarburo cíclico insaturado |
| Índice de Refracción | 1.475 (a 20 °C) |
| Característica Estructural | Dienos conjugados |
Reactividad y Reacciones Notables
La reactividad del 1,3-Ciclohexadieno está dominada por sus dos dobles enlaces. Estos enlaces π son ricos en electrones, lo que los convierte en un objetivo para electrófilos. Sin embargo, la reacción más célebre en la que participa es, sin duda, la reacción de Diels-Alder. En esta poderosa cicloadición, el 1,3-Ciclohexadieno actúa como el "dieno" y reacciona con otra molécula que contiene un doble o triple enlace, llamada "dienófilo", para formar un nuevo anillo de seis miembros. Esta reacción es increíblemente valiosa en síntesis orgánica porque permite construir esqueletos de carbono complejos con un alto grado de control estereoquímico en un solo paso.
Además, su conversión a benceno es un proceso termodinámicamente favorable. La hidrogenación del 1,3-Ciclohexadieno para formar benceno y una molécula de hidrógeno (H2) es una reacción exotérmica, liberando aproximadamente 26.5 kJ/mol. Esto demuestra la increíble estabilidad del anillo aromático del benceno en comparación con el sistema de dienos conjugados del ciclohexadieno.
Comparativa Termodinámica
- Ciclohexano → 1,3-Ciclohexadieno + 2 H2: ΔH = +231.5 kJ/mol (Muy endotérmica)
- Ciclohexano → Benceno + 3 H2: ΔH = +205 kJ/mol (Endotérmica)
- 1,3-Ciclohexadieno → Benceno + H2: ΔH = -26.5 kJ/mol (Exotérmica)
Estos datos ilustran que, si bien se requiere energía para crear insaturaciones en el ciclohexano, la formación del sistema aromático del benceno a partir del dieno es un paso que libera energía, destacando la estabilidad única de la aromaticidad.
Síntesis y Comparación con Isómeros
El 1,3-Ciclohexadieno puede prepararse en el laboratorio a través de diversas rutas. Un método común es la doble deshidrobromación del 1,2-dibromociclohexano. En esta reacción, se utilizan bases fuertes para eliminar dos moléculas de bromuro de hidrógeno (HBr) del sustrato, generando los dos dobles enlaces en el anillo de ciclohexano.
Es importante no confundir el 1,3-Ciclohexadieno con su isómero, el 1,4-Ciclohexadieno. Aunque ambos comparten la misma fórmula molecular (C6H8), la disposición de sus dobles enlaces es diferente. En el isómero 1,4, los dobles enlaces están separados por dos enlaces simples, lo que los convierte en dienos aislados, no conjugados. Esta diferencia estructural tiene consecuencias directas en su estabilidad. El 1,3-Ciclohexadieno es aproximadamente 1.6 kJ/mol más estable que el 1,4-Ciclohexadieno. Esta mayor estabilidad se atribuye a la deslocalización de los electrones π a través del sistema conjugado, un efecto estabilizador que no está presente en el isómero 1,4.
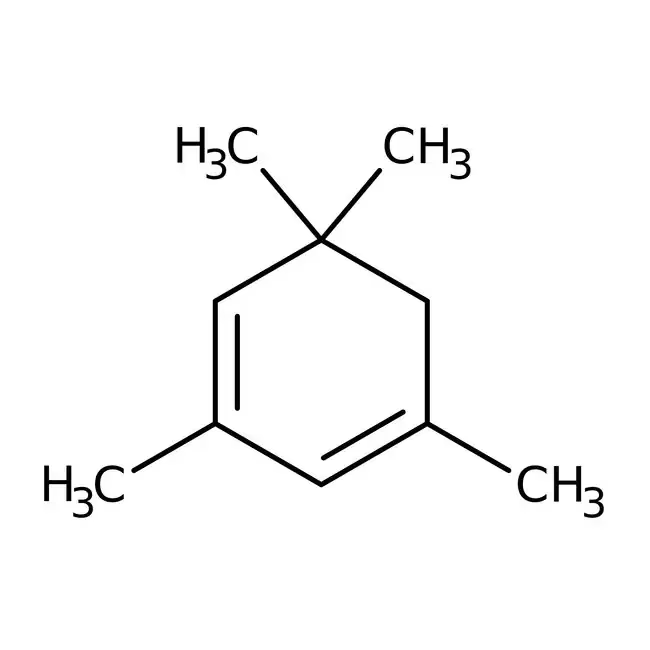
Derivados y Compuestos Relacionados: El 1,1,3-Trimetilciclohexano
Al explorar el mundo de los ciclohexanos, encontramos una gran variedad de derivados. Un ejemplo es el 1,1,3-Trimetilciclohexano. A diferencia del dieno, este compuesto es un alcano cíclico, es decir, está completamente saturado (no tiene dobles enlaces). Su nombre nos indica que tiene tres grupos metilo (-CH3) unidos al anillo de ciclohexano: dos en el carbono 1 y uno en el carbono 3. Su fórmula es C9H18.
Debido a su naturaleza saturada, es mucho menos reactivo que el 1,3-Ciclohexadieno. Su principal utilidad no reside en la síntesis, sino en el campo de la química analítica. Compuestos como este se fabrican con una pureza muy alta y se utilizan como materiales de referencia certificados o patrones analíticos. Estos patrones son cruciales para calibrar instrumentos como cromatógrafos de gases (GC) o espectrómetros de masas (MS), asegurando que los análisis de muestras desconocidas sean precisos y fiables. La información sobre su trazabilidad (por ejemplo, al NIST), certificaciones ISO y cumplimiento de normativas de seguridad (GHS/OSHA) es vital para los laboratorios que dependen de mediciones exactas.
Manejo y Seguridad
Como se mencionó, el 1,3-Ciclohexadieno es un líquido inflamable. Su manejo requiere tomar precauciones estándar para productos químicos orgánicos volátiles. Es fundamental trabajar en un área bien ventilada, como una campana de extracción de gases, para evitar la inhalación de vapores. Se debe mantener alejado de fuentes de ignición, como llamas abiertas, chispas o superficies calientes. El uso de equipo de protección personal (EPP), incluyendo guantes, gafas de seguridad y bata de laboratorio, es obligatorio para prevenir el contacto con la piel y los ojos.
Preguntas Frecuentes (FAQ)
¿Cuál es la principal diferencia entre el 1,3-ciclohexadieno y el benceno?
La principal diferencia radica en la aromaticidad. El benceno (C6H6) tiene un anillo de seis electrones π completamente deslocalizados en un sistema cíclico y plano, lo que le confiere una estabilidad excepcional. El 1,3-ciclohexadieno (C6H8) tiene solo cuatro electrones π en un sistema conjugado y no es aromático, lo que lo hace mucho más reactivo y propenso a reacciones de adición.
¿Por qué el 1,3-ciclohexadieno es más estable que el 1,4-ciclohexadieno?
Su mayor estabilidad se debe a la conjugación de sus dobles enlaces. En el isómero 1,3, los orbitales p de los cuatro carbonos involucrados en los dobles enlaces pueden solaparse, permitiendo que los electrones π se deslocalicen sobre esos cuatro átomos. Esta deslocalización reduce la energía total de la molécula, haciéndola más estable que el isómero 1,4, donde los dobles enlaces están aislados y no pueden interactuar de esta manera.
¿Qué es exactamente una reacción de Diels-Alder?
Es una reacción de cicloadición [4+2] entre un dieno conjugado (el componente de 4 electrones π, como el 1,3-ciclohexadieno) y un dienófilo (el componente de 2 electrones π). La reacción forma un nuevo anillo de seis miembros en un solo paso concertado. Es una de las herramientas más poderosas en síntesis orgánica para la construcción de anillos.
¿Es peligroso manipular el 1,3-Ciclohexadieno?
Como muchos solventes orgánicos, presenta riesgos si no se maneja adecuadamente. Es inflamable y sus vapores pueden ser irritantes. Sin embargo, siguiendo los protocolos de seguridad estándar de laboratorio (buena ventilación, EPP, evitar fuentes de ignición), se puede trabajar con él de forma segura.
Si quieres conocer otros artículos parecidos a 1,3-Ciclohexadieno: Estructura, Reactividad y Usos puedes visitar la categoría Automovilismo.

