05/05/2018
El rugido de los motores, el olor a goma quemada y el destello de los monoplazas a más de 300 km/h son la cara visible del automovilismo. Es un espectáculo de velocidad, habilidad y riesgo. Sin embargo, detrás de cada récord de vuelta, de cada adelantamiento al límite y de cada victoria, existe un universo invisible de ciencia y tecnología. Un mundo donde la química y la física dictan las reglas del juego. Hoy nos sumergiremos en ese mundo microscópico para analizar una reacción aparentemente simple pero con principios fundamentales que resuenan en el paddock: la adición de Bromuro de Hidrógeno (HBr) al 1-buteno. Puede sonar como algo sacado de un libro de texto, pero los conceptos que gobiernan esta reacción son los mismos que permiten a los ingenieros diseñar combustibles más eficientes, neumáticos con más agarre y materiales más ligeros y resistentes.

- Entendiendo a los Protagonistas: 1-Buteno y HBr
- La Reacción Clave: Un Baile Molecular con Reglas
- El Mecanismo Detallado: Paso a Paso Hacia la Victoria Molecular
- Tabla Comparativa de Productos: La Decisión en la Pista Molecular
- Del Laboratorio al Circuito: ¿Cómo se Aplican estos Principios?
- Preguntas Frecuentes (FAQ)
Entendiendo a los Protagonistas: 1-Buteno y HBr
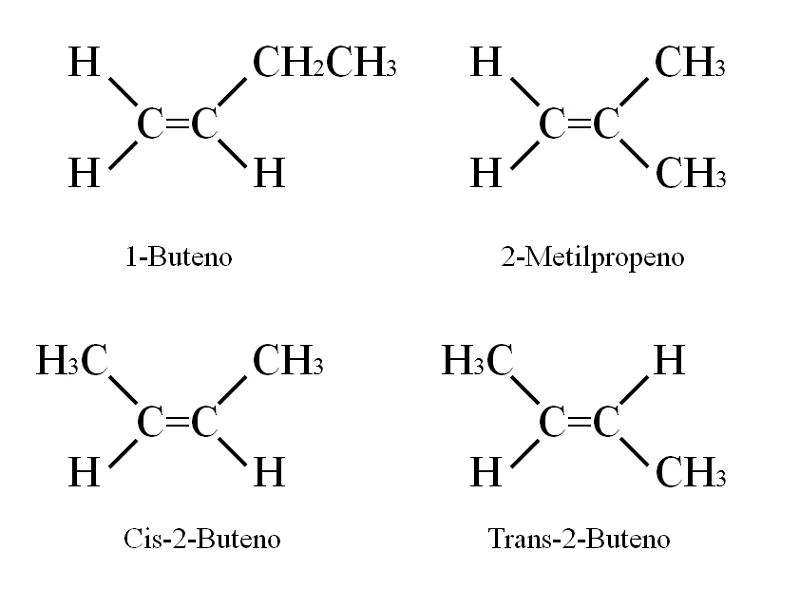
Para comprender la importancia de esta reacción en el motorsport, primero debemos conocer a sus actores. El 1-buteno (C4H8) es un hidrocarburo, específicamente un alqueno. Los hidrocarburos son el componente principal de la gasolina y otros combustibles fósiles que, con formulaciones muy avanzadas, impulsan a las bestias mecánicas que compiten en categorías como la Fórmula 1, el WRC o la NASCAR. El 1-buteno, con su doble enlace carbono-carbono, es una molécula reactiva, un bloque de construcción fundamental en la industria petroquímica.

Por otro lado, tenemos el Bromuro de Hidrógeno (HBr). Es un compuesto químico simple, un ácido fuerte. En el contexto de nuestra reacción, actúa como el "agresor" que romperá el doble enlace del buteno para formar una nueva molécula. Esta interacción, conocida como una reacción de adición electrofílica, es un pilar de la química orgánica y sus principios son cruciales para entender cómo se modifican y crean moléculas para obtener propiedades específicas, algo vital en la búsqueda de rendimiento en las carreras.
La Reacción Clave: Un Baile Molecular con Reglas
Cuando el 1-buteno y el HBr se encuentran, no reaccionan al azar. La química, como las carreras, tiene reglas estrictas. La más importante en este caso es la Regla de Markovnikov. Esta regla, formulada por el químico ruso Vladímir Markovnikov en 1870, dicta que en la adición de un reactivo como el HBr a un alqueno asimétrico, el átomo de hidrógeno se unirá al carbono del doble enlace que ya tiene más átomos de hidrógeno.
En el 1-buteno, el primer carbono del doble enlace tiene dos hidrógenos, mientras que el segundo carbono solo tiene uno. Siguiendo la regla de Markovnikov:
- El Hidrógeno (H+) del HBr se añadirá al primer carbono.
- El Bromo (Br-) se añadirá al segundo carbono.
El resultado principal de esta reacción no es el 1-bromobutano, como se podría pensar, sino el 2-bromobutano. Este producto es la clave para entender el siguiente nivel de complejidad de la reacción.
El Nacimiento de la Quiralidad: Un Concepto Crucial
Aquí es donde la química se vuelve fascinante y se conecta con conceptos de diseño y precisión. El producto de la reacción, el 2-bromobutano, tiene una propiedad muy especial: posee un carbono quiral. Un carbono quiral (o asimétrico) es un átomo de carbono que está enlazado a cuatro grupos o átomos diferentes. En el caso del 2-bromobutano, el segundo carbono está unido a:
- Un átomo de Hidrógeno (H)
- Un átomo de Bromo (Br)
- Un grupo metilo (-CH3)
- Un grupo etilo (-CH2CH3)
La presencia de este centro quiral significa que la molécula no es superponible con su imagen en un espejo, como nuestras manos. Esto da lugar a la existencia de dos versiones de la misma molécula, conocidas como isómeros ópticos o enantiómeros. Son químicamente casi idénticos, pero desvían la luz polarizada en direcciones opuestas. Aunque en esta reacción se producen ambos en una mezcla 50/50 (mezcla racémica), el concepto de quiralidad es vital en la fabricación de fármacos y, en el automovilismo, en el diseño de polímeros y aditivos con estructuras tridimensionales muy específicas para lograr un rendimiento óptimo.
El Mecanismo Detallado: Paso a Paso Hacia la Victoria Molecular
Entender el "porqué" de la Regla de Markovnikov nos lleva al mecanismo de la reacción, una secuencia de eventos que ocurren en una fracción de segundo, similar a la secuencia de acciones de un piloto en una curva.
- Ataque al Protón: El doble enlace del 1-buteno es rico en electrones. Es atraído por el protón (H+) del HBr, que es pobre en electrones. Los electrones del doble enlace "atacan" al hidrógeno, rompiendo el enlace H-Br.
- Formación del Carbocatión: Este ataque forma un enlace carbono-hidrógeno y deja al otro carbono del antiguo doble enlace con una carga positiva. Este intermediario se llama carbocatión. Aquí es donde se decide la carrera: si el hidrógeno se une al primer carbono, se forma un carbocatión secundario (la carga positiva está en el segundo carbono). Si se uniera al segundo carbono, se formaría un carbocatión primario. Los carbocationes secundarios son mucho más estables que los primarios, por lo que esta ruta es la que se sigue de forma abrumadoramente mayoritaria. Esta mayor estabilidad es la explicación electrónica de la Regla de Markovnikov.
- Ataque del Bromuro: El ion bromuro (Br-), que quedó libre en el primer paso, ahora tiene una carga negativa y es atraído por el carbocatión positivo. Ataca a este carbono cargado, formando el enlace final carbono-bromo.
Este proceso, que favorece al intermediario más estable, es un principio fundamental en química. En el motorsport, la búsqueda de la estabilidad es constante: estabilidad aerodinámica, estabilidad del compuesto del neumático a altas temperaturas, estabilidad del lubricante bajo presión extrema. El principio es el mismo: los sistemas tienden al estado más estable posible.

Tabla Comparativa de Productos: La Decisión en la Pista Molecular
| Característica | Producto Mayoritario (2-bromobutano) | Producto Minoritario (1-bromobutano) |
|---|---|---|
| Vía de Reacción | A través del carbocatión secundario | A través del carbocatión primario |
| Estabilidad del Intermediario | Alta | Baja |
| Centro Quiral | Sí, en el Carbono 2 | No |
| Abundancia Relativa | ~90% o más | ~10% o menos |
Del Laboratorio al Circuito: ¿Cómo se Aplican estos Principios?
Nadie está añadiendo HBr al combustible de un coche de IndyCar, pero los principios que hemos discutido son la base de tecnologías que sí están en la pista.
- Combustibles de Competición: La comprensión de la estabilidad de los hidrocarburos y sus isómeros es clave para diseñar combustibles con alto índice de octanaje. Combustibles que resisten la detonación (autoencendido) bajo la inmensa compresión de un motor de carreras. La ramificación de las cadenas de hidrocarburos, un concepto relacionado con la estabilidad de los carbocationes, es una estrategia para aumentar este octanaje.
- Polímeros y Materiales Compuestos: Los alquenos como el buteno son monómeros, los ladrillos para construir polímeros. La polimerización es una serie de reacciones de adición. Los plásticos, las fibras de aramida (Kevlar) y las resinas que unen la fibra de carbono en un chasis de F1 se crean mediante procesos químicos complejos donde controlar la estructura molecular es fundamental para obtener la rigidez y ligereza deseadas.
- Neumáticos: La fabricación de caucho sintético para los neumáticos de competición es un arte químico. Se combinan diferentes monómeros en procesos de polimerización para crear compuestos con propiedades muy específicas de agarre, durabilidad y comportamiento a diferentes temperaturas. La química de adición es el corazón de este proceso.
Preguntas Frecuentes (FAQ)
¿Por qué es más estable un carbocatión secundario que uno primario?
La estabilidad de un carbocatión se debe al efecto de "hiperconjugación". Los grupos alquilo vecinos (como los grupos metilo y etilo) pueden "donar" densidad electrónica al carbono con carga positiva, ayudando a estabilizarlo. Un carbocatión secundario tiene dos grupos alquilo vecinos haciendo esto, mientras que uno primario solo tiene uno. Más ayuda significa más estabilidad.
¿Qué aplicación práctica tienen los isómeros ópticos en el motorsport?
Aunque en esta reacción específica no es un factor controlable, en la síntesis de aditivos para aceites o polímeros avanzados, controlar la quiralidad puede llevar a materiales con estructuras tridimensionales precisas. Esto puede influir en cómo las moléculas interactúan entre sí, afectando propiedades como la viscosidad de un lubricante o la elasticidad de un polímero en un neumático.
¿Cómo se obtiene el HBr para usarlo en un laboratorio?
El Bromuro de Hidrógeno es un gas corrosivo. Generalmente, se compra disuelto en ácido acético o agua, o se genera "in situ" (en el momento de la reacción) a partir de la reacción de un bromuro de sal, como el bromuro de sodio (NaBr), con un ácido fuerte no volátil como el ácido sulfúrico o el ácido fosfórico.
En conclusión, la próxima vez que veas un coche de carreras devorando el asfalto, recuerda que debajo del capó y en la misma estructura del coche, hay un mundo de química en acción. Reacciones como la adición de HBr a 1-buteno, aunque no ocurran literalmente en la pista, nos enseñan los principios fundamentales de estabilidad, selectividad y estructura molecular que los ingenieros explotan para llevar la tecnología del automovilismo al límite absoluto. Es la ciencia invisible que separa a los contendientes de los campeones.
Si quieres conocer otros artículos parecidos a Química en la Pista: La Reacción de Buteno y HBr puedes visitar la categoría Automovilismo.