05/03/2019
En el vertiginoso mundo del automovilismo deportivo, a menudo centramos nuestra atención en la aerodinámica, la pericia del piloto o la potencia bruta del motor. Sin embargo, una de las batallas más cruciales y científicamente complejas se libra a nivel molecular, oculta en el interior del tanque de combustible. La gasolina que impulsa a un monoplaza de Fórmula 1 o a un coche del WRC no es la misma que usamos en nuestros vehículos de calle; es un cóctel químico diseñado con precisión milimétrica para extraer hasta la última milésima de segundo en la pista. Para entender esta ciencia, debemos sumergirnos en la química de la combustión, donde moléculas como el buteno juegan un papel fundamental, siendo protagonistas silenciosos del rendimiento extremo.

¿Qué es el Buteno y por qué es Clave en el Motorsport?
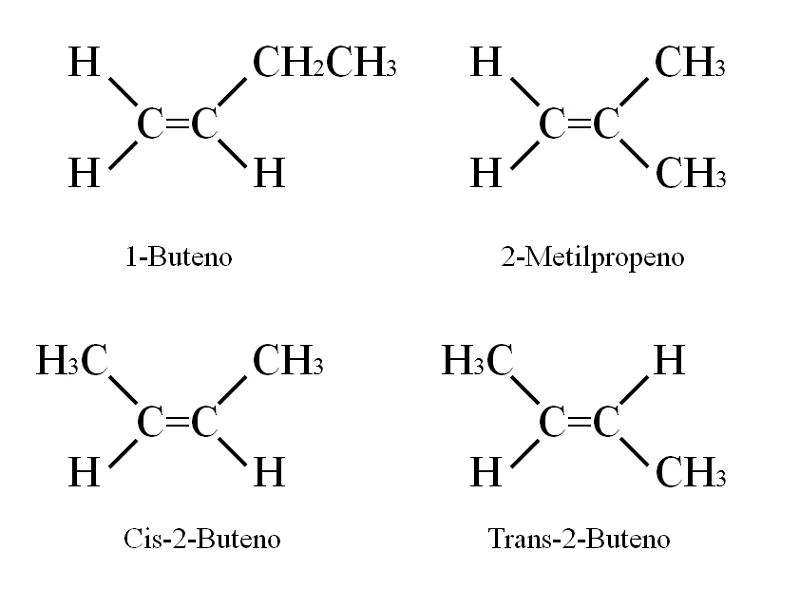
Para el aficionado común, un combustible es simplemente un líquido que hace funcionar un motor. Para un ingeniero de Ferrari o Mercedes-AMG Petronas, es un campo de estudio vital. El buteno es un hidrocarburo insaturado, específicamente un alqueno, con la fórmula química C4H8. Lo fascinante del buteno es que no es una única molécula, sino que existe en varias formas estructurales llamadas isómeros: 1-buteno, cis-2-buteno, trans-2-buteno e isobuteno. Cada uno de estos isómeros, a pesar de compartir la misma fórmula, se comporta de manera diferente durante la combustión.
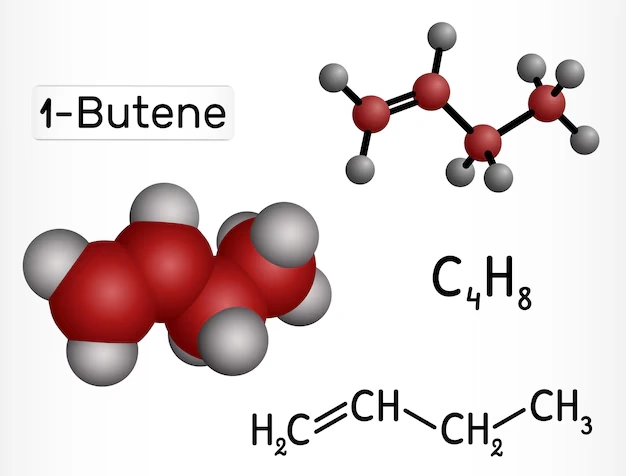
En el contexto de los combustibles de alto rendimiento, los isómeros de buteno son cruciales por dos razones. Primero, son productos intermedios clave en la pirólisis (descomposición por calor) y oxidación de los hidrocarburos más grandes y complejos que componen la gasolina de competición. Segundo, su propia química de combustión revela principios fundamentales sobre cómo liberar energía de manera eficiente y controlada. Entender cómo se quema el 1-buteno, por ejemplo, ayuda a los científicos a predecir y optimizar la combustión de mezclas de combustible mucho más complejas, impactando directamente en la potencia y la eficiencia del motor.
La Reactividad: El Delicado Equilibrio entre Potencia y Control
No todos los combustibles se queman igual. La "reactividad" es un término que describe la facilidad y velocidad con la que un compuesto químico reacciona, en este caso, con el oxígeno durante la combustión. Estudios detallados sobre los isómeros de buteno han demostrado que su reactividad varía significativamente.
Investigaciones han revelado que la reactividad de estos isómeros aumenta en el siguiente orden: isobuteno (el menos reactivo), 2-buteno y 1-buteno (el más reactivo). Esta diferencia no es trivial. Un combustible más reactivo puede liberar su energía más rápidamente, lo que podría traducirse en más potencia. Sin embargo, una reactividad excesiva o descontrolada es el enemigo número uno de un motor de alto rendimiento: provoca la temida "detonación" o "picado de bielas" (engine knock), un fenómeno destructivo donde la mezcla aire-combustible explota de forma prematura y violenta en lugar de quemarse suavemente. Por lo tanto, el objetivo de los ingenieros de combustible no es simplemente maximizar la reactividad, sino ajustarla con precisión para las condiciones extremas de presión y temperatura de un motor de carreras.
Tabla Comparativa de Reactividad de Isómeros de Buteno
| Isómero | Nivel de Reactividad | Temperatura de Ignición | Implicación en Motorsport |
|---|---|---|---|
| Isobuteno | Baja | La más alta | Componente útil para aumentar la resistencia a la detonación (mayor octanaje). |
| 2-Buteno (cis y trans) | Media | Intermedia | Aporta un equilibrio entre estabilidad y liberación de energía. |
| 1-Buteno | Alta | La más baja | Puede mejorar la velocidad de la llama, pero debe usarse con cuidado para evitar la detonación. |
El Infierno Químico dentro del Cilindro
Dentro de un cilindro de un motor de F1, las temperaturas pueden superar los 2,500 °C. En estas condiciones, la química se vuelve un caos controlado. La combustión a alta temperatura del buteno nos enseña que las moléculas de combustible no simplemente se queman; son destrozadas violentamente. Los enlaces C-C (carbono-carbono) y C-H (carbono-hidrógeno) se rompen, generando una sopa de fragmentos moleculares altamente reactivos conocidos como "radicales libres" (como ȮH, Ḣ, ĊH₃).
El comportamiento de estos radicales es el verdadero secreto del rendimiento. Reacciones como la "abstracción de átomos de hidrógeno" por parte de radicales hidroxilo (ȮH) son fundamentales. Curiosamente, estas reacciones pueden tanto promover como inhibir la reactividad general del sistema. Por ejemplo, al consumir un radical ȮH muy reactivo para formar un radical estabilizado por resonancia (como el Ċ₄H₇), la reacción general se ralentiza, inhibiendo la combustión. Los químicos de combustible manipulan la composición de la gasolina para controlar precisamente qué radicales se forman y cómo reaccionan, ajustando la velocidad de la combustión en cada fase del ciclo del motor para una entrega de potencia óptima.
La Ciencia del Control: Evitando la Catástrofe a Bajas y Medias Temperaturas
Si bien las altas temperaturas son sinónimo de potencia máxima, la fase de compresión, a temperaturas más bajas e intermedias (por debajo de 850 °C), es igual de crítica. Es aquí donde se gesta la detonación. La química a baja temperatura es dominada por reacciones de adición, donde los radicales (como el ȮH) se añaden a la molécula de combustible en lugar de romperla.

Estos procesos son la base de la química de "baja temperatura", que puede llevar a una ramificación de la cadena de reacciones que acelera drásticamente la combustión. En el caso del 1-buteno, la adición de un radical ȮH puede iniciar una cascada de reacciones con el oxígeno que promueven una ignición muy rápida. Controlar esta química es la esencia de los combustibles de alto octanaje. Los aditivos y las estructuras moleculares específicas están diseñados para interferir en estas cascadas de reacciones a baja temperatura, aumentando el "tiempo de retardo de la ignición" (ignition delay time) y permitiendo que el motor opere con relaciones de compresión mucho más altas sin riesgo de detonación. Esta es la ciencia que permite a los motores modernos de F1 ser tan eficientemente potentes.
Preguntas Frecuentes (FAQ)
- ¿Por qué los equipos de F1 desarrollan su propio combustible?
Porque el combustible es una parte integral del diseño de la unidad de potencia. Los equipos trabajan con socios petroleros (como Shell con Ferrari o Petronas con Mercedes) para crear mezclas a medida que se adaptan perfectamente a las características de su motor, optimizando la potencia, la eficiencia y la fiabilidad, siempre dentro de las estrictas regulaciones de la FIA.
- ¿Qué es el "octanaje" y cómo se relaciona con esta química?
El octanaje es una medida estándar de la resistencia de un combustible a la detonación o autoignición. Un combustible de alto octanaje resiste mejor las altas presiones y temperaturas durante la compresión. Esto se logra a través de una formulación química, usando compuestos como el isobuteno, que inhiben las reacciones en cadena de baja temperatura que conducen a la ignición prematura.
- ¿La gasolina de un auto de NASCAR es diferente a la de un F1?
Sí, son muy diferentes. Las regulaciones y las tecnologías de motor son distintas. Los motores V8 de NASCAR utilizan un combustible con especificaciones diferentes a las de las complejas unidades de potencia híbridas V6 turbo de la F1. Mientras los principios químicos de la combustión son universales, la formulación específica del combustible se adapta a las necesidades de cada categoría.
- Finalmente, ¿cuál es la fórmula química del 1-buteno?
La fórmula química tanto del 1-buteno como de todos sus isómeros es C4H8. Está compuesto por cuatro átomos de carbono y ocho átomos de hidrógeno.
En conclusión, la próxima vez que veas un coche de carreras rugiendo en la pista, recuerda que la proeza no es solo mecánica, sino profundamente química. La danza molecular de compuestos como el buteno, su reactividad controlada y su compleja descomposición bajo calor y presión extremos son los que verdaderamente desatan la furia contenida en cada gota de combustible. Es una disciplina donde la química más avanzada se traduce directamente en velocidad, y donde la comprensión de estas reacciones fundamentales puede marcar la diferencia entre la victoria y la derrota.
Si quieres conocer otros artículos parecidos a La Química Secreta del Combustible de Competición puedes visitar la categoría Automovilismo.