26/05/2024
En el corazón de cada motor rugiente, desde el V6 híbrido de un monoplaza de Fórmula 1 hasta el motor de un auto de Turismo Carretera, yace un principio fundamental que gobierna el universo entero: la Primera Ley de la Termodinámica. A menudo resumida como la ley de conservación de la energía, esta regla no solo es un pilar de la física, sino la base que nos permite comprender cómo convertimos el calor de una combustión en el movimiento vertiginoso que nos apasiona en las pistas. Es la ciencia que explica cómo la energía no se crea ni se destruye, simplemente se transforma, y entender su fórmula es el primer paso para dominar el lenguaje del rendimiento y la eficiencia en el motorsport.

¿Qué es la Primera Ley de la Termodinámica?
La Primera Ley de la Termodinámica es una afirmación universal sobre la naturaleza de la energía. Establece que el cambio en la energía interna de un sistema es igual a la suma del calor agregado al sistema y el trabajo realizado sobre el sistema. En esencia, nos dice que la energía no puede aparecer de la nada ni desaparecer en la nada; solo puede cambiar de forma. Por ejemplo, la energía química almacenada en el combustible se convierte en energía térmica (calor) durante la combustión, la cual a su vez se convierte en energía mecánica (trabajo) para mover los pistones y, finalmente, las ruedas.

Para cualquier proceso, existe una función de estado llamada energía interna, denotada como E. El cambio en esta energía (ΔE) depende exclusivamente de los estados termodinámicos inicial y final del sistema, sin importar el camino o los pasos intermedios que se tomaron para llegar de uno a otro.
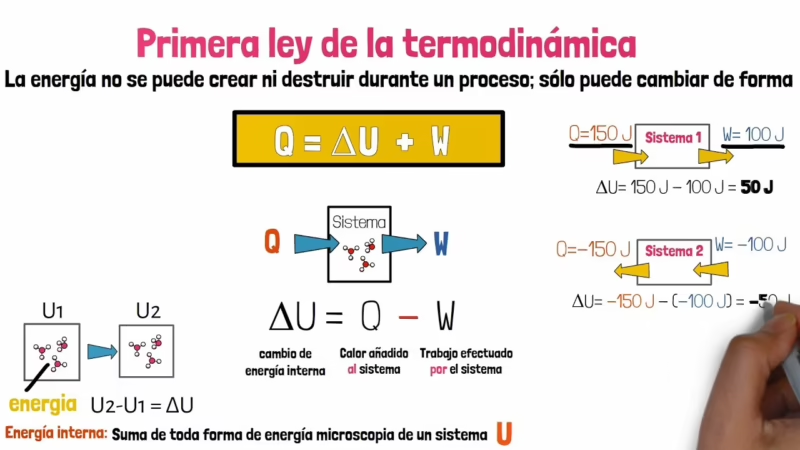
La Fórmula Clave: ΔE = Q + W
La expresión matemática que encapsula esta ley fundamental es engañosamente simple, pero inmensamente poderosa:
ΔE = Q + W
Donde:
- ΔE: Representa el cambio en la energía interna del sistema. Es la diferencia entre la energía interna final (Ef) y la energía interna inicial (Ei).
- Q: Es el calor transferido al sistema. Por convención, si el calor fluye hacia el sistema, Q es positivo (el sistema se calienta). Si el calor sale del sistema, Q es negativo (el sistema se enfría).
- W: Es el trabajo realizado sobre el sistema. Si el entorno realiza trabajo sobre el sistema (por ejemplo, comprimiendo un gas), W es positivo. Si el sistema realiza trabajo sobre su entorno (por ejemplo, un gas en expansión que empuja un pistón), W es negativo.
Es crucial notar que, si bien la suma de Q y W (es decir, ΔE) es siempre la misma para un cambio de estado dado, los valores individuales de Q y W pueden variar enormemente dependiendo de cómo se realice el proceso. Esto nos lleva a una distinción fundamental.
Funciones de Estado vs. Funciones de Trayectoria
La diferencia más importante que revela la Primera Ley es la que existe entre funciones de estado y funciones de trayectoria. La energía interna (E) es una función de estado. Esto significa que su valor solo depende de la condición actual del sistema (su temperatura, presión, volumen, etc.), no de cómo llegó a esa condición. Una analogía útil es la altitud: la diferencia de altitud entre la cima y la base de una montaña es siempre la misma, sin importar si subiste por el camino más corto y empinado o por uno largo y sinuoso.
Por otro lado, el calor (Q) y el trabajo (W) son funciones de trayectoria. Sus valores dependen del camino específico seguido durante un proceso. Usando la misma analogía, la cantidad de energía (y sudor) que gastas para subir la montaña depende totalmente de la ruta que elijas. Del mismo modo, la cantidad de calor y trabajo intercambiados en un proceso termodinámico depende de la "ruta" termodinámica.
Tabla Comparativa
| Característica | Función de Estado (Energía Interna) | Función de Trayectoria (Calor, Trabajo) |
|---|---|---|
| Dependencia | Solo del estado inicial y final del sistema. | Del camino o proceso específico seguido. |
| Ejemplo Analógico | La diferencia de altitud entre dos puntos. | La distancia recorrida para ir entre esos dos puntos. |
| Símbolo Diferencial | dE (diferencial exacto) | đQ, đW (diferencial inexacto) |
El Proceso Adiabático: La Vía para Medir la Energía
Una de las implicaciones más fascinantes de la Primera Ley surge cuando consideramos un proceso adiabático. Un proceso es adiabático cuando no hay transferencia de calor entre el sistema y su entorno, es decir, Q = 0. Esto se logra aislando térmicamente el sistema, como dentro de un termo ideal o en procesos que ocurren tan rápidamente que no hay tiempo para que el calor se transfiera.
Bajo estas condiciones, la fórmula de la Primera Ley se simplifica enormemente:
ΔE = Wa
Esto es increíblemente útil. Nos dice que el cambio en la energía interna de un sistema durante un proceso adiabático es exactamente igual al trabajo realizado sobre él. Esta es una experiencia fundamental de la humanidad: el trabajo realizado en condiciones de aislamiento térmico (Wa) para llevar un sistema de un estado inicial a uno final es independiente del tipo de trabajo realizado y del camino seguido. Por lo tanto, nos proporciona un método directo y experimental para medir el cambio en una función de estado (ΔE) midiendo una cantidad dependiente de la trayectoria (W) bajo la condición específica de Q=0.
La Importancia Crítica de Definir el Sistema y su Entorno
Los ejemplos teóricos a menudo pueden ser confusos si no se tiene un cuidado extraordinario en definir qué constituye el "sistema" y qué constituye el "entorno". El cálculo del trabajo y la interpretación de los cambios de energía dependen por completo de dónde trazamos la frontera imaginaria.
Ejemplo: La Expansión Libre de un Gas
Imaginemos un contenedor rígido y adiabático dividido en dos compartimentos. Uno contiene un gas (A) y el otro está vacío (B). Si quitamos la división, el gas se expande para ocupar todo el volumen (A+B). ¿Qué trabajo se ha realizado? La respuesta depende de cómo definamos el sistema.
- Si el sistema es todo el contenedor (A+B): Como el contenedor está aislado, no hay intercambio de calor (Q=0) ni de trabajo con el exterior (las paredes no se mueven, W=0). Por lo tanto, ΔE = 0. La energía interna total del gas no ha cambiado, aunque su presión y temperatura sí lo hayan hecho.
- Si el sistema fuera solo el volumen A: La definición se complica, ya que el gas abandona el sistema. Este se convierte en un sistema abierto, cuyas reglas son más complejas.
Este ejemplo demuestra que para un sistema aislado, la energía se conserva, sin importar los procesos internos que ocurran.
Aplicaciones en el Automovilismo Deportivo
El motor de combustión interna es un sistema termodinámico abierto en su máxima expresión. La Primera Ley está en acción en cada ciclo:
- Admisión: La mezcla de aire y combustible entra en el cilindro.
- Compresión: El pistón sube, realizando trabajo sobre el gas (W > 0), lo que aumenta su energía interna y temperatura.
- Combustión (Expansión): La chispa enciende la mezcla, liberando una enorme cantidad de energía química como calor (Q > 0 para el gas). Este calor aumenta drásticamente la presión, y el gas se expande, empujando el pistón hacia abajo. Aquí, el sistema (el gas) realiza trabajo sobre el entorno (el pistón) (W < 0). Este es el trabajo útil que impulsa el coche.
- Escape: Los gases quemados son expulsados.
La eficiencia de un motor se reduce a cuán efectivamente puede convertir el calor (Q) de la combustión en trabajo útil (W). Las pérdidas de calor a través de las paredes del cilindro y el sistema de escape son inevitables, y minimizar estas pérdidas mientras se maximiza el trabajo extraído es el objetivo principal de la ingeniería de motores, todo gobernado por la Primera Ley de la Termodinámica.
Preguntas Frecuentes (FAQ)
¿La Primera Ley de la Termodinámica es lo mismo que la conservación de la energía?
Sí, en esencia, la Primera Ley es la aplicación del principio de conservación de la energía a los sistemas termodinámicos, donde la energía puede manifestarse como energía interna, calor y trabajo.
¿Por qué a veces la fórmula se escribe como ΔE = Q - W?
Es una simple cuestión de convención. La fórmula ΔE = Q + W es común en química y algunas ramas de la física, donde W se define como el trabajo realizado *sobre* el sistema. En muchas ramas de la ingeniería y la física, se prefiere la fórmula ΔE = Q - W, donde W se define como el trabajo realizado *por* el sistema sobre su entorno. Ambas son correctas, siempre que se sea consistente con la definición de W.
¿Qué es una "función de estado" en términos simples?
Es una propiedad de un sistema que depende únicamente de su estado actual, no de la historia de cómo llegó a ese estado. La temperatura, la presión, el volumen y la energía interna son funciones de estado. Piensa en tu ubicación GPS: solo describe dónde estás ahora, no la ruta que tomaste para llegar allí.
¿Se puede medir la energía interna total de un sistema?
No, no existe una forma de medir el valor absoluto de la energía interna de un sistema. La termodinámica solo se ocupa de los *cambios* en la energía interna (ΔE), que sí pueden medirse o calcularse, por ejemplo, a través del trabajo adiabático. Este hecho no tiene consecuencias prácticas, ya que son las diferencias de energía las que impulsan todos los procesos.
Si quieres conocer otros artículos parecidos a Primera Ley de la Termodinámica: Fórmula y Claves puedes visitar la categoría Automovilismo.