21/05/2018
En el vertiginoso mundo del automovilismo deportivo, cada milisegundo cuenta. La aerodinámica, la habilidad del piloto y la estrategia de equipo son cruciales, pero existe un héroe invisible que ruge en el corazón de cada motor: el combustible. Lejos de ser la gasolina que usamos en nuestros coches de calle, el combustible de competición es una pócima de alta tecnología, una mezcla compleja diseñada para extraer hasta la última gota de rendimiento. En este artículo, nos sumergiremos en el fascinante mundo de la química del motorsport, desglosando las moléculas que marcan la diferencia entre la victoria y la derrota, y explorando compuestos clave como el 2,3,3-trimetilpentano y sus parientes químicos.

- ¿Qué es el Índice de Octano y por qué Obsesiona a los Ingenieros?
- Los Alquinos Ramificados: Héroes Anónimos del Combustible
- Análisis de Isómeros: El Poder de la Estructura
- ¿Y qué pasa con los Alquenos? El 2,3,3-Trimetil-1-Buteno
- De la Molécula a la Pista: La Alquimia Final
- Preguntas Frecuentes (FAQ)
¿Qué es el Índice de Octano y por qué Obsesiona a los Ingenieros?
Antes de analizar moléculas específicas, es fundamental entender un concepto clave: el índice de octano. En términos sencillos, el octanaje mide la capacidad de un combustible para resistir la compresión en un motor sin detonar prematuramente. Esta detonación, conocida como "picado de bielas" o "knocking", es una combustión incontrolada y explosiva que puede dañar gravemente el motor y reducir drásticamente su potencia.

Los motores de alto rendimiento, como los de un Fórmula 1 o un coche de WRC, operan con relaciones de compresión extremadamente altas para maximizar la eficiencia y la potencia. Para evitar la detonación, necesitan un combustible con un octanaje muy elevado. Mientras que la gasolina comercial suele tener entre 95 y 98 octanos, los combustibles de competición pueden superar los 102 octanos, gracias a una formulación precisa donde la estructura molecular de sus componentes es la gran protagonista.
Los Alquinos Ramificados: Héroes Anónimos del Combustible
Aquí es donde la química orgánica entra en juego. No todos los hidrocarburos son iguales. La clave para un alto octanaje reside en la estructura de las moléculas. Los alcanos de cadena larga y lineal tienden a detonar fácilmente (bajo octanaje), mientras que los alcanos altamente ramificados son mucho más estables y resistentes a la compresión (alto octanaje).
El Caso del 2,2,3-Trimetilbutano (Triptano)
Un ejemplo paradigmático es el 2,2,3-Trimetilbutano, también conocido como Triptano. Este compuesto es un alcano de cadena ramificada (fórmula molecular C7H16) que presenta un esqueleto de butano con tres grupos metilo unidos a los carbonos 2 y 3. Este alto grado de ramificación le confiere propiedades excepcionales:
- Alto Índice de Octano: El Triptano tiene un índice de octano de investigación (RON) superior a 112, lo que lo convierte en un componente extremadamente valioso para formular gasolinas de alto rendimiento, como los combustibles de aviación (Avgas) y, por supuesto, de competición.
- Estabilidad: Es una molécula relativamente estable y no polar, lo que garantiza un comportamiento predecible dentro del motor.
- Volatilidad: Su estructura compacta le otorga un punto de ebullición relativamente bajo en comparación con alcanos de peso similar, lo que influye en la forma en que se vaporiza y mezcla con el aire en la cámara de combustión.
Su capacidad para mejorar el rendimiento del combustible y reducir el golpeteo del motor lo ha convertido en un aditivo de élite en la búsqueda de la potencia pura.
Análisis de Isómeros: El Poder de la Estructura
En química, los isómeros son moléculas que tienen la misma fórmula molecular pero diferentes arreglos de átomos. En el mundo de los combustibles, esta diferencia estructural es abismal en términos de rendimiento. Tomemos como ejemplo el 2,3,3-trimetilpentano.

El 2,3,3-Trimetilpentano: Otro Campeón del Octanaje
Este compuesto es un isómero del octano, lo que significa que su fórmula molecular es C8H18. Al igual que el Triptano, su nombre nos indica una estructura altamente ramificada: una cadena principal de cinco carbonos (pentano) con tres grupos metilo adicionales. Esta ramificación es, una vez más, la clave de su excelente comportamiento antidetonante.
La fórmula semidesarrollada del 2,3,3-trimetilpentano es: CH3-CH(CH3)-C(CH3)2-CH2-CH3.
A continuación, una tabla comparativa con algunas de sus propiedades y las del Triptano para ilustrar las sutiles pero importantes diferencias.
| Característica | 2,3,3-Trimetilpentano | 2,2,3-Trimetilbutano (Triptano) |
|---|---|---|
| Fórmula Molecular | C8H18 | C7H16 |
| Masa Molar | 114,23 g/mol | 100,21 g/mol |
| Estructura Base | Cadena de Pentano | Cadena de Butano |
| Punto de Fusión | 172 K (−101 °C) | 248 K (-25 °C) |
| Propiedad Clave | Excelente componente antidetonante para gasolinas. | Índice de octano extremadamente alto, usado como aditivo premium. |
¿Y qué pasa con los Alquenos? El 2,3,3-Trimetil-1-Buteno
No todo en el combustible son alcanos. Ocasionalmente, otros tipos de hidrocarburos, como los alquenos, pueden estar presentes. Los alquenos se caracterizan por tener al menos un doble enlace carbono-carbono en su estructura. Un ejemplo es el 2,3,3-trimetilbut-1-eno.
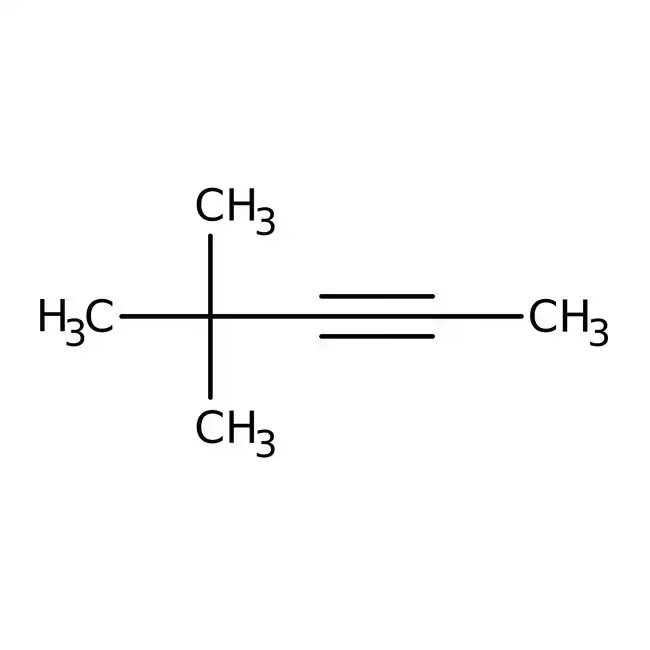
Este compuesto tiene la fórmula molecular C7H14. La presencia del doble enlace lo hace "insaturado" y, por lo general, más reactivo que su contraparte alcano (el Triptano, en este caso). Si bien su reactividad puede ser útil en ciertos procesos químicos, en un combustible de motor puede ser una desventaja, ya que podría llevar a la formación de gomas y depósitos indeseados. Por esta razón, los combustibles de competición suelen estar compuestos principalmente por alcanos y compuestos aromáticos muy estables.
Datos Técnicos del 2,3,3-Trimetilbut-1-eno:
- Nombre IUPAC: 2,3,3-trimethylbut-1-ene
- Fórmula Molecular: C7H14
- Masa Molar: 98.19 g/mol
- InChI: InChI=1S/C7H14/c1-6(2)7(3,4)5/h1H2,2-5H3
- CAS Number: 594-56-9
De la Molécula a la Pista: La Alquimia Final
Un combustible de Fórmula 1 o de Le Mans no es una sola sustancia, sino una mezcla cuidadosamente orquestada de hasta 200 componentes diferentes. Los químicos e ingenieros de petroleras como Shell, Petronas o Mobil 1 trabajan codo a codo con los equipos para desarrollar formulaciones a medida.
Utilizan una base de hidrocarburos de alto octanaje, como los isómeros ramificados que hemos visto, y añaden un cóctel de aditivos: oxigenantes (para una combustión más completa), detergentes (para mantener limpios los inyectores), modificadores de fricción y otros compuestos secretos. Cada mezcla se ajusta para un motor específico, las condiciones de la pista (altitud, humedad) y las regulaciones de la FIA, que son cada vez más estrictas en cuanto a la sostenibilidad y composición de los combustibles.
Preguntas Frecuentes (FAQ)
- ¿Por qué los combustibles de carrera no se usan en autos de calle?
- Principalmente por tres razones: su altísimo costo de producción, su formulación específica para motores que operan en condiciones extremas (altas revoluciones y temperaturas) que no se dan en la conducción normal, y porque a menudo no están diseñados para la durabilidad a largo plazo que requiere un vehículo de calle.
- ¿Qué significa "fórmula semidesarrollada"?
- Es una forma de representar una molécula química que muestra los átomos de carbono y los átomos unidos a ellos, pero sin detallar los enlaces de cada átomo de hidrógeno. Por ejemplo, en lugar de dibujar cada enlace en un grupo metilo, simplemente se escribe CH3. Es un punto intermedio entre la fórmula molecular (C8H18) y la fórmula desarrollada (que muestra todos los enlaces).
- ¿Todos los equipos de F1 usan el mismo combustible?
- No. Cada equipo tiene un socio técnico que le suministra combustible y lubricantes. Por ejemplo, Ferrari trabaja con Shell y Mercedes con Petronas. Estos socios desarrollan mezclas únicas y exclusivas, lo que convierte al combustible en un área clave de competencia técnica y una fuente de ventaja competitiva.
En conclusión, la próxima vez que veas un auto de carreras rugiendo en la pista, recuerda que su increíble velocidad no solo proviene de la aerodinámica y la potencia del motor, sino también de la danza invisible de moléculas como el 2,3,3-trimetilpentano. Es un recordatorio de que en el motorsport, la victoria se cocina tanto en el laboratorio como en el asfalto. La química, en su forma más pura y potente, es el verdadero combustible de los campeones.
Si quieres conocer otros artículos parecidos a La Química de la Velocidad: El Combustible Secreto puedes visitar la categoría Automovilismo.
