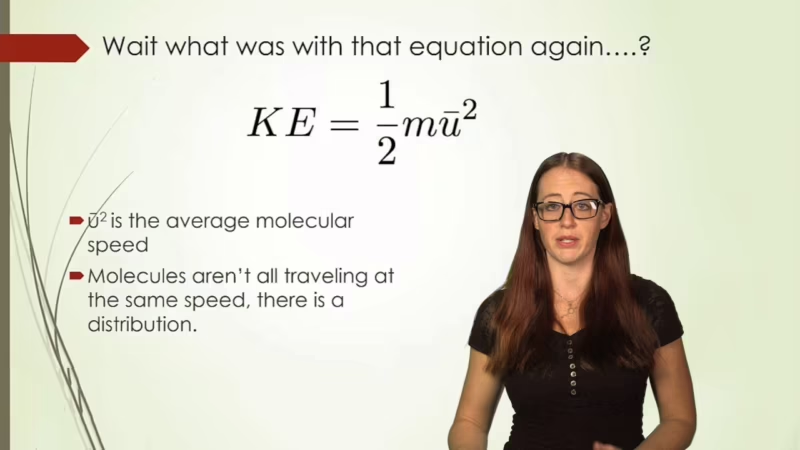26/09/2025
Cuando escuchamos a un piloto de Fórmula 1 quejarse por la radio de que sus neumáticos no están "en la ventana de temperatura", o a un ingeniero discutir las presiones de inflado con una precisión milimétrica, no siempre somos conscientes de la increíble ciencia que se esconde detrás de esas conversaciones. No se trata de magia ni de sensaciones abstractas, sino de física pura y dura. En el corazón de estos fenómenos se encuentra la Teoría Cinético-Molecular de los gases, un modelo que, aunque describe el comportamiento de gases "ideales" teóricos, es fundamental para entender y predecir cómo se comportará un coche de carreras en el mundo real.
- ¿Qué es un Gas Ideal y Qué Tiene que Ver con las Carreras?
- Los 5 Postulados de la Teoría Cinético-Molecular (KMT)
- 1. Las partículas de gas están en movimiento constante, aleatorio y rectilíneo.
- 2. El volumen de las partículas de gas es despreciable en comparación con el espacio entre ellas.
- 3. No existen fuerzas de atracción o repulsión entre las partículas de gas.
- 4. Las colisiones son perfectamente elásticas.
- 5. La energía cinética promedio de las moléculas es directamente proporcional a la temperatura absoluta (en Kelvin).
- Distribuciones de Maxwell-Boltzmann: Visualizando la Velocidad Molecular
- Ejemplo Práctico: De los Boxes a la Pista
- Tabla Comparativa: Gas Ideal vs. Gas Real en el Motorsport
- Preguntas Frecuentes (FAQ)
¿Qué es un Gas Ideal y Qué Tiene que Ver con las Carreras?
En el mundo de la ciencia, un "gas ideal" es un gas teórico compuesto por partículas que se mueven al azar y que no interactúan entre sí. Es una simplificación que nos permite establecer leyes y ecuaciones predecibles, como la famosa Ley del Gas Ideal. En la realidad, ningún gas es perfectamente ideal, pero bajo ciertas condiciones, muchos se comportan de manera muy similar. Curiosamente, los gases que más se acercan a este comportamiento ideal son el Hidrógeno (H₂) y el Helio (He), debido a que sus partículas son extremadamente pequeñas y no polares.
Las condiciones en las que un gas real se comporta más como un gas ideal son de baja presión y alta temperatura. ¿Y dónde encontramos estas condiciones en el automovilismo? ¡En todas partes! Desde el aire comprimido dentro de un neumático que se calienta a más de 100°C en pista, hasta la mezcla de aire y combustible que explota dentro de un cilindro del motor a temperaturas altísimas. Comprender los principios del gas ideal nos da una base sólida para optimizar el rendimiento.
Los 5 Postulados de la Teoría Cinético-Molecular (KMT)
La Teoría Cinético-Molecular (conocida como KMT por sus siglas en inglés) se basa en cinco supuestos o postulados principales que explican el comportamiento de los gases a nivel microscópico. Veamos cada uno de ellos y su aplicación directa en el motorsport.
1. Las partículas de gas están en movimiento constante, aleatorio y rectilíneo.
Imagina el interior de un neumático de F1. No está lleno de aire estático. En realidad, está repleto de miles de millones de moléculas de nitrógeno y oxígeno que se mueven a velocidades increíbles en todas direcciones, como si fueran balas de cañón microscópicas. Viajan en línea recta hasta que chocan con otra molécula o, más importante aún, con la pared interna del neumático.
2. El volumen de las partículas de gas es despreciable en comparación con el espacio entre ellas.
Aunque hay miles de millones de moléculas, el espacio vacío entre ellas es inmenso. Esto significa que los gases son altamente compresibles. En un motor, esta propiedad permite que el pistón comprima una gran cantidad de mezcla de aire y combustible en el pequeño espacio de la cámara de combustión, un paso crucial para generar una explosión potente.
3. No existen fuerzas de atracción o repulsión entre las partículas de gas.
Este es uno de los puntos clave de un gas "ideal". Se asume que las moléculas no se atraen ni se repelen entre sí; simplemente se ignoran hasta que colisionan. En la realidad, existen fuerzas débiles (fuerzas de Van der Waals), pero a las altas temperaturas y bajas presiones relativas del automovilismo, este postulado es una aproximación muy útil y precisa para la mayoría de los cálculos.
4. Las colisiones son perfectamente elásticas.
Esto es fundamental para entender la presión. Cuando una molécula de gas choca contra la pared interna del neumático, no pierde energía. Transfiere su momento y rebota con la misma energía con la que llegó. La presión que medimos en un neumático no es más que el resultado de la fuerza acumulada de incontables colisiones de estas moléculas contra cada centímetro cuadrado de la superficie interna del caucho. Cada colisión ejerce una fuerza diminuta, pero la suma de billones de ellas por segundo crea la presión que soporta el peso de todo el coche.
5. La energía cinética promedio de las moléculas es directamente proporcional a la temperatura absoluta (en Kelvin).
Este es el postulado más importante para un ingeniero de carreras. La energía cinética es la energía del movimiento, y su fórmula es KE = 1/2mv², donde 'm' es la masa y 'v' es la velocidad. Lo que este postulado nos dice es simple: si aumentas la temperatura de un gas, sus moléculas se mueven más rápido. Y si se mueven más rápido, chocarán contra las paredes del contenedor (el neumático) con más fuerza y con mayor frecuencia. ¿El resultado? Un aumento de la presión.
Aquí es donde la famosa "ventana de temperatura" de los neumáticos cobra sentido. Un neumático frío tiene una presión más baja. A medida que el coche rueda y el neumático se calienta por la fricción con el asfalto, la temperatura del gas en su interior aumenta, las moléculas se aceleran, y la presión sube. Si la presión sube demasiado, la superficie de contacto del neumático con el asfalto se reduce, disminuyendo el agarre. Si es demasiado baja, el neumático se deforma en exceso, se sobrecalienta y se desgasta prematuramente. El trabajo del ingeniero es predecir este cambio y ajustar la presión inicial en frío para que en la pista, a la temperatura de operación, la presión sea la óptima.
Distribuciones de Maxwell-Boltzmann: Visualizando la Velocidad Molecular
No todas las moléculas en un gas se mueven a la misma velocidad. Algunas son más lentas, otras son increíblemente rápidas, y la mayoría se agrupa en torno a una velocidad promedio. Un gráfico de distribución de Maxwell-Boltzmann nos muestra exactamente esto: cuántas moléculas se mueven a cada velocidad para una temperatura dada.
A menudo, estos gráficos pueden ser confusos. Un gas más frío tendrá un pico más alto y estrecho en el gráfico. Esto no significa que tenga más energía; significa que una gran cantidad de sus moléculas se mueven a una velocidad similar y relativamente lenta. Por otro lado, un gas más caliente tendrá una curva más aplanada y ancha. Esto indica que hay una mayor dispersión de velocidades y, crucialmente, que muchas más moléculas se están moviendo a velocidades muy altas. Esas moléculas de alta velocidad son las que más contribuyen a la presión y a la transferencia de energía.
Pensemos en los neumáticos de nuevo. En la vuelta de formación (neumático frío), la distribución de velocidades de las moléculas de nitrógeno es estrecha. A mitad de carrera (neumático caliente), esa curva se ha aplanado y extendido, indicando un estado de mucha mayor energía y, por lo tanto, mayor presión.
Ejemplo Práctico: De los Boxes a la Pista
Imaginemos que un ingeniero de Haas F1 Team mide la presión de un neumático en el garaje. La temperatura ambiente es de 26°C (299 Kelvin) y la presión es de 1.5 atm. El ingeniero sabe que en la pista, la temperatura del neumático alcanzará los 152°C (425 Kelvin). ¿Cuál será la nueva presión?
Aquí aplicamos la Ley de Gay-Lussac, que se deriva directamente de la KMT y relaciona presión y temperatura a volumen constante (el volumen del neumático es prácticamente fijo).
- Fórmula: P₁ / T₁ = P₂ / T₂
- Datos iniciales (P₁, T₁): 1.5 atm, 299 K
- Datos finales (T₂): 425 K
- Cálculo: (1.5 atm / 299 K) = P₂ / 425 K
- Despejando P₂: P₂ = (1.5 atm * 425 K) / 299 K
- Resultado: P₂ ≈ 2.13 atm
La presión ha aumentado más de un 40% solo por el efecto de la temperatura. Este cálculo simple, basado en la Teoría Cinético-Molecular, es una de las herramientas más básicas y poderosas para un equipo de carreras.
Tabla Comparativa: Gas Ideal vs. Gas Real en el Motorsport
| Característica | Modelo del Gas Ideal | Comportamiento del Gas Real (en el coche) |
|---|---|---|
| Fuerzas Intermoleculares | Inexistentes. | Existen fuerzas débiles, pero a altas temperaturas su efecto es mínimo. La predicción es muy buena. |
| Volumen Molecular | Despreciable, cero. | Las moléculas tienen un volumen real. A presiones extremadamente altas (como en sistemas hidráulicos), este volumen importa. |
| Aplicación | Proporciona ecuaciones simples y predicciones muy precisas para la mayoría de las condiciones en carrera. | Para simulaciones de máxima precisión (CFD, combustión), se usan modelos más complejos (ecuación de Van der Waals), pero los principios de la KMT siguen siendo la base. |
Preguntas Frecuentes (FAQ)
¿Por qué los equipos de F1 usan nitrógeno en lugar de aire normal en los neumáticos?
El aire que respiramos contiene aproximadamente un 21% de oxígeno y también vapor de agua. El agua es el principal problema: al calentarse, se expande de manera mucho menos predecible que un gas seco como el nitrógeno. Usar nitrógeno puro, que es un gas inerte y seco, permite a los ingenieros tener un control mucho más preciso y consistente sobre cómo aumenta la presión del neumático con la temperatura, ya que su comportamiento se acerca más al de un gas ideal.
¿Cómo afecta la altitud (menor presión atmosférica) al rendimiento?
La KMT nos dice que la presión depende del número de colisiones. A mayor altitud, como en el Gran Premio de México, el aire es menos denso. Hay menos moléculas de oxígeno por metro cúbico. Esto tiene dos efectos principales: 1) El motor de combustión tiene menos oxígeno para quemar, lo que reduce la potencia (aunque los turbocompresores ayudan a compensarlo). 2) Hay menos aire para la aerodinámica, lo que significa menos carga aerodinámica (downforce) y menos resistencia al avance (drag). Los equipos tienen que usar alerones más grandes para recuperar el agarre perdido.
¿Es la Teoría Cinético-Molecular una ley exacta?
No, es un modelo teórico. Su propósito es simplificar la complejidad del mundo real para poder hacer predicciones útiles. Describe perfectamente un "gas ideal" que no existe. Sin embargo, para las condiciones de temperatura y presión que se manejan en la mayoría de las aplicaciones del automovilismo, las predicciones que se derivan de esta teoría son extraordinariamente precisas y forman la base de la ingeniería de gases en la competición.
Así que la próxima vez que veas una carrera, recuerda que dentro de esos neumáticos y esos motores, hay un universo invisible de partículas en movimiento, gobernado por las elegantes leyes de la física. La Teoría Cinético-Molecular no es solo una aburrida lección de química; es una de las claves para desbloquear la máxima velocidad.
Si quieres conocer otros artículos parecidos a La Ciencia Oculta de la F1: Teoría Cinético-Molecular puedes visitar la categoría Automovilismo.