20/08/2024
En el vasto universo de la química orgánica, pocas moléculas son tan icónicas y fundamentales como el benceno. Con una fórmula molecular aparentemente simple, C6H6, este compuesto esconde una complejidad estructural y un comportamiento químico que desafiaron a los científicos durante décadas y que, a día de hoy, sigue siendo un pilar para entender una clase entera de compuestos: los hidrocarburos aromáticos. El benceno no es solo una molécula de libro de texto; es un componente crucial en la industria, un producto natural presente en volcanes e incendios forestales, y, a su vez, una sustancia con serias implicaciones para la salud humana. Este artículo se sumerge en el corazón del benceno, desentrañando los secretos de su fórmula, su estructura única y su doble cara como pilar industrial y riesgo tóxico.
- La Fórmula Molecular: C6H6, un Código Engañosamente Simple
- El Enigma Estructural: El Sueño de Kekulé y la Realidad Cuántica
- Más Allá de las Líneas: La Deslocalización de Electrones y la Aromaticidad
- Propiedades Físicas y Químicas del Benceno
- El Benceno en el Mundo Real: Usos y Peligros
- Preguntas Frecuentes (FAQ) sobre el Benceno
La Fórmula Molecular: C6H6, un Código Engañosamente Simple
La puerta de entrada a cualquier compuesto químico es su fórmula molecular, y la del benceno es C6H6. Esto nos dice que cada molécula de benceno está compuesta por exactamente seis átomos de carbono (C) y seis átomos de hidrógeno (H). A primera vista, podría parecer sencillo, pero esta proporción fue una de las primeras pistas de que el benceno no era un hidrocarburo ordinario. Si lo comparamos con un hidrocarburo de cadena abierta con seis carbonos, como el hexano (C6H14), notamos una gran "deficiencia" de hidrógeno. Esta diferencia sugería que la molécula debía contener múltiples enlaces dobles o una estructura cíclica para satisfacer la valencia del carbono, que es cuatro (cada átomo de carbono tiende a formar cuatro enlaces químicos).
El descubrimiento de esta fórmula se remonta a 1834, cuando el químico alemán Eilhard Mitscherlich la determinó, aunque la sustancia ya había sido aislada en 1825 por el célebre científico Michael Faraday. Sin embargo, conocer los ingredientes no era suficiente; el verdadero desafío era entender cómo estos doce átomos se organizaban en el espacio para formar una molécula estable.
El Enigma Estructural: El Sueño de Kekulé y la Realidad Cuántica
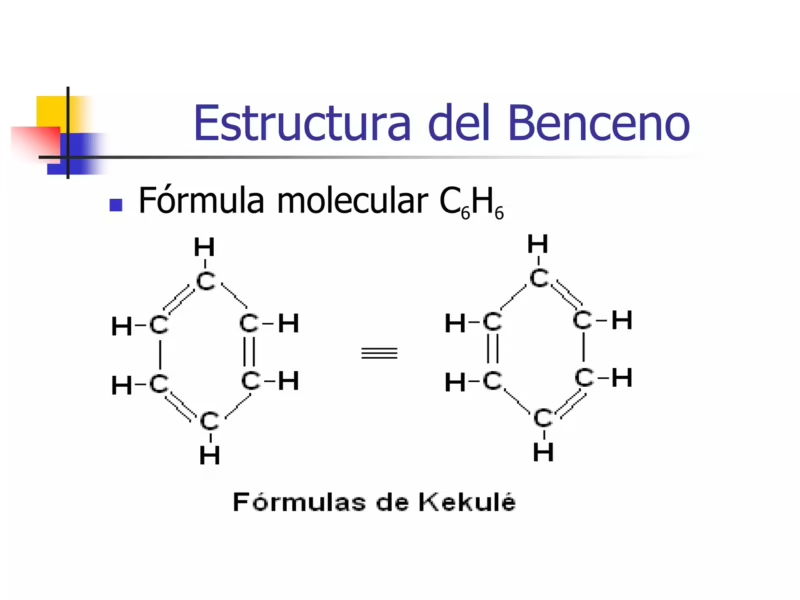
Durante casi 40 años, la estructura del benceno fue uno de los mayores rompecabezas de la química. Muchos intentaron proponer arreglos que encajaran con la fórmula C6H6 y sus propiedades conocidas, pero fue en 1865 cuando Friedrich August Kekulé propuso la idea que cambiaría la química orgánica para siempre. La leyenda cuenta que la idea le vino en un sueño en el que vio una serpiente mordiéndose la cola, una imagen del antiguo símbolo del Ouroboros. Inspirado, propuso que los seis átomos de carbono del benceno estaban dispuestos en un anillo hexagonal plano, con cada carbono unido a un átomo de hidrógeno. Para satisfacer la valencia de cuatro para cada carbono, sugirió que había tres enlaces dobles y tres enlaces simples alternándose alrededor del anillo.
Esta estructura fue revolucionaria y explicaba muchas de las propiedades del benceno. Sin embargo, presentaba un problema: si existieran enlaces dobles y simples fijos, debería haber dos longitudes de enlace diferentes en el anillo (un enlace doble es más corto que uno simple). Además, esto implicaría la existencia de diferentes isómeros para derivados disustituidos que, en la práctica, no se observaban. La química experimental demostraba que todos los enlaces carbono-carbono en el benceno eran idénticos.
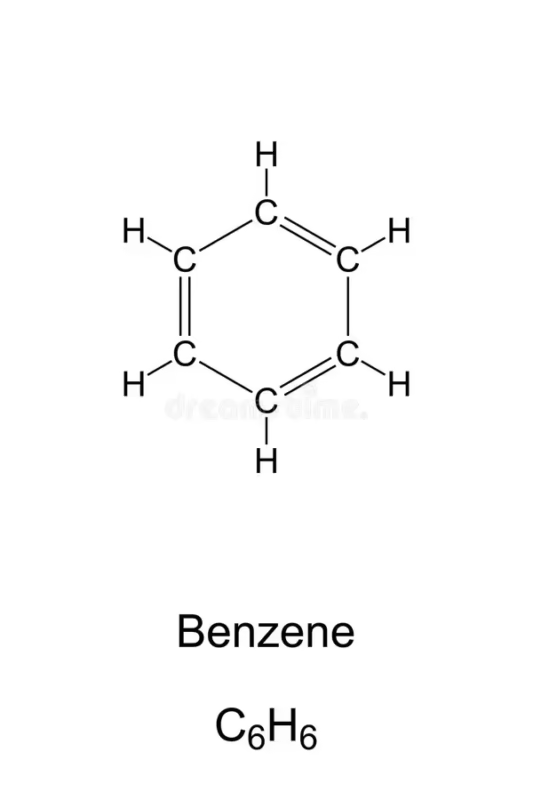
Más Allá de las Líneas: La Deslocalización de Electrones y la Aromaticidad
La solución al dilema de Kekulé llegó con el desarrollo de la química cuántica y el concepto de resonancia. Se entendió que la estructura del benceno no es una de las dos formas con dobles enlaces alternos, sino un híbrido de ambas. Los seis electrones de los enlaces "dobles" (conocidos como electrones π) no están localizados entre pares específicos de átomos de carbono, sino que están deslocalizados, moviéndose libremente por todo el anillo en una nube electrónica por encima y por debajo del plano de la molécula.
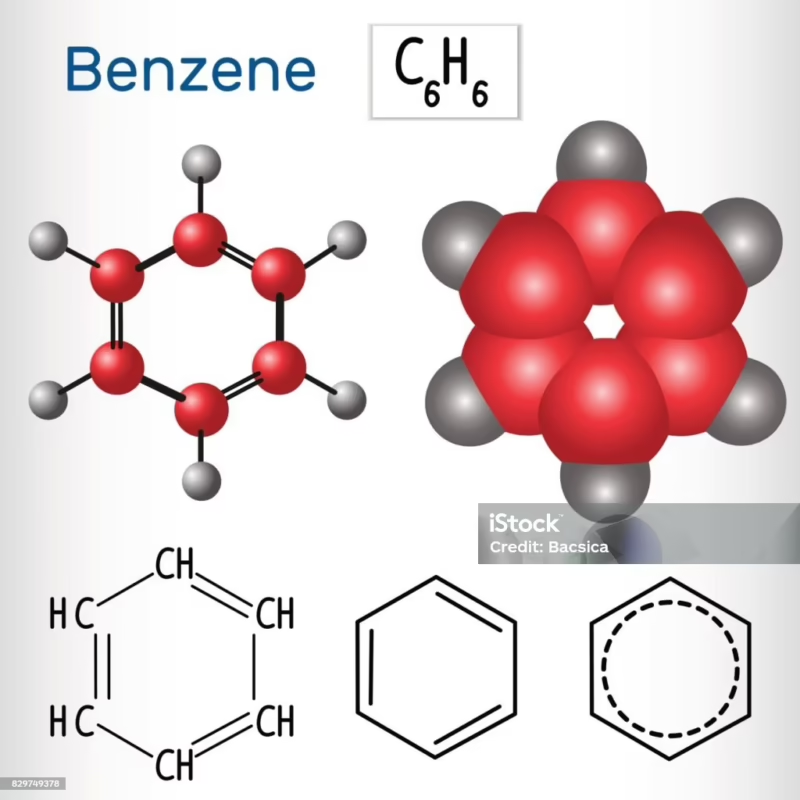
Esta deslocalización de electrones es la clave de la excepcional estabilidad del benceno. Esta propiedad se conoce como aromaticidad, un término que originalmente se refería al olor fragante de estos compuestos pero que ahora describe esta estabilidad electrónica única. Gracias a esta deslocalización, todos los enlaces carbono-carbono en el benceno tienen la misma longitud: 140 picómetros (pm), un valor intermedio entre un enlace simple (147 pm) y uno doble (135 pm). Para representar esta realidad, hoy en día el benceno se dibuja de dos maneras:
- Estructura de Kekulé: Un hexágono con tres dobles enlaces alternos, a menudo con una flecha de doble punta entre las dos formas resonantes para indicar que la estructura real es un híbrido.
- Estructura de Robinson: Un hexágono con un círculo inscrito en su interior. Este círculo es una representación elegante y precisa de la nube de seis electrones π deslocalizados que estabiliza la molécula.
Propiedades Físicas y Químicas del Benceno
La estructura única del benceno dicta sus propiedades. Es un líquido incoloro a temperatura ambiente, altamente inflamable y con un olor característico que se describe como dulce o aromático. Es volátil, lo que significa que se evapora fácilmente. Su naturaleza no polar hace que sea insoluble en agua pero muy soluble en disolventes orgánicos no polares como el éter o el cloroformo.
Tabla de Propiedades del Benceno
| Propiedad | Valor |
|---|---|
| Fórmula Molecular | C6H6 |
| Masa Molar | 78.11 g/mol |
| Apariencia | Líquido incoloro |
| Punto de Ebullición | 80.1 °C |
| Punto de Fusión | 5.5 °C |
| Densidad | 0.8765 g/cm³ |
| Solubilidad en agua | Insoluble |
Químicamente, la aromaticidad del benceno lo hace reaccionar de manera muy diferente a los alquenos (hidrocarburos con dobles enlaces). En lugar de sufrir reacciones de adición que romperían la estabilidad del anillo aromático, el benceno sufre preferentemente reacciones de sustitución electrofílica aromática. En estas reacciones, uno de los átomos de hidrógeno del anillo es reemplazado por otro grupo de átomos, manteniendo intacto el sistema de electrones deslocalizados.
El Benceno en el Mundo Real: Usos y Peligros
El benceno es una de las materias primas más importantes en la industria química. Es un componente del petróleo crudo y la gasolina, y se utiliza como punto de partida para sintetizar una enorme variedad de productos. Algunos de sus usos más importantes incluyen:
- Producción de plásticos como el poliestireno (a partir de estireno).
- Fabricación de resinas y fibras sintéticas como el nailon.
- Síntesis de productos farmacéuticos, detergentes, pesticidas y colorantes.
Sin embargo, esta utilidad industrial contrasta fuertemente con su toxicidad. El benceno es un conocido carcinógeno humano. La exposición a largo plazo, incluso a niveles bajos, está directamente relacionada con un mayor riesgo de desarrollar leucemia y otros cánceres de la sangre. La exposición aguda (a corto plazo y en altas concentraciones) por inhalación puede causar somnolencia, mareos, dolores de cabeza, e incluso pérdida del conocimiento y la muerte. El contacto con la piel puede causar irritación y sequedad. Debido a estos graves riesgos para la salud, su uso está estrictamente regulado en todo el mundo y se ha eliminado de muchos productos de consumo en los que se utilizaba anteriormente, como los disolventes.

Preguntas Frecuentes (FAQ) sobre el Benceno
¿Cuál es la fórmula del benceno?
La fórmula molecular del benceno es C6H6, lo que indica que está compuesto por seis átomos de carbono y seis átomos de hidrógeno.
¿Por qué el benceno es tan estable?
Su excepcional estabilidad se debe a la aromaticidad, un fenómeno causado por la deslocalización de seis electrones π en una nube continua alrededor del anillo hexagonal de carbono. Esto distribuye la energía de manera más eficiente que si los enlaces fueran fijos.
¿Cómo se representa la estructura del benceno?
Se representa comúnmente de dos maneras: como un hexágono con tres dobles enlaces alternos (estructura de Kekulé) o, de forma más precisa, como un hexágono con un círculo en su interior para simbolizar los electrones deslocalizados.
¿Es peligroso el benceno?
Sí, es muy peligroso. Es una sustancia tóxica y un carcinógeno humano confirmado por la Agencia Internacional para la Investigación del Cáncer (IARC). La exposición prolongada puede causar leucemia.
¿Qué significa que el benceno es un hidrocarburo aromático?
Significa que es un compuesto de carbono e hidrógeno que contiene uno o más anillos con electrones π deslocalizados. Esta característica le confiere una gran estabilidad y un comportamiento químico específico, diferente al de otros hidrocarburos.
En conclusión, el benceno es mucho más que su simple fórmula C6H6. Es una molécula que encarna la elegancia y la complejidad de la química, una pieza clave cuyo descubrimiento y comprensión abrieron nuevas fronteras en la ciencia. Su estructura resonante y su aromaticidad son conceptos fundamentales para cualquier estudiante o aficionado a la química. Al mismo tiempo, su historia nos recuerda la importante dualidad de la ciencia: una sustancia que ha impulsado el desarrollo industrial y tecnológico puede ser también una amenaza silenciosa para la salud, subrayando la necesidad de un manejo responsable y un conocimiento profundo de las herramientas que la naturaleza y la ciencia ponen a nuestro alcance.
Si quieres conocer otros artículos parecidos a Benceno: Fórmula, Estructura y Secretos puedes visitar la categoría Automovilismo.
