11/07/2022
En el vasto universo de la química inorgánica, los ácidos oxácidos, también conocidos como oxoácidos, representan una familia de compuestos fundamental. Se trata de compuestos ternarios, lo que significa que están formados por tres elementos distintos: hidrógeno (H), oxígeno (O) y un elemento no metálico (o en algunos casos, un metal de transición en un alto estado de oxidación). Su característica principal, que los distingue de los hidrácidos (como el HCl), es la presencia de al menos un átomo de oxígeno en su estructura. Estos compuestos son vitales en numerosos procesos industriales y biológicos, y comprender su formulación y nomenclatura es un pilar esencial para cualquier estudiante o aficionado a la química.

La formación de estos ácidos es un proceso fascinante que generalmente parte de la reacción entre un óxido no metálico, también llamado anhídrido, y agua. Este artículo se sumerge en las profundidades de los oxácidos, desglosando sus fórmulas, las reglas para escribirlas correctamente y el sistema de nomenclatura tradicional que permite nombrarlos de manera inequívoca.

- ¿Qué es Exactamente un Ácido Oxácido?
- El Origen: Formación a Partir de Óxidos Ácidos
- Formulación de Oxácidos: Reglas Clave
- Nomenclatura Tradicional de los Oxácidos
- Familias de Oxácidos y sus Aniones Correspondientes
- Casos Especiales: Ácidos Meta-, Piro- y Orto-
- Preguntas Frecuentes (FAQ) sobre Ácidos Oxácidos
¿Qué es Exactamente un Ácido Oxácido?
Un ácido oxácido es un compuesto que contiene hidrógeno, oxígeno y al menos otro elemento (generalmente un no metal), con al menos un átomo de hidrógeno enlazado a un átomo de oxígeno. Este enlace H-O es crucial, ya que es el que se rompe en disolución acuosa para liberar un protón (H⁺) y el anión correspondiente, confiriendo al compuesto sus propiedades ácidas. La fórmula general que representa a estos compuestos es HₐXₐOₐ, donde 'X' es el elemento central no metálico.
Históricamente, bajo la teoría original de Lavoisier, se creía que todos los ácidos contenían oxígeno (de ahí el nombre, del griego oxys, 'ácido', y genes, 'creador'). Aunque más tarde se descubrieron ácidos sin oxígeno, como los hidrácidos, el término oxácido se mantuvo para este importante grupo. Su acidez no depende de la fuerza del enlace H-X, sino de factores como la electronegatividad del átomo central 'X' y, de manera muy significativa, del número de átomos de oxígeno unidos a él que no están unidos a un hidrógeno.

El Origen: Formación a Partir de Óxidos Ácidos
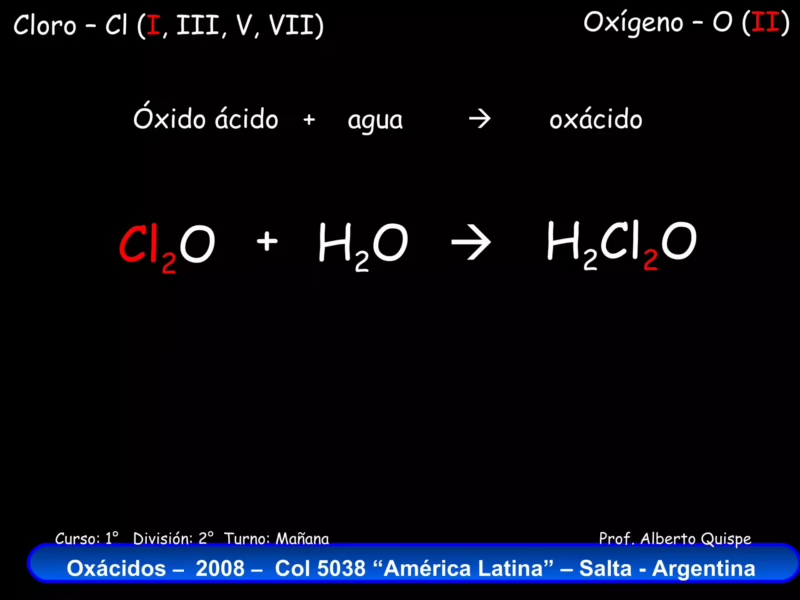
La síntesis más común de un oxácido implica la hidratación de su anhídrido correspondiente. Un anhídrido u óxido ácido es un compuesto formado por un no metal y oxígeno. Al reaccionar con agua (H₂O), se produce el ácido oxácido. El proceso se puede visualizar de la siguiente manera:
Óxido Ácido (Anhídrido) + Agua → Ácido Oxácido
Un ejemplo clásico es la formación del ácido nítrico (HNO₃) a partir del pentóxido de dinitrógeno (N₂O₅):
N₂O₅ + H₂O ⟶ H₂N₂O₆ ⟶ 2 HNO₃
En esta reacción, la molécula de agua se adiciona al óxido. Los átomos de cada elemento se suman y, si es posible, la fórmula resultante se simplifica para obtener la fórmula molecular final del ácido. Este método es la base para deducir la fórmula de la mayoría de los oxácidos.
Formulación de Oxácidos: Reglas Clave
Para escribir correctamente la fórmula de un oxácido, se sigue un orden específico: primero el Hidrógeno (H), luego el no metal (X) y finalmente el Oxígeno (O). La clave para determinar los subíndices (el número de átomos de cada elemento) radica en el número de oxidación del elemento no metálico. Existen dos reglas generales dependiendo de si este número es par o impar.
Caso 1: El No Metal tiene Número de Oxidación Impar
Cuando el elemento central no metálico actúa con un número de oxidación impar (como +1, +3, +5, +7), la fórmula del oxácido resultante tendrá un solo átomo de hidrógeno. La fórmula se construye de la siguiente manera:
H X O(valencia + 1)/2
Veamos un ejemplo con el Cloro (Cl), que puede actuar con valencias +1, +3, +5 y +7:
- Valencia +1: H Cl O(1+1)/2 → HClO (Ácido hipocloroso)
- Valencia +3: H Cl O(3+1)/2 → HClO₂ (Ácido cloroso)
- Valencia +5: H Cl O(5+1)/2 → HClO₃ (Ácido clórico)
- Valencia +7: H Cl O(7+1)/2 → HClO₄ (Ácido perclórico)
Caso 2: El No Metal tiene Número de Oxidación Par
Cuando el elemento central no metálico actúa con un número de oxidación par (como +2, +4, +6), la fórmula del oxácido resultante tendrá dos átomos de hidrógeno. La fórmula se construye así:
H₂ X O(valencia + 2)/2
Tomemos como ejemplo el Azufre (S), que actúa con valencias +4 y +6:
- Valencia +4: H₂ S O(4+2)/2 → H₂SO₃ (Ácido sulfuroso)
- Valencia +6: H₂ S O(6+2)/2 → H₂SO₄ (Ácido sulfúrico)
Nomenclatura Tradicional de los Oxácidos
La nomenclatura tradicional es ampliamente utilizada para nombrar estos compuestos. Utiliza un sistema de prefijos y sufijos que se añaden al nombre del no metal para indicar el estado de oxidación con el que está trabajando. La asignación depende de cuántos estados de oxidación posea el elemento:
| Número de Estados de Oxidación | Estado de Oxidación | Prefijo | Sufijo | Ejemplo (Cloro) |
|---|---|---|---|---|
| 4 Estados | Menor (+1) | Hipo- | -oso | Ácido hipocloroso (HClO) |
| Segundo menor (+3) | - | -oso | Ácido cloroso (HClO₂) | |
| Segundo mayor (+5) | - | -ico | Ácido clórico (HClO₃) | |
| Mayor (+7) | Per- | -ico | Ácido perclórico (HClO₄) | |
| 2 Estados | Menor (+4) | - | -oso | Ácido sulfuroso (H₂SO₃) |
| Mayor (+6) | - | -ico | Ácido sulfúrico (H₂SO₄) |
Familias de Oxácidos y sus Aniones Correspondientes
Cuando un ácido oxácido pierde sus hidrógenos ácidos (protones), forma un ion negativo llamado anión. El nombre del anión se deriva del nombre del ácido, cambiando los sufijos de la siguiente manera: -oso se convierte en -ito, y -ico se convierte en -ato. A continuación, se detallan algunas de las familias más importantes.
Grupo 17: Halógenos (Cloro, Bromo, Yodo)
Estos elementos forman cuatro oxácidos distintos, correspondiendo a sus estados de oxidación +1, +3, +5 y +7.

| Fórmula del Ácido | Nombre del Ácido | Fórmula del Anión | Nombre del Anión |
|---|---|---|---|
| HXO | Ácido hipo...oso | XO⁻ | Hipohalogenito |
| HXO₂ | Ácido ...oso | XO₂⁻ | Halogenito |
| HXO₃ | Ácido ...ico | XO₃⁻ | Halogenato |
| HXO₄ | Ácido per...ico | XO₄⁻ | Perhalogenato |
Grupo 16: Calcógenos (Azufre, Selenio, Telurio)
Forman ácidos con dos hidrógenos debido a sus estados de oxidación pares (+4, +6).
| Fórmula del Ácido | Nombre del Ácido | Fórmula del Anión | Nombre del Anión |
|---|---|---|---|
| H₂XO₂ | Ácido hipo...oso | XO₂²⁻ | Hipo...ito |
| H₂XO₃ | Ácido ...oso | XO₃²⁻ | ...ito |
| H₂XO₄ | Ácido ...ico | XO₄²⁻ | ...ato |
Ejemplo concreto: H₂SO₄ es el Ácido Sulfúrico, y su anión SO₄²⁻ es el ion Sulfato.
Grupo 15: Nitrogenoideos (Nitrógeno, Fósforo, Arsénico)
Estos elementos presentan una química más compleja, dando lugar a los ácidos especiales tipo orto-, que se consideran la forma más hidratada del ácido.
| Fórmula del Ácido | Nombre del Ácido | Fórmula del Anión | Nombre del Anión |
|---|---|---|---|
| H₃XO₃ | Ácido (orto)...oso | XO₃³⁻ | (Orto)...ito |
| H₃XO₄ | Ácido (orto)...ico | XO₄³⁻ | (Orto)...ato |
Ejemplo concreto: H₃PO₄ es el Ácido (orto)fosfórico, componente clave de bebidas gaseosas y fertilizantes. Su anión es el PO₄³⁻, ion Fosfato.
Casos Especiales: Ácidos Meta-, Piro- y Orto-
Para algunos elementos como el Fósforo, Arsénico y Boro, el grado de hidratación del óxido ácido es importante y da lugar a diferentes ácidos. Los prefijos meta-, piro- y orto- indican este grado de hidratación:
- Meta-: Es la forma menos hidratada. Se obtiene de la reacción de una molécula de anhídrido con una de agua.
- Piro-: Es una forma intermedia, obtenida por la condensación de dos moléculas del ácido orto con la pérdida de una molécula de agua (2 Ácido Orto → 1 Ácido Piro + H₂O). Su fórmula general es H₄X₂Oₙ.
- Orto-: Es la forma más hidratada y la que se considera por defecto si no se especifica prefijo. Se obtiene de la reacción de una molécula de anhídrido con tres de agua (para el grupo 15).
Por ejemplo, para el Fósforo (V):
- Ácido metafosfórico: P₂O₅ + H₂O → H₂P₂O₆ → 2 HPO₃
- Ácido pirofosfórico: P₂O₅ + 2H₂O → H₄P₂O₇
- Ácido ortofosfórico: P₂O₅ + 3H₂O → H₆P₂O₈ → 2 H₃PO₄
Preguntas Frecuentes (FAQ) sobre Ácidos Oxácidos
- ¿Cuál es la principal diferencia entre un oxácido y un hidrácido?
- La principal diferencia es su composición. Los oxácidos son compuestos ternarios que contienen hidrógeno, oxígeno y un no metal. Los hidrácidos son compuestos binarios que contienen hidrógeno y un no metal, pero no contienen oxígeno (ej. HCl, H₂S).
- ¿Cómo sé si debo usar la regla del número de oxidación par o impar?
- Debes conocer los posibles números de oxidación del no metal central. Si el número de oxidación que está utilizando en el compuesto es un número impar (1, 3, 5, 7), el ácido tendrá un hidrógeno (HXOₙ). Si es par (2, 4, 6), tendrá dos hidrógenos (H₂XOₙ).
- ¿Qué indican los sufijos -oso e -ico?
- En la nomenclatura tradicional, estos sufijos indican el estado de oxidación relativo del no metal. '-oso' se usa para el estado de oxidación menor (entre dos opciones), mientras que '-ico' se usa para el mayor. Si hay más de dos, se usan además los prefijos hipo- y per-.
- ¿Todos los ácidos contienen oxígeno?
- No. Aunque la teoría inicial de Lavoisier así lo proponía, posteriormente se descubrieron los hidrácidos, que son ácidos y no contienen oxígeno. Por tanto, la presencia de oxígeno no es un requisito para que una sustancia sea un ácido.
Si quieres conocer otros artículos parecidos a Ácidos Oxácidos: Guía Completa de Formulación puedes visitar la categoría Automovilismo.
