25/05/2025
Frecuentemente, en el vasto mundo de la química, nos encontramos con compuestos cuyos nombres pueden generar confusión. Una de estas preguntas comunes es sobre la 'fórmula del acetato de mercurio 1'. Si bien esta denominación puede ser una referencia al estado de oxidación del mercurio, el compuesto más común y ampliamente utilizado en laboratorios es el acetato de mercurio (II), también conocido como acetato mercúrico. Este compuesto es una pieza clave en numerosas reacciones de síntesis orgánica, funcionando como un reactivo versátil para la creación de moléculas más complejas. Se presenta como un polvo cristalino de color blanco, similar a la arena fina, aunque con el tiempo puede adquirir una tonalidad amarillenta debido a su descomposición. A lo largo de este artículo, desglosaremos en detalle su estructura, métodos de producción, sus aplicaciones más importantes y las consideraciones de seguridad que se deben tener al manipularlo.

¿Qué es Exactamente el Acetato de Mercurio (II)?
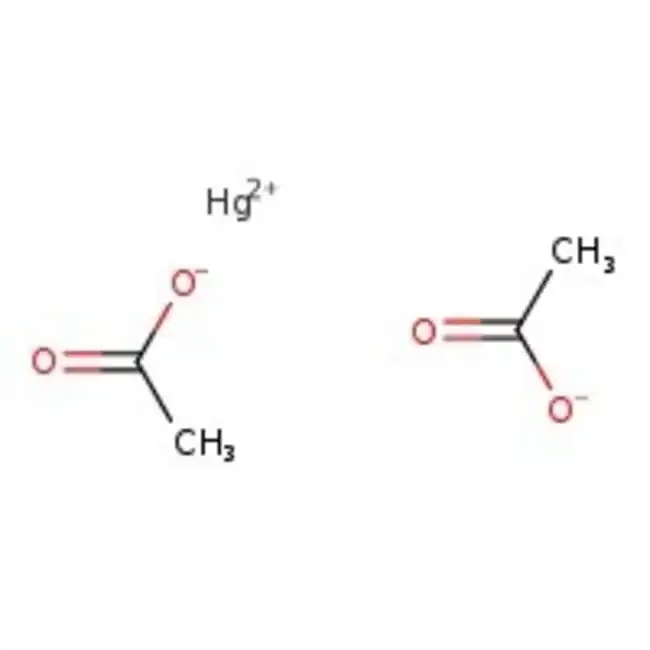
El acetato de mercurio (II) es un compuesto químico, específicamente una sal de mercurio del ácido acético. Su fórmula química es Hg(C₂H₃O₂)₂, aunque comúnmente se representa de forma más explícita como Hg(CH₃COO)₂ o se abrevia en la literatura científica como Hg(OAc)₂. Esta fórmula nos indica que cada molécula está formada por un ion de mercurio con un estado de oxidación de +2 (Hg²⁺), unido a dos iones acetato (CH₃COO⁻).
Desde un punto de vista estructural, en su estado sólido cristalino, el compuesto consiste en moléculas aisladas de Hg(OAc)₂. En estas moléculas, las distancias entre el átomo de mercurio y los átomos de oxígeno son de aproximadamente 2.07 Å (angstroms). Además de estos enlaces primarios, existen interacciones intermoleculares más débiles entre el mercurio y los átomos de oxígeno de moléculas vecinas, lo que resulta en una geometría de coordinación ligeramente distorsionada, similar a una pirámide de base cuadrada. Esta estructura es fundamental para entender su reactividad. Es un sólido soluble en agua, lo que facilita su uso en soluciones para diversas reacciones químicas.
Síntesis y Producción: ¿Cómo se Crea?
La producción del acetato de mercurio (II) en un entorno de laboratorio es un proceso relativamente directo, basado en una reacción ácido-base clásica. El método más común implica la reacción del óxido mercúrico (II) con ácido acético. La ecuación química que describe este proceso es la siguiente:
HgO + 2 CH₃COOH → Hg(CH₃COO)₂ + H₂O
En esta reacción, el óxido de mercurio (II) (HgO), un sólido de color rojo o amarillo, reacciona con dos moléculas de ácido acético (CH₃COOH), el componente principal del vinagre. El resultado de esta neutralización es la formación de acetato de mercurio (II) y agua (H₂O). El producto se puede aislar posteriormente mediante la evaporación del agua y el exceso de ácido acético para obtener el sólido cristalino blanco.
Aplicaciones Clave en la Química Orgánica
El verdadero valor del acetato de mercurio (II) reside en su capacidad para actuar como un reactivo químico en la síntesis orgánica. Su principal función es generar compuestos organomercuriales a partir de precursores orgánicos insaturados. A continuación, se detallan sus aplicaciones más significativas.
Reacciones de Oximercuración-Desmercuración
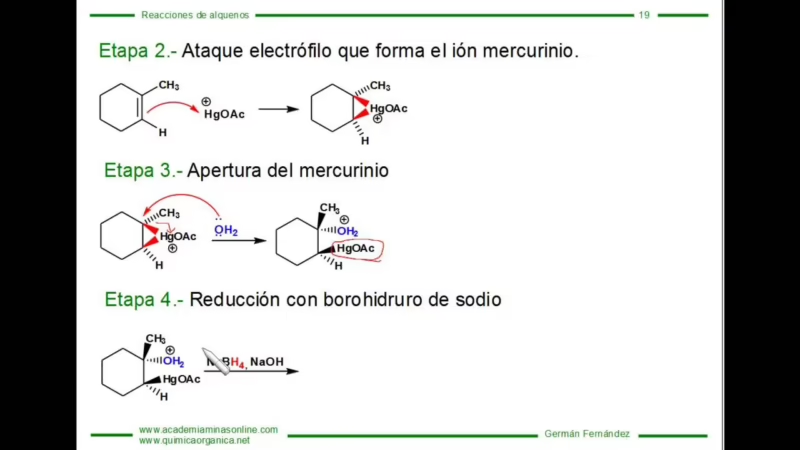
Esta es, sin duda, una de las aplicaciones más famosas del Hg(OAc)₂. La oximercuración es una reacción que permite la adición de un grupo hidroxilo (-OH) o un grupo alcóxido (-OR) a un alqueno (un compuesto con un doble enlace carbono-carbono). El centro de mercurio (Hg²⁺) se une al doble enlace del alqueno, activándolo para el ataque de una molécula de agua o un alcohol. Por ejemplo, al tratar un alqueno con acetato de mercurio en una solución acuosa, se forma un intermediario organomercurial, que luego puede ser tratado con borohidruro de sodio (NaBH₄) para reemplazar el mercurio por un átomo de hidrógeno, resultando en un alcohol. Esta secuencia de dos pasos es altamente eficiente y sigue la regla de Markovnikov, lo que la hace muy predecible y útil en síntesis.
Mercuración de Compuestos Aromáticos (Arenos)
Los compuestos aromáticos ricos en electrones, como el fenol, pueden someterse a un proceso llamado "mercuración" cuando se tratan con acetato de mercurio (II). En esta reacción, un grupo acetoximercurio (-HgOAc) se une directamente a uno de los carbonos del anillo aromático, desplazando a un átomo de hidrógeno. Un ejemplo clásico es la reacción con fenol:
C₆H₅OH + Hg(OAc)₂ → C₆H₄(OH)-2-HgOAc + CH₃COOH
El compuesto organomercurial resultante puede ser utilizado en reacciones posteriores. Por ejemplo, el grupo acetato unido al mercurio puede ser fácilmente reemplazado por un halógeno como el cloro, lo que abre la puerta a otras transformaciones químicas.
Desprotección de Grupos Tiol
En la síntesis orgánica compleja, a menudo es necesario proteger ciertos grupos funcionales para que no reaccionen mientras se modifica otra parte de la molécula. Los grupos tiol (-SH) son uno de ellos. El mercurio (II) tiene una afinidad extremadamente alta por el azufre. Esta propiedad se explota utilizando Hg(OAc)₂ como reactivo para eliminar grupos protectores a base de azufre, liberando el grupo tiol para que pueda participar en reacciones posteriores. Es una herramienta estratégica para los químicos orgánicos.
Conversión de Ésteres de Tiocarbonato
De manera similar a su afinidad por los tioles, el acetato de mercurio (II) se utiliza para convertir ésteres de tiocarbonato en ditiocarbonatos. La reacción aprovecha la formación de sulfuro de mercurio (HgS), un compuesto muy estable, para impulsar la transformación química deseada.
Tabla Comparativa: Propiedades Fundamentales
| Propiedad | Descripción |
|---|---|
| Nombre Químico | Acetato de Mercurio (II) o Acetato Mercúrico |
| Fórmula Molecular | Hg(CH₃COO)₂ |
| Abreviatura Común | Hg(OAc)₂ |
| Masa Molar | 318.68 g/mol |
| Apariencia | Sólido cristalino blanco, puede volverse amarillento |
| Solubilidad | Soluble en agua y ácido acético |
| Uso Principal | Reactivo en síntesis orgánica (oximercuración, etc.) |
Consideraciones de Seguridad y Toxicidad
Es imposible hablar de compuestos de mercurio sin abordar su alta toxicidad. El acetato de mercurio (II) no es una excepción. Es un compuesto extremadamente tóxico por ingestión, inhalación y contacto con la piel. La exposición puede causar daños severos en los riñones, el sistema nervioso y el tracto gastrointestinal. Por esta razón, su manipulación debe realizarse exclusivamente en entornos de laboratorio controlados, utilizando equipo de protección personal adecuado, que incluye guantes resistentes a productos químicos, gafas de seguridad y, fundamentalmente, una campana de extracción de gases para evitar la inhalación de polvo o vapores. Además, los residuos que contienen mercurio deben ser gestionados como residuos peligrosos siguiendo estrictas normativas ambientales para evitar la contaminación del suelo y el agua.

Preguntas Frecuentes (FAQ)
¿Existe el acetato de mercurio (I)?
Sí, existe. El ion mercurio (I) es un ion diatómico, Hg₂²⁺. Por lo tanto, la fórmula del acetato de mercurio (I) es Hg₂(CH₃COO)₂. Es un compuesto diferente, menos común en síntesis orgánica que su contraparte de mercurio (II).
¿Para qué se usa principalmente el acetato de mercurio (II)?
Su uso principal es como reactivo en la síntesis orgánica, especialmente para reacciones de oximercuración de alquenos, que son un método fiable para producir alcoholes. También se utiliza en la mercuración de compuestos aromáticos y para manipular grupos funcionales que contienen azufre.
¿Es peligroso manipular el acetato de mercurio (II)?
Sí, es extremadamente peligroso. Es un compuesto altamente tóxico y requiere precauciones de seguridad rigurosas. La exposición puede causar graves problemas de salud y daños permanentes. Solo debe ser manejado por personal capacitado en un laboratorio equipado.
¿Por qué una muestra de acetato de mercurio puede volverse amarilla?
La coloración amarillenta que pueden desarrollar algunas muestras con el tiempo es un signo de descomposición del compuesto. Esto puede ser acelerado por la exposición a la luz o al calor.
Si quieres conocer otros artículos parecidos a Acetato de Mercurio (II): Guía Completa del Reactivo puedes visitar la categoría Automovilismo.