19/09/2024
En el vasto universo de la química orgánica, los hidrocarburos forman la columna vertebral sobre la que se construye una inmensa variedad de compuestos. Dentro de este grupo, dos familias fundamentales destacan por su simplicidad estructural y su importancia: los alcanos y los alquenos. Mientras que los alcanos son conocidos por su estabilidad y simplicidad, los alquenos introducen una mayor reactividad gracias a sus dobles enlaces. Este artículo se sumerge en el mundo de estos compuestos, proporcionando una lista exhaustiva de los primeros 100 alcanos, y explorando en detalle la naturaleza, nomenclatura y propiedades de los alquenos, para ofrecer una visión completa y comparativa que resuelva todas tus dudas.

¿Qué son los Alcanos? Los Hidrocarburos Saturados
Los alcanos son la clase más simple de hidrocarburos, caracterizados por tener únicamente enlaces simples carbono-carbono (C-C) y carbono-hidrógeno (C-H). Debido a que cada átomo de carbono está unido a otros cuatro átomos (ya sea carbono o hidrógeno), se dice que están "saturados" de hidrógenos. Su fórmula general es CnH2n+2, donde 'n' representa el número de átomos de carbono.
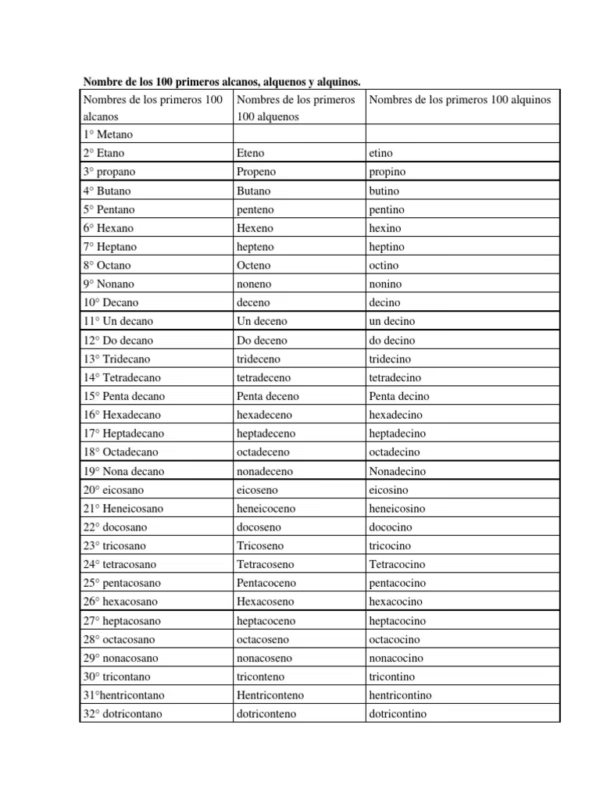
La nomenclatura de los alcanos es la base para nombrar a la mayoría de los compuestos orgánicos. Se utiliza un prefijo que indica el número de átomos de carbono en la cadena principal y se le añade el sufijo "-ano". Son compuestos generalmente no polares, lo que los hace insolubles en agua, y son considerablemente menos reactivos en comparación con otros grupos funcionales, siendo sus reacciones más comunes la combustión y la halogenación por radicales libres.
Lista Completa: Los Primeros 100 Alcanos Lineales
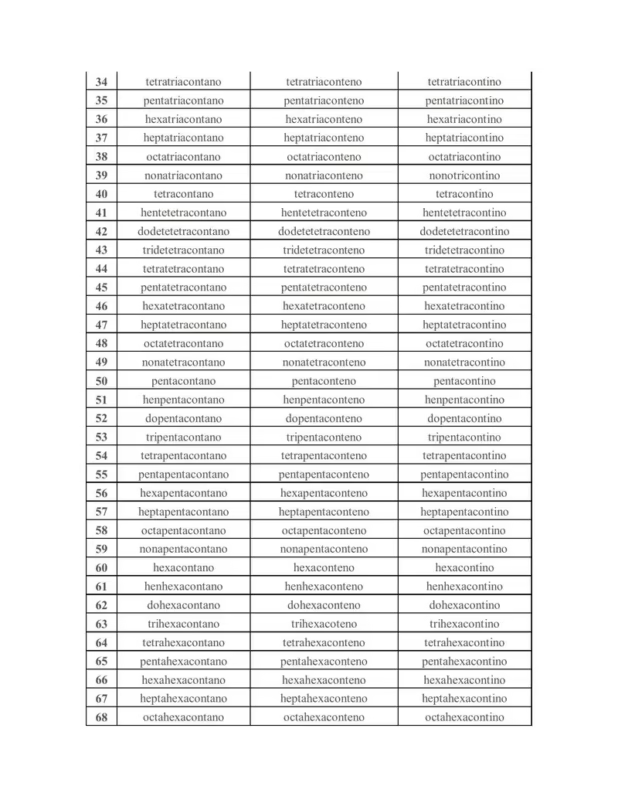
A continuación, se presenta una tabla detallada con los nombres y las fórmulas moleculares de los primeros 100 alcanos de cadena lineal, también conocidos como n-alcanos.

| Número de Carbonos (n) | Nombre del Alcano | Fórmula Molecular |
|---|---|---|
| 1 | Metano | CH₄ |
| 2 | Etano | C₂H₆ |
| 3 | Propano | C₃H₈ |
| 4 | Butano | C₄H₁₀ |
| 5 | Pentano | C₅H₁₂ |
| 6 | Hexano | C₆H₁₄ |
| 7 | Heptano | C₇H₁₆ |
| 8 | Octano | C₈H₁₈ |
| 9 | Nonano | C₉H₂₀ |
| 10 | Decano | C₁₀H₂₂ |
| 11 | Undecano | C₁₁H₂₄ |
| 12 | Dodecano | C₁₂H₂₆ |
| 13 | Tridecano | C₁₃H₂₈ |
| 14 | Tetradecano | C₁₄H₃₀ |
| 15 | Pentadecano | C₁₅H₃₂ |
| 16 | Hexadecano | C₁₆H₃₄ |
| 17 | Heptadecano | C₁₇H₃₆ |
| 18 | Octadecano | C₁₈H₃₈ |
| 19 | Nonadecano | C₁₉H₄₀ |
| 20 | Eicosano | C₂₀H₄₂ |
| 21 | Heneicosano | C₂₁H₄₄ |
| 22 | Docosano | C₂₂H₄₆ |
| 23 | Tricosano | C₂₃H₄₈ |
| 24 | Tetracosano | C₂₄H₅₀ |
| 25 | Pentacosano | C₂₅H₅₂ |
| 26 | Hexacosano | C₂₆H₅₄ |
| 27 | Heptacosano | C₂₇H₅₆ |
| 28 | Octacosano | C₂₈H₅₈ |
| 29 | Nonacosano | C₂₉H₆₀ |
| 30 | Triacontano | C₃₀H₆₂ |
| 31 | Hentriacontano | C₃₁H₆₄ |
| 32 | Dotriacontano | C₃₂H₆₆ |
| 33 | Tritriacontano | C₃₃H₆₈ |
| 34 | Tetratriacontano | C₃₄H₇₀ |
| 35 | Pentatriacontano | C₃₅H₇₂ |
| 36 | Hexatriacontano | C₃₆H₇₄ |
| 37 | Heptatriacontano | C₃₇H₇₆ |
| 38 | Octatriacontano | C₃₈H₇₈ |
| 39 | Nonatriacontano | C₃₉H₈₀ |
| 40 | Tetracontano | C₄₀H₈₂ |
| 41 | Hentetracontano | C₄₁H₈₄ |
| 42 | Dotetracontano | C₄₂H₈₆ |
| 43 | Tritetracontano | C₄₃H₈₈ |
| 44 | Tetratetracontano | C₄₄H₉₀ |
| 45 | Pentatetracontano | C₄₅H₉₂ |
| 46 | Hexatetracontano | C₄₆H₉₄ |
| 47 | Heptatetracontano | C₄₇H₉₆ |
| 48 | Octatetracontano | C₄₈H₉₈ |
| 49 | Nonatetracontano | C₄₉H₁₀₀ |
| 50 | Pentacontano | C₅₀H₁₀₂ |
| 51 | Henpentacontano | C₅₁H₁₀₄ |
| 52 | Dopentacontano | C₅₂H₁₀₆ |
| 53 | Tripentacontano | C₅₃H₁₀₈ |
| 54 | Tetrapentacontano | C₅₄H₁₁₀ |
| 55 | Pentapentacontano | C₅₅H₁₁₂ |
| 56 | Hexapentacontano | C₅₆H₁₁₄ |
| 57 | Heptapentacontano | C₅₇H₁₁₆ |
| 58 | Octapentacontano | C₅₈H₁₁₈ |
| 59 | Nonapentacontano | C₅₉H₁₂₀ |
| 60 | Hexacontano | C₆₀H₁₂₂ |
| 61 | Henhexacontano | C₆₁H₁₂₄ |
| 62 | Dohexacontano | C₆₂H₁₂₆ |
| 63 | Trihexacontano | C₆₃H₁₂₈ |
| 64 | Tetrahexacontano | C₆₄H₁₃₀ |
| 65 | Pentahexacontano | C₆₅H₁₃₂ |
| 66 | Hexahexacontano | C₆₆H₁₃₄ |
| 67 | Heptahexacontano | C₆₇H₁₃₆ |
| 68 | Octahexacontano | C₆₈H₁₃₈ |
| 69 | Nonahexacontano | C₆₉H₁₄₀ |
| 70 | Heptacontano | C₇₀H₁₄₂ |
| 71 | Henheptacontano | C₇₁H₁₄₄ |
| 72 | Doheptacontano | C₇₂H₁₄₆ |
| 73 | Triheptacontano | C₇₃H₁₄₈ |
| 74 | Tetraheptacontano | C₇₄H₁₅₀ |
| 75 | Pentaheptacontano | C₇₅H₁₅₂ |
| 76 | Hexaheptacontano | C₇₆H₁₅₄ |
| 77 | Heptaheptacontano | C₇₇H₁₅₆ |
| 78 | Octaheptacontano | C₇₈H₁₅₈ |
| 79 | Nonaheptacontano | C₇₉H₁₆₀ |
| 80 | Octacontano | C₈₀H₁₆₂ |
| 81 | Henoctacontano | C₈₁H₁₆₄ |
| 82 | Dooctacontano | C₈₂H₁₆₆ |
| 83 | Trioctacontano | C₈₃H₁₆₈ |
| 84 | Tetraoctacontano | C₈₄H₁₇₀ |
| 85 | Pentaoctacontano | C₈₅H₁₇₂ |
| 86 | Hexaoctacontano | C₈₆H₁₇₄ |
| 87 | Heptaoctacontano | C₈₇H₁₇₆ |
| 88 | Octaoctacontano | C₈₈H₁₇₈ |
| 89 | Nonaoctacontano | C₈₉H₁₈₀ |
| 90 | Nonacontano | C₉₀H₁₈₂ |
| 91 | Hennonacontano | C₉₁H₁₈₄ |
| 92 | Dononacontano | C₉₂H₁₈₆ |
| 93 | Trinonacontano | C₉₃H₁₈₈ |
| 94 | Tetranonacontano | C₉₄H₁₉₀ |
| 95 | Pentanonacontano | C₉₅H₁₉₂ |
| 96 | Hexanonacontano | C₉₆H₁₉₄ |
| 97 | Heptanonacontano | C₉₇H₁₉₆ |
| 98 | Octanonacontano | C₉₈H₁₉₈ |
| 99 | Nonanonacontano | C₉₉H₂₀₀ |
| 100 | Hectano | C₁₀₀H₂₀₂ |
Explorando los Hidrocarburos Insaturados: Los Alquenos
Los alquenos, también conocidos como olefinas, son hidrocarburos que contienen al menos un enlace doble carbono-carbono (C=C). Este doble enlace los convierte en hidrocarburos "insaturados", ya que tienen menos átomos de hidrógeno que el alcano correspondiente con el mismo número de carbonos. La fórmula general para un alqueno acíclico con un solo doble enlace es CnH2n.
La presencia del doble enlace, compuesto por un enlace sigma (σ) fuerte y un enlace pi (π) más débil y expuesto, es la causa de la mayor reactividad química de los alquenos. Este enlace π puede romperse con relativa facilidad para permitir reacciones de adición, como la hidrogenación (adición de H₂), la halogenación (adición de halógenos como Cl₂ o Br₂) y la hidrohalogenación (adición de HBr o HCl).
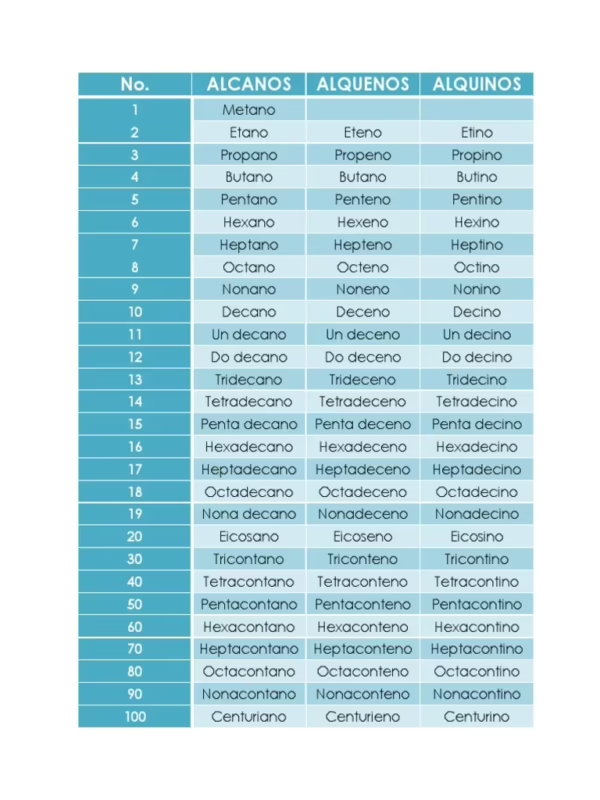
Nomenclatura IUPAC de los Alquenos
Nombrar a los alquenos sigue un conjunto de reglas sistemáticas establecidas por la IUPAC para garantizar la claridad y la coherencia:
- Cadena Principal: Se identifica la cadena de carbono más larga que contenga el doble enlace. El nombre base se deriva del alcano correspondiente, pero el sufijo "-ano" se cambia por "-eno".
- Numeración: La cadena se numera desde el extremo más cercano al doble enlace, de modo que los carbonos del doble enlace reciban los localizadores más bajos posibles.
- Localizador del Enlace: La posición del doble enlace se indica con un número (el del primer carbono del enlace) justo antes del sufijo "-eno" (nomenclatura moderna) o antes del nombre base (nomenclatura más antigua).
- Sustituyentes: Los grupos o sustituyentes se nombran y numeran como en los alcanos, listándose en orden alfabético al principio del nombre.
- Múltiples Dobles Enlaces: Si hay más de un doble enlace, se usan los sufijos "-dieno", "-trieno", etc., y se indican las posiciones de cada uno.
A continuación, una tabla que muestra la evolución de la nomenclatura recomendada por la IUPAC:
| Fórmula | Recomendaciones IUPAC-1979 | Recomendaciones IUPAC-1993 (Actual) |
|---|---|---|
| CH₃-CH₂-CH=CH₂ | 1-buteno | but-1-eno |
| CH₃-CH=CH-CH₃ | 2-buteno | but-2-eno |
| CH₂=CH-CH=CH₂ | 1,3-butadieno | buta-1,3-dieno |
Propiedades Físicas y Químicas Clave
Las propiedades de los alquenos están directamente influenciadas por la presencia del doble enlace.
- Estado Físico: Al igual que los alcanos, los alquenos más pequeños (eteno, propeno, buteno) son gases a temperatura ambiente. A medida que aumenta la masa molecular, se vuelven líquidos y, finalmente, sólidos cerosos.
- Polaridad: El doble enlace introduce una ligera polaridad. En isómeros cis, donde los grupos sustituyentes están del mismo lado del doble enlace, los momentos dipolares de los enlaces se suman, creando una molécula polar. En los isómeros trans, los momentos dipolares a menudo se cancelan, resultando en una molécula no polar o menos polar.
- Acidez: Los hidrógenos unidos a los carbonos de un doble enlace (hidrógenos vinílicos) son ligeramente más ácidos que los de un alcano. Esto se debe a que el carbono con hibridación sp² tiene un mayor carácter "s" que un carbono sp³, lo que estabiliza mejor la carga negativa que queda tras la pérdida de un protón. A pesar de esto, su acidez sigue siendo muy baja.
Alcano vs. Alqueno: Una Comparación Directa
Para resumir las diferencias fundamentales, la siguiente tabla compara las características más importantes de ambas familias de hidrocarburos.

| Característica | Alcanos | Alquenos |
|---|---|---|
| Tipo de Enlace C-C | Enlace simple (σ) | Al menos un enlace doble (σ + π) |
| Fórmula General | CnH2n+2 | CnH2n (con un doble enlace) |
| Saturación | Saturados | Insaturados |
| Hibridación del Carbono | sp³ | sp² (en el doble enlace) |
| Geometría (alrededor del C) | Tetraédrica (109.5°) | Trigonal plana (120°) |
| Reactividad | Baja (reacciones de sustitución) | Alta (reacciones de adición) |
| Isomería Geométrica | No presentan | Sí, isomería cis-trans |
Preguntas Frecuentes (FAQ)
¿Cuál es el alcano más simple?
El alcano más simple es el metano, con la fórmula CH₄. Consiste en un solo átomo de carbono unido a cuatro átomos de hidrógeno.
¿Por qué los alquenos son más reactivos que los alcanos?
La mayor reactividad de los alquenos se debe al enlace pi (π) de su doble enlace. Este enlace es más débil y sus electrones están más expuestos que los del enlace sigma (σ). Por lo tanto, el enlace π puede romperse fácilmente para formar nuevos enlaces en reacciones de adición, algo que no es posible en los alcanos sin romper un fuerte enlace C-C o C-H.
¿Qué es la isomería cis-trans en los alquenos?
La isomería cis-trans (o isomería geométrica) ocurre en los alquenos porque la rotación alrededor del doble enlace carbono-carbono está restringida. Si cada carbono del doble enlace está unido a dos grupos diferentes, pueden existir dos configuraciones: cis, cuando los grupos de mayor prioridad están del mismo lado del doble enlace, y trans, cuando están en lados opuestos.
¿El primer alqueno es el "meteno"?
No. El alqueno más simple es el eteno (C₂H₄), comúnmente llamado etileno. Se necesita un mínimo de dos átomos de carbono para formar un doble enlace, por lo que no puede existir un "meteno" con un solo carbono.
Si quieres conocer otros artículos parecidos a Alcanos del 1 al 100: Guía Definitiva y Alquenos puedes visitar la categoría Automovilismo.

