30/08/2022
Los alquenos representan una de las familias más fascinantes y fundamentales de la química orgánica. Son hidrocarburos, compuestos formados únicamente por carbono e hidrógeno, pero con una característica distintiva que los diferencia de sus parientes, los alcanos: la presencia de al menos un doble enlace carbono-carbono (C=C) en su estructura. Este simple rasgo los clasifica como hidrocarburos insaturados y es la fuente de su notable reactividad y de sus propiedades únicas, convirtiéndolos en piezas clave para la síntesis de una infinidad de compuestos químicos, desde plásticos hasta productos farmacéuticos.

La Estructura Única de los Alquenos: Hibridación sp²
Para comprender a los alquenos, es crucial analizar la geometría de sus átomos. A diferencia de los alcanos, donde los átomos de carbono presentan una hibridación sp³, los carbonos involucrados en el doble enlace de un alqueno tienen una hibridación sp². Esta configuración electrónica dicta una geometría molecular específica. Cada átomo de carbono forma tres enlaces sigma (σ) que se sitúan en un mismo plano, apuntando hacia los vértices de un triángulo equilátero imaginario. Los ángulos entre estos enlaces son de aproximadamente 120°.
Pero, ¿qué sucede con el doble enlace? Este se compone de dos partes: uno de los enlaces sigma (σ) ya mencionados, formado por la superposición frontal de dos orbitales híbridos sp², y un enlace pi (π), que se origina por la superposición lateral de los orbitales p puros (no hibridados) que quedan en cada átomo de carbono. Estos orbitales p son perpendiculares al plano de los enlaces sigma. La nube de electrones del enlace pi se encuentra por encima y por debajo del plano de la molécula, lo que hace que estos electrones estén menos retenidos por los núcleos y, por tanto, sean más accesibles para reaccionar. Esta es la clave de la alta reactividad de los alquenos.
El ejemplo más sencillo es el eteno (C₂H₄), el primer miembro de la serie. En esta molécula, los dos átomos de carbono y los cuatro de hidrógeno yacen en el mismo plano, confirmando su estructura plana trigonal. La rotación alrededor del eje del doble enlace C=C está restringida, a diferencia de lo que ocurre con los enlaces simples C-C, lo que da lugar al fenómeno de la isomería geométrica (cis-trans) en alquenos más complejos.
La Serie Homóloga y Nomenclatura de los Alquenos
Al igual que los alcanos, los alquenos forman una serie homóloga, un conjunto de compuestos que comparten la misma fórmula general y propiedades químicas similares, donde cada miembro difiere del siguiente por un grupo metileno (-CH₂-). La fórmula general para los alquenos acíclicos con un solo doble enlace es CₙH₂ₙ, donde 'n' es el número de átomos de carbono.
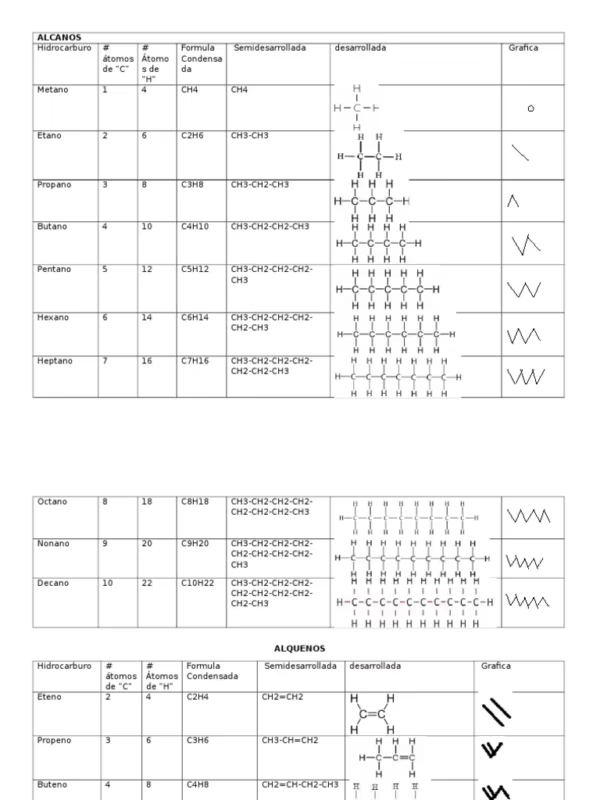
La nomenclatura se deriva directamente de los alcanos correspondientes, cambiando el sufijo '-ano' por '-eno'. Por ejemplo, el alcano de dos carbonos es el etano, mientras que el alqueno es el eteno. A continuación, se muestra una tabla comparativa de los primeros miembros de la serie:
| N° de Carbonos (n) | Nombre del Alcano | Fórmula del Alcano (CₙH₂ₙ₊₂) | Nombre del Alqueno | Fórmula del Alqueno (CₙH₂ₙ) |
|---|---|---|---|---|
| 2 | Etano | C₂H₆ | Eteno | C₂H₄ |
| 3 | Propano | C₃H₈ | Propeno | C₃H₆ |
| 4 | Butano | C₄H₁₀ | Buteno | C₄H₈ |
| 5 | Pentano | C₅H₁₂ | Penteno | C₅H₁₀ |
| 6 | Hexano | C₆H₁₄ | Hexeno | C₆H₁₂ |
Isomería Posicional
A partir del buteno (n=4), surge un nuevo nivel de complejidad: la isomería posicional. Los isómeros son compuestos que tienen la misma fórmula molecular pero diferentes estructuras. En los alquenos, la posición del doble enlace puede variar, dando lugar a diferentes isómeros. Por ejemplo, para la fórmula C₄H₈, el doble enlace puede estar entre el primer y segundo carbono (but-1-eno) o entre el segundo y tercer carbono (but-2-eno). Estos dos compuestos, aunque comparten la misma fórmula, tienen propiedades físicas y químicas ligeramente diferentes.
Propiedades Físicas y Químicas
Los alquenos exhiben un conjunto de propiedades que se derivan directamente de su estructura no polar.

- Naturaleza no polar: Debido a la pequeña diferencia de electronegatividad entre el carbono y el hidrógeno, los alquenos son compuestos no polares. Esto los hace hidrofóbicos (insolubles en agua) pero solubles en disolventes orgánicos no polares como el hexano o el benceno.
- Puntos de Fusión y Ebullición: Al igual que en los alcanos, los puntos de fusión y ebullición aumentan a medida que aumenta el número de átomos de carbono (y por tanto, la masa molecular). Esto se debe al incremento de las fuerzas de dispersión de London entre las moléculas.
- Densidad: La densidad de los alquenos también aumenta con el tamaño de la molécula, aunque siempre son menos densos que el agua.
- Reactividad: Su actividad química es considerablemente mayor que la de los alcanos, especialmente en los miembros de cadena corta. El enlace pi es el centro de esta reactividad.
Métodos de Obtención de Alquenos
La síntesis de alquenos en el laboratorio o en la industria generalmente implica reacciones de eliminación, donde se eliminan dos sustituyentes de átomos de carbono adyacentes para formar el doble enlace. Algunos de los métodos más comunes son:
- Deshidrogenación de alcanos: La eliminación de hidrógeno (H₂) de un alcano a altas temperaturas y con un catalizador.
- Deshidratación de alcoholes: La eliminación de una molécula de agua de un alcohol, generalmente en presencia de un ácido fuerte como el ácido sulfúrico.
- Deshidrohalogenación de halogenoalcanos: La reacción de un halogenuro de alquilo con una base fuerte, que elimina un átomo de halógeno y un átomo de hidrógeno.
- Reacción de dihalogenoalcanos con zinc: Un dihalogenuro vecinal (con halógenos en carbonos adyacentes) puede reaccionar con polvo de zinc para eliminar ambos halógenos y formar el alqueno.
- Hidrogenación parcial de alquinos: La adición controlada de hidrógeno a un alquino (con triple enlace) utilizando catalizadores específicos (como el catalizador de Lindlar) permite detener la reacción en la etapa de alqueno.
El Corazón de la Reactividad: Reacciones Típicas
El grupo funcional de los alquenos, el doble enlace C=C, es una región de alta densidad electrónica debido al enlace pi. Esto lo convierte en un objetivo ideal para reactivos deficientes en electrones, conocidos como electrófilos. La reacción característica de los alquenos es la adición electrofílica.
Adición Electrofílica
Este es un mecanismo de dos pasos. Primero, el electrófilo es atacado por los electrones del enlace pi, rompiéndolo y formando un nuevo enlace simple con uno de los carbonos. Esto deja al otro carbono con una carga positiva, creando un intermediario altamente reactivo llamado carbocatión. En el segundo paso, una especie rica en electrones (nucleófilo) ataca rápidamente al carbocatión para formar el producto final. Ejemplos clásicos incluyen la adición de halógenos (Br₂), hidrácidos (HBr) o agua (hidratación).
Otras Reacciones Importantes
- Adición de Radicales Libres: En ciertas condiciones (por ejemplo, en presencia de peróxidos), la adición de HBr puede seguir un mecanismo de radicales libres, que a menudo conduce a un producto diferente al esperado por la adición electrofílica (anti-Markovnikov).
- Sustitución Alílica: No todas las reacciones ocurren en el doble enlace. En la posición alílica (el átomo de carbono adyacente al doble enlace), pueden ocurrir reacciones de sustitución, similares a las de los alcanos, donde un hidrógeno es reemplazado, por ejemplo, por un halógeno.
- Oxidación y Reducción: Los alquenos pueden ser oxidados para formar epóxidos, dioles o incluso romperse por completo. También pueden ser reducidos (hidrogenados) para formar los alcanos correspondientes mediante la adición de H₂ con un catalizador metálico.
- Polimerización: Quizás una de las reacciones más importantes a nivel industrial. Bajo las condiciones adecuadas, las moléculas de alqueno (monómeros) pueden unirse entre sí para formar cadenas muy largas llamadas polímeros, como el polietileno, a partir del eteno.
Preguntas Frecuentes (FAQ) sobre los Alquenos
¿Cuál es la principal diferencia entre un alcano y un alqueno?
La diferencia fundamental radica en sus enlaces de carbono. Los alcanos son hidrocarburos saturados, lo que significa que solo tienen enlaces simples (C-C). Los alquenos son insaturados, ya que contienen al menos un doble enlace (C=C). Esto también se refleja en su fórmula general: CₙH₂ₙ₊₂ para los alcanos y CₙH₂ₙ para los alquenos.
¿Por qué los alquenos son más reactivos que los alcanos?
La mayor reactividad de los alquenos se debe a la presencia del enlace pi (π). Los electrones en este enlace están más expuestos y menos fuertemente retenidos que los electrones en los enlaces sigma (σ). Esto los convierte en un sitio fácilmente atacable por reactivos electrofílicos, iniciando reacciones de adición que no son posibles en los alcanos.
¿Qué es un polímero derivado de un alqueno?
Es una macromolécula formada por la unión repetida de muchas unidades pequeñas de alqueno, llamadas monómeros. Por ejemplo, el polietileno, uno de los plásticos más comunes del mundo, se produce mediante la polimerización de miles de moléculas de eteno.
Si quieres conocer otros artículos parecidos a Alquenos: Fórmulas, Estructura y Reactividad puedes visitar la categoría Automovilismo.

