17/01/2020
En el vertiginoso mundo del automovilismo de alta competición, donde cada milésima de segundo cuenta, a menudo centramos nuestra atención en la aerodinámica, la potencia del motor o la habilidad del piloto. Sin embargo, existe una ciencia invisible y fundamental que dicta el rendimiento en la pista: la química. El combustible que fluye por las venas de un monoplaza de Fórmula 1 o de un coche de NASCAR no es simplemente un líquido; es una compleja obra de ingeniería molecular diseñada para liberar la máxima energía. Para comprender cómo se logra esto, debemos descender al nivel de los átomos y los enlaces que los unen. Hoy, utilizaremos como ejemplo el 1-penteno, un hidrocarburo de fórmula C₅H₁₀, para explorar una herramienta visual clave para los químicos: la Estructura de Lewis.

¿Qué es el 1-Penteno y Por Qué Nos Interesa?
El 1-penteno es un alqueno, un tipo de hidrocarburo que se caracteriza por tener al menos un doble enlace entre átomos de carbono. Su fórmula molecular, C₅H₁₀, nos dice que cada molécula está compuesta por cinco átomos de carbono y diez de hidrógeno. Si bien no es el componente exacto de los combustibles de competición (que son mezclas mucho más complejas y reguladas), pertenece a la misma gran familia de compuestos orgánicos. Entender su estructura nos abre la puerta a comprender cómo se comportan moléculas más grandes y cómo su forma y enlaces determinan propiedades cruciales como el octanaje y la eficiencia de la combustión, factores decisivos en cualquier carrera.
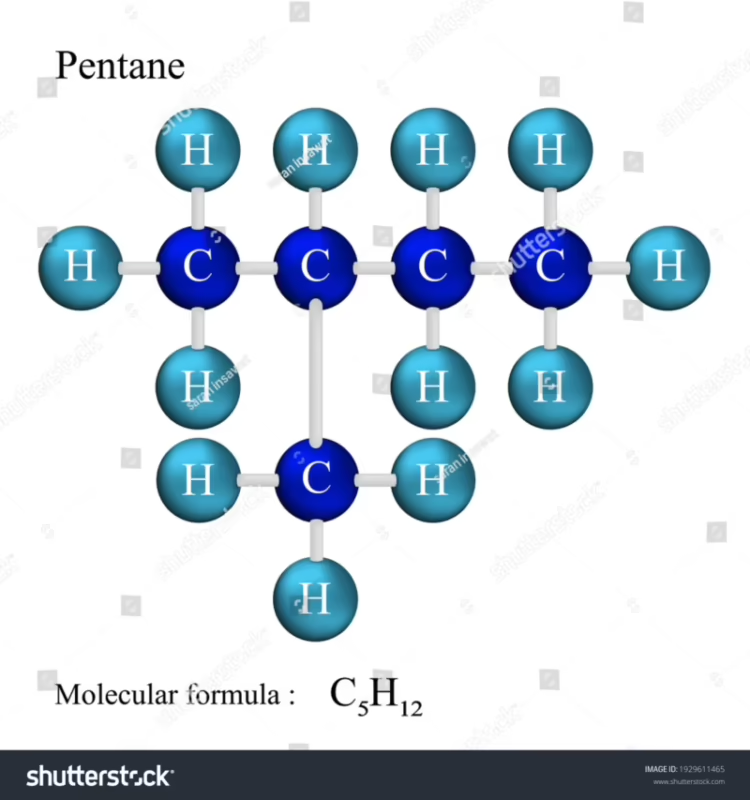
Desentrañando la Molécula: La Estructura de Lewis
Propuesta por primera vez por el químico Gilbert Lewis en 1916, la Estructura de Lewis (también conocida como diagrama de puntos) es una representación gráfica bidimensional de una molécula. Su propósito es mostrar no solo qué átomos están conectados entre sí, sino también cómo se distribuyen los electrones de valencia, que son los electrones de la capa más externa de un átomo y los responsables de la formación de enlaces químicos.
En estos diagramas:
- Cada átomo se representa con su símbolo químico (por ejemplo, 'C' para carbono, 'H' para hidrógeno).
- Los enlaces covalentes (donde los átomos comparten electrones) se dibujan como líneas entre los átomos. Una línea representa un enlace simple (dos electrones compartidos), dos líneas un enlace doble (cuatro electrones) y tres líneas un enlace triple (seis electrones).
- Los electrones de valencia que no participan en los enlaces, conocidos como pares solitarios o pares no enlazantes, se representan como pares de puntos alrededor de su átomo correspondiente.
Esta sencilla herramienta visual es increíblemente poderosa, ya que nos permite predecir la geometría de una molécula y entender su reactividad, un conocimiento vital para los ingenieros químicos que diseñan desde combustibles hasta los polímeros de los neumáticos.
Construyendo un Diagrama de Lewis Paso a Paso
Elaborar una Estructura de Lewis sigue un método lógico. Aunque al principio pueda parecer complejo, seguir una serie de pasos ordenados simplifica enormemente el proceso.

- Contar el total de electrones de valencia: Se suma el número de electrones de valencia de cada átomo en la molécula. Para iones, se resta un electrón por cada carga positiva y se suma uno por cada carga negativa.
- Determinar el átomo central: Generalmente, es el átomo menos electronegativo (excluyendo al hidrógeno) o el que aparece en menor cantidad en la fórmula. En cadenas de carbono, los carbonos forman el esqueleto central.
- Dibujar el esqueleto molecular: Se conectan los átomos mediante enlaces simples al átomo central o entre sí para formar la cadena principal. Cada enlace simple utiliza dos electrones de valencia.
- Distribuir los electrones restantes: Los electrones que no se usaron en los enlaces se distribuyen como pares solitarios, comenzando por los átomos más electronegativos (los átomos terminales) hasta completar su octeto, y luego se colocan los restantes en el átomo central.
- Verificar la regla del octeto: Si el átomo central no tiene ocho electrones, se forman enlaces dobles o triples moviendo pares solitarios de los átomos terminales para compartirlos con el átomo central.
La Regla del Octeto: La Búsqueda de Estabilidad
El pilar fundamental detrás de la construcción de las Estructuras de Lewis es la regla del octeto. Esta regla empírica establece que los átomos tienden a formar enlaces de manera que cada átomo quede rodeado por ocho electrones de valencia (similar a la configuración de un gas noble), lo que les confiere una gran estabilidad. Un enlace covalente cuenta como dos electrones para cada uno de los átomos que une.
Sin embargo, como en toda regla, existen excepciones importantes:
- Octeto incompleto: Elementos como el berilio (Be) o el boro (B) pueden ser estables con menos de ocho electrones. El hidrógeno (H) es la excepción más común, ya que alcanza su máxima estabilidad con solo dos electrones (un enlace simple).
- Octeto expandido: Los elementos del tercer período en adelante (como el fósforo, P, o el azufre, S) pueden albergar más de ocho electrones en su capa de valencia, ya que tienen orbitales 'd' disponibles para alojar estos electrones extra.
Análisis del 1-Penteno (C₅H₁₀)
Apliquemos lo aprendido a nuestro ejemplo, el 1-penteno. Su nombre nos indica que es una cadena de 5 carbonos ('pent-') y que tiene un doble enlace ('-eno') en la primera posición ('1-').
- Electrones de valencia: El carbono (Grupo 14) tiene 4 electrones de valencia. El hidrógeno (Grupo 1) tiene 1. Total = (5 x 4) + (10 x 1) = 20 + 10 = 30 electrones de valencia.
- Esqueleto: Formamos una cadena de 5 carbonos. Colocamos un doble enlace entre el primer y el segundo carbono, y enlaces simples entre los demás.
- Añadir hidrógenos: Completamos los cuatro enlaces que cada carbono necesita añadiendo átomos de hidrógeno.
- C1 (con doble enlace): Necesita 2 H.
- C2 (con doble enlace y un enlace simple): Necesita 1 H.
- C3 (con dos enlaces simples): Necesita 2 H.
- C4 (con dos enlaces simples): Necesita 2 H.
- C5 (terminal con un enlace simple): Necesita 3 H.
Total de hidrógenos: 2+1+2+2+3 = 10. Coincide con la fórmula.
- Verificación: Contemos los electrones en los enlaces. Hay 4 enlaces C-C (uno de ellos doble) y 10 enlaces C-H. El doble enlace cuenta como 4 electrones, los 3 C-C simples como 6, y los 10 C-H como 20. Total = 4 + 6 + 20 = 30 electrones. Todos los electrones de valencia se han utilizado para formar los enlaces. No hay pares solitarios en esta molécula.
La estructura de Lewis nos muestra claramente el doble enlace, una zona de alta densidad de electrones que hace a la molécula más reactiva que su contraparte saturada, el pentano (C₅H₁₂) y que influye directamente en cómo se quema y cuánta energía libera.
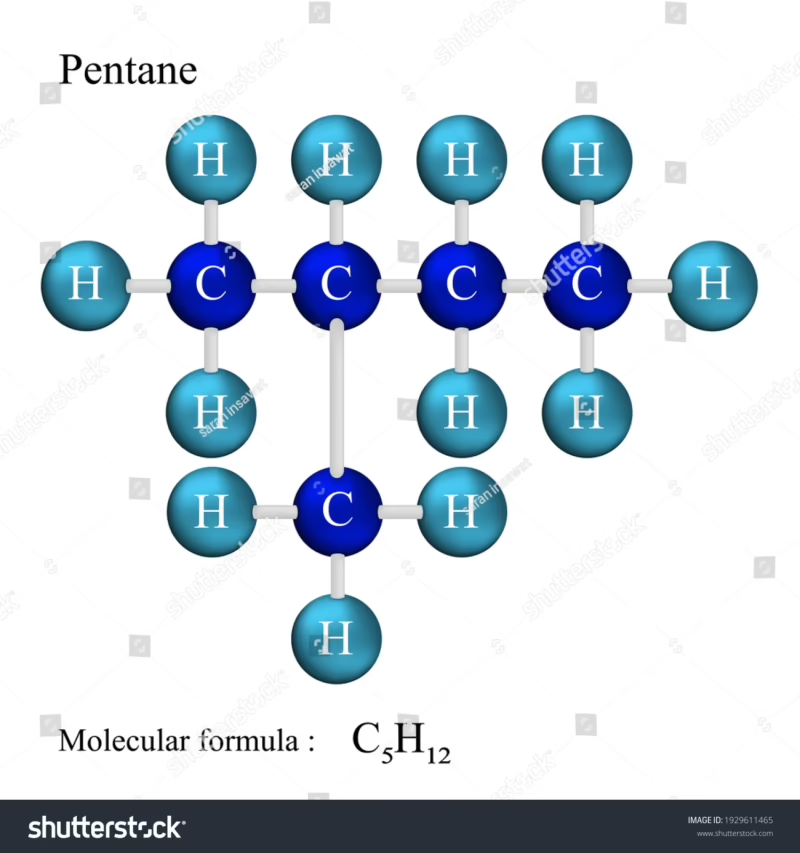
Conceptos Avanzados: Carga Formal y Resonancia
A veces, una sola Estructura de Lewis no es suficiente para describir una molécula. Aquí entran en juego dos conceptos más avanzados.
Carga Formal
La carga formal es una "carga" teórica asignada a un átomo en una molécula, asumiendo que los electrones en los enlaces se comparten por igual. Ayuda a determinar cuál de varias posibles estructuras de Lewis es la más estable (generalmente, aquella con las cargas formales más cercanas a cero). Se calcula con la fórmula:
Carga Formal = (Nº de e⁻ de valencia del átomo libre) – (Nº de e⁻ no enlazantes) – (1/2 * Nº de e⁻ enlazantes)
Resonancia
En ciertas moléculas o iones, es posible dibujar varias estructuras de Lewis válidas que solo difieren en la posición de los electrones (generalmente de dobles enlaces y pares solitarios). Este es el caso del ion nitrato (NO₃⁻), por ejemplo. En la realidad, la molécula no alterna entre estas formas, sino que existe como un híbrido promedio de todas ellas, un fenómeno llamado resonancia. Los enlaces en estas moléculas son idénticos entre sí, con una longitud y fuerza intermedias entre un enlace simple y uno doble. La resonancia confiere una gran estabilidad a la molécula.
Tabla Comparativa de Fórmulas Químicas
| Tipo de Fórmula | Descripción | Ejemplo (1-Penteno) |
|---|---|---|
| Fórmula Molecular | Indica el tipo y número de átomos en la molécula, sin mostrar su disposición. | C₅H₁₀ |
| Fórmula Estructural Condensada | Muestra la conexión de los átomos de forma abreviada en una línea. | CH₂=CHCH₂CH₂CH₃ |
| Estructura de Lewis | Representa todos los átomos, enlaces y pares de electrones solitarios. | (Descripción gráfica de todos los enlaces C-C, C=C y C-H) |
| Fórmula Esquelética | Representa el esqueleto de carbono como líneas en zigzag. Los vértices son carbonos y los hidrógenos se omiten. | Una línea en zigzag de 4 segmentos con una línea doble en el primer segmento. |
Preguntas Frecuentes (FAQ)
- ¿Por qué es importante la estructura de una molécula de combustible?
- La estructura determina cómo se rompen los enlaces durante la combustión. Las moléculas ramificadas, por ejemplo, tienden a quemarse de manera más controlada y uniforme que las cadenas lineales, lo que previene la detonación (o "picado de bielas") y permite mayores relaciones de compresión en el motor. Esto se traduce directamente en más potencia y eficiencia.
- ¿Qué es un isómero? ¿El 1-penteno tiene isómeros?
- Los isómeros son moléculas que tienen la misma fórmula molecular pero diferente estructura. El C₅H₁₀ tiene muchos isómeros, como el 2-penteno (el doble enlace está en el segundo carbono) o el ciclopentano (los cinco carbonos forman un anillo). Cada isómero tiene propiedades físicas y químicas distintas, a pesar de estar hecho de los mismos átomos.
- ¿Qué diferencia hay entre un enlace simple y un enlace doble?
- Un enlace simple comparte dos electrones, mientras que un doble enlace comparte cuatro. Esto hace que el enlace doble sea más corto, más fuerte y más rígido que un enlace simple. También es una zona de mayor reactividad química.
Desde el diseño de un alerón hasta la estrategia de paradas en boxes, el automovilismo es un deporte de detalles. La química del combustible es uno de esos detalles cruciales que, aunque invisible para el espectador, es una de las arenas más competitivas. Entender herramientas como la Estructura de Lewis nos permite apreciar la increíble complejidad y la ciencia precisa que se esconden detrás de cada rugido de motor en la línea de meta.
Si quieres conocer otros artículos parecidos a La Fórmula Secreta: Estructura de Lewis y Motor puedes visitar la categoría Automovilismo.

