22/01/2020
El alcohol butílico, conocido técnicamente como butanol, es un compuesto orgánico fascinante y multifacético que juega un papel crucial en numerosas industrias. Aunque su nombre puede no ser tan familiar como el del etanol o el metanol, su importancia es innegable. Se presenta como un líquido incoloro, con un olor característico a menudo descrito como similar al de un plátano dulce pero con un toque alcohólico áspero. Desde su uso como solvente en la fabricación de pinturas y lacas hasta su emergente rol como un biocombustible de nueva generación con potencial para superar al etanol, el butanol es una molécula con una historia rica y un futuro prometedor. En este artículo, exploraremos en profundidad su fórmula química, sus diferentes formas o isómeros, sus propiedades, métodos de producción, aplicaciones y las precauciones de seguridad necesarias para su manejo.

- ¿Qué es Exactamente el Alcohol Butílico?
- Fórmula y Estructura Molecular del Butanol
- Los Isómeros del Butanol: Cuatro Caras de la Misma Moneda
- Propiedades Físicas y Químicas Clave
- ¿Cómo se Produce el Alcohol Butílico?
- Aplicaciones y Usos Industriales del Butanol
- Butanol vs. Etanol como Biocombustible
- Seguridad, Riesgos y Manejo
- Preguntas Frecuentes (FAQ)
¿Qué es Exactamente el Alcohol Butílico?
El alcohol butílico o butanol es un alcohol primario con una estructura de cuatro átomos de carbono. Su fórmula química general es C₄H₉OH. Pertenece al grupo de los llamados “alcoholes de fusel”, que son alcoholes con más de dos átomos de carbono y que tienen una solubilidad significativa en agua. Este compuesto no solo se sintetiza a escala industrial, sino que también se encuentra en la naturaleza. Es un subproducto menor que se genera durante la fermentación de azúcares y otros carbohidratos por parte de ciertos microorganismos, lo que explica su presencia en pequeñas cantidades en muchas bebidas alcohólicas como la cerveza y el vino, y en alimentos fermentados. De hecho, su presencia es tan común que está permitido como saborizante artificial en Estados Unidos, utilizándose para crear aromas de mantequilla, crema, frutas, ron y whisky en una amplia gama de productos comestibles.
Fórmula y Estructura Molecular del Butanol
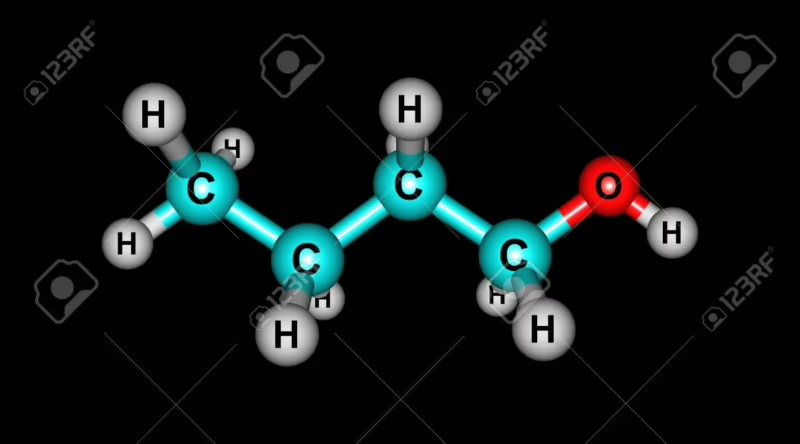
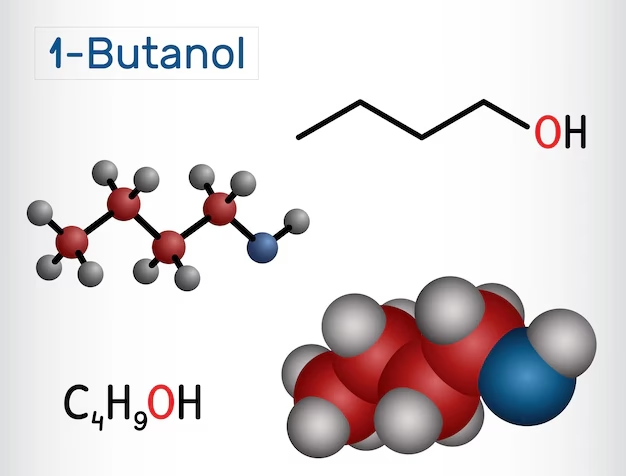
Comprender la fórmula y la estructura del butanol es fundamental para entender sus propiedades y comportamiento. La fórmula química puede representarse de varias maneras, cada una ofreciendo un nivel diferente de detalle:
- Fórmula Molecular: C₄H₁₀O. Esta fórmula nos indica la cantidad total de átomos de cada elemento en la molécula (4 de carbono, 10 de hidrógeno y 1 de oxígeno), pero no cómo están conectados.
- Fórmula Semidesarrollada: C₄H₉OH. Esta es más específica, ya que muestra el grupo funcional hidroxilo (-OH) que caracteriza a los alcoholes, unido a un grupo butilo (C₄H₉).
- Fórmula Estructural Desarrollada (para el n-butanol): CH₃-CH₂-CH₂-CH₂-OH. Esta es la representación más clara, mostrando la cadena lineal de cuatro carbonos con el grupo hidroxilo en un extremo.
La estructura del butan-1-ol (su nombre IUPAC) es la de un alcohol primario, lo que significa que el átomo de carbono al que está unido el grupo -OH está, a su vez, unido a un solo átomo de carbono adicional. Esta estructura es clave para sus reacciones químicas y sus propiedades como solvente.
Los Isómeros del Butanol: Cuatro Caras de la Misma Moneda
Una de las características más interesantes del butanol es que existe en cuatro formas diferentes, conocidas como isómeros. Todos comparten la misma fórmula molecular (C₄H₁₀O), pero la disposición de sus átomos es distinta, lo que les confiere propiedades físicas y químicas únicas.
Tabla Comparativa de los Isómeros del Butanol
| Nombre Común | Nombre IUPAC | Estructura | Tipo de Alcohol | Punto de Ebullición |
|---|---|---|---|---|
| n-butanol | Butan-1-ol | CH₃CH₂CH₂CH₂OH | Primario | 117.7 °C |
| Isobutanol | 2-metilpropan-1-ol | (CH₃)₂CHCH₂OH | Primario | 108 °C |
| sec-butanol | Butan-2-ol | CH₃CH(OH)CH₂CH₃ | Secundario | 99.5 °C |
| tert-butanol | 2-metilpropan-2-ol | (CH₃)₃COH | Terciario | 82.4 °C |
Como se puede observar, el n-butanol (normal-butanol) tiene la estructura de cadena lineal. El isobutanol tiene una cadena ramificada. El sec-butanol (secundario) tiene el grupo -OH en un carbono interno de la cadena lineal, y el tert-butanol (terciario) tiene el grupo -OH en un carbono central unido a otros tres carbonos. Estas diferencias estructurales afectan drásticamente a sus puntos de ebullición, solubilidad y reactividad.

Propiedades Físicas y Químicas Clave
El n-butanol, siendo el isómero más común y de mayor uso industrial, posee un conjunto de propiedades que definen sus aplicaciones.
- Peso Molecular: 74.12 g/mol
- Apariencia: Líquido incoloro y refractivo.
- Olor: Alcohólico, dulce, similar al plátano.
- Punto de Ebullición: 117.7 °C
- Punto de Fusión: –89.8 °C
- Densidad: 0.81 g/cm³ a 20 °C
- Solubilidad: Moderadamente soluble en agua, pero miscible con la mayoría de los solventes orgánicos comunes como etanol y éter.
- Punto de Inflamación: 37 °C (copa cerrada), lo que lo clasifica como un líquido inflamable.
- Acidez (pKa): Alrededor de 16.10, similar a otros alcoholes primarios.
¿Cómo se Produce el Alcohol Butílico?
La producción de butanol se realiza principalmente a través de dos rutas: la petroquímica y la biotecnológica.
1. Síntesis Petroquímica
La ruta dominante a nivel comercial parte de materias primas derivadas del petróleo. El proceso más común es la oxo-reacción del propeno (un subproducto del refinado del petróleo). En este proceso, el propeno reacciona con monóxido de carbono e hidrógeno (gas de síntesis) para formar una mezcla de n-butiraldehído e isobutiraldehído. Estos aldehídos son posteriormente hidrogenados para producir n-butanol e isobutanol, que se separan por destilación.
2. Fermentación Biotecnológica (Proceso ABE)
Históricamente, el butanol se producía mediante un proceso de fermentación conocido como ABE (Acetona-Butanol-Etanol). Este proceso utiliza cepas de bacterias del género Clostridium (como Clostridium acetobutylicum) para fermentar biomasa rica en azúcares (como maíz o melaza). Aunque este método fue desplazado por la producción petroquímica más barata, ha resurgido con fuerza debido al interés en los biocombustibles y las materias primas renovables. La investigación actual se centra en optimizar estas bacterias y utilizar biomasa no alimentaria (celulósica) para hacer el proceso más sostenible y económicamente viable.

Aplicaciones y Usos Industriales del Butanol
La versatilidad del butanol le permite tener un amplio abanico de aplicaciones en diferentes sectores.
- Solvente Industrial: Es quizás su uso más extendido. Actúa como un excelente solvente para pinturas, lacas, barnices, resinas naturales y sintéticas, gomas, aceites vegetales y alcaloides. Su tasa de evaporación relativamente lenta es ideal para acabados de superficies, ya que evita que la pintura se seque demasiado rápido.
- Intermediario Químico: Sirve como materia prima para la síntesis de una gran variedad de otros productos químicos. Por ejemplo, se utiliza para fabricar acrilato de butilo (para pinturas y adhesivos), acetato de butilo (un solvente y saborizante) y plastificantes como el ftalato de dibutilo.
- Industria Alimentaria y de Fragancias: Como se mencionó, se utiliza como agente saborizante artificial para recrear sabores afrutados y cremosos en helados, dulces, productos horneados y bebidas.
- Potencial como Biocombustible: El biobutanol es considerado un biocombustible superior al etanol por varias razones. Tiene una mayor densidad energética (más energía por litro), es menos corrosivo para los motores y las tuberías, y no se mezcla tan fácilmente con el agua, lo que simplifica su almacenamiento y transporte. Podría utilizarse directamente en motores de gasolina sin necesidad de grandes modificaciones.
Butanol vs. Etanol como Biocombustible
| Propiedad | Butanol | Etanol |
|---|---|---|
| Densidad Energética (MJ/L) | ~29.2 | ~21.2 |
| Higroscopicidad (Afinidad por el agua) | Baja | Alta |
| Corrosividad | Baja, similar a la gasolina | Alta |
| Presión de Vapor | Baja | Alta |
| Compatibilidad con Motores | Alta, puede usarse en concentraciones mayores | Limitada, requiere modificaciones (E85) |
Seguridad, Riesgos y Manejo
A pesar de sus múltiples beneficios, el butanol es una sustancia química que debe manejarse con precaución.
- Inflamabilidad: Es un líquido altamente inflamable. Sus vapores pueden formar mezclas explosivas con el aire, por lo que debe almacenarse lejos de fuentes de calor, chispas o llamas abiertas.
- Toxicidad: Es perjudicial si se ingiere. El contacto directo puede causar irritación severa en los ojos y la piel.
- Riesgos por Inhalación: La exposición a altas concentraciones de sus vapores puede irritar el tracto respiratorio y causar depresión del sistema nervioso central, cuyos síntomas incluyen somnolencia, mareos y dolor de cabeza.
Es imprescindible utilizar equipo de protección personal adecuado, como guantes, gafas de seguridad y trabajar en áreas bien ventiladas al manipular alcohol butílico.
Preguntas Frecuentes (FAQ)
¿Cuál es la fórmula del alcohol n-butílico?
La fórmula más común para representar el n-butanol (butan-1-ol) es C₄H₉OH. Su fórmula molecular es C₄H₁₀O y su estructura lineal es CH₃CH₂CH₂CH₂OH.

¿Qué tipo de alcohol es el butílico?
El n-butanol y el isobutanol son alcoholes primarios. El sec-butanol es un alcohol secundario y el tert-butanol es un alcohol terciario. Todos ellos pertenecen al grupo de los alcoholes de fusel.
¿Es el butanol seguro para el consumo humano?
No. A diferencia del etanol (presente en bebidas alcohólicas), el butanol es tóxico y no es apto para el consumo. Su ingestión puede causar graves problemas de salud.
¿Por qué se considera al butanol un buen candidato a biocombustible?
Principalmente por su mayor densidad energética en comparación con el etanol, lo que se traduce en una mejor autonomía del vehículo. Además, es menos corrosivo y se separa más fácilmente del agua, lo que lo hace más compatible con la infraestructura de distribución y los motores existentes.
Si quieres conocer otros artículos parecidos a Alcohol Butílico: Fórmula, Usos y Potencial puedes visitar la categoría Automovilismo.