19/08/2023
En el vertiginoso mundo del automovilismo deportivo, la atención suele centrarse en la aerodinámica, la pericia del piloto o la potencia bruta del motor. Sin embargo, en el corazón de cada bestia de competición, fluye un componente vital que a menudo pasa desapercibido pero que es tan crucial como cualquier otro: el combustible. No hablamos de la gasolina que cargas en tu coche de calle; nos referimos a una pócima química diseñada con precisión milimétrica para extraer hasta la última gota de rendimiento. Hoy nos sumergiremos en ese universo molecular para desentrañar los secretos de compuestos como el 2-metilheptano y entender por qué la química es, en realidad, una de las disciplinas más importantes en cualquier equipo de carreras.

¿Qué es el 2-Metilheptano? La Anatomía de un Componente Clave
A primera vista, el nombre "2-metilheptano" puede sonar intimidante y más propio de un laboratorio que de un paddock de Fórmula 1. Sin embargo, su estructura y propiedades son fundamentales para comprender cómo funciona un combustible de alto rendimiento. Se trata de un compuesto orgánico, específicamente un alcano de cadena ramificada. Su fórmula molecular es C8H18, lo que significa que cada molécula está compuesta por 8 átomos de carbono y 18 de hidrógeno.
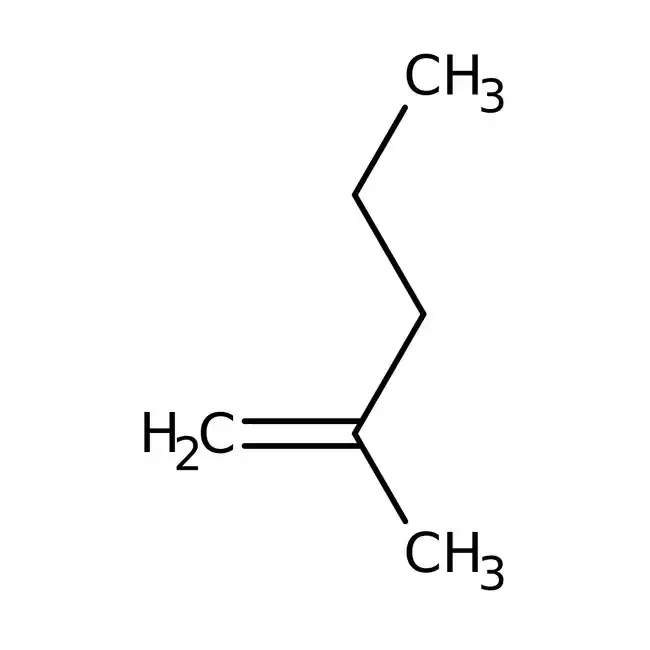
La clave de su nombre y de su comportamiento reside en su estructura. Imaginemos una cadena principal de siete átomos de carbono, lo que en química se conoce como "heptano". Ahora, en el segundo carbono de esa cadena, se engancha un pequeño grupo adicional de un carbono, llamado "grupo metilo". Esta ramificación es lo que lo diferencia del n-heptano (heptano de cadena lineal) y le confiere propiedades radicalmente diferentes y mucho más deseables para un motor de combustión interna. Físicamente, es un líquido incoloro, con un olor característico a hidrocarburo, insoluble en agua pero muy soluble en otros disolventes orgánicos. Esta naturaleza no polar es típica de los componentes de la gasolina.
La Importancia del Octanaje: De la Calle al Circuito
Aquí es donde el 2-metilheptano se convierte en una estrella. Para entender su rol, debemos hablar del concepto de octanaje. En un motor de alta compresión, como los utilizados en competición, la mezcla de aire y combustible se somete a una presión extrema antes de que la bujía genere la chispa. Si el combustible no es lo suficientemente estable, puede auto-encenderse prematuramente debido a la presión y el calor, un fenómeno conocido como "picado de bielas" o detonación. Esta combustión descontrolada es el enemigo silencioso de cualquier motor: reduce la potencia, genera un estrés mecánico brutal y puede destruir los componentes internos en cuestión de segundos.
El índice de octano es la medida de la capacidad de un combustible para resistir esta detonación. La escala se estableció utilizando dos compuestos de referencia:
- N-heptano: Un alcano de cadena lineal, muy propenso a la detonación. Se le asignó un valor de octano de 0.
- Iso-octano (2,2,4-trimetilpentano): Un isómero del octano (misma fórmula C8H18, pero diferente estructura) muy ramificado y extremadamente resistente a la detonación. Se le asignó un valor de octano de 100.
El 2-metilheptano, al ser un isómero ramificado del octano, tiene un índice de octano significativamente mayor que el n-heptano, aunque menor que el del iso-octano de referencia. Su estructura ramificada lo hace más estable y menos propenso a la combustión espontánea. Por ello, compuestos como este son ingredientes valiosos en la formulación de gasolinas de alto octanaje. Los ingenieros químicos de equipos como Ferrari o Red Bull Racing juegan con las proporciones de estos y otros cientos de compuestos para crear un combustible que maximice el rendimiento sin riesgo de detonación, ajustándose siempre a las estrictas regulaciones de la FIA.
Tabla Comparativa de Isómeros y Octanaje
Para visualizar mejor el impacto de la estructura molecular en el rendimiento del combustible, observemos la siguiente tabla comparativa. Todos son isómeros (excepto el n-heptano, usado como referencia de bajo octanaje) con la misma cantidad de átomos, pero su organización lo cambia todo.
| Compuesto | Fórmula Molecular | Estructura | Índice de Octano (RON Aprox.) |
|---|---|---|---|
| n-Heptano | C7H16 | Lineal | 0 |
| n-Octano | C8H18 | Lineal | -20 |
| 2-Metilheptano | C8H18 | Ligeramente Ramificada | 23 |
| Iso-octano (2,2,4-trimetilpentano) | C8H18 | Altamente Ramificada | 100 |
Más Allá del 2-Metilheptano: Un Ballet Químico
Un combustible de competición es mucho más que un solo compuesto. Es una mezcla compleja donde cada molécula tiene un propósito. Junto a alcanos como el 2-metilheptano, encontramos otros actores. Por ejemplo, el 2-metil-1-penteno (fórmula C6H12). A diferencia de los alcanos, que solo tienen enlaces simples entre carbonos, los alquenos como este poseen un doble enlace. Estos dobles enlaces pueden influir en la velocidad de combustión y en el índice de octano, añadiendo otra variable al complejo rompecabezas de la formulación.
Además, los combustibles de competición modernos, como los de la Fórmula 1, contienen aditivos específicos:
- Oxigenantes: Compuestos como el etanol que contienen oxígeno en su molécula. Esto asegura una combustión más completa y eficiente, lo que se traduce en más potencia.
- Detergentes: Mantienen limpios los inyectores y las válvulas, asegurando que el motor funcione a su máximo potencial durante toda la carrera.
- Modificadores de fricción: Reducen la fricción interna en el motor, liberando unos pocos caballos de fuerza adicionales que pueden marcar la diferencia entre ganar y perder.
Todo este ballet químico es desarrollado en laboratorios de alta tecnología por socios de los equipos, como Shell para Ferrari o Petronas para Mercedes. Cada nueva evolución del motor requiere una nueva formulación de combustible, en una carrera armamentista química que se libra lejos de las cámaras pero que es igual de intensa que la que vemos en la pista.

Preguntas Frecuentes (FAQ)
¿Por qué la estructura ramificada de un hidrocarburo aumenta el octanaje?
Una estructura ramificada es inherentemente más estable y compacta. Durante la compresión en el cilindro, las moléculas lineales como el n-heptano pueden romperse más fácilmente y formar radicales libres que inician la combustión prematura (detonación). Las moléculas ramificadas como el iso-octano o el 2-metilheptano resisten mucho mejor esta ruptura, permitiendo alcanzar mayores niveles de compresión antes de que salte la chispa, lo que se traduce en una mayor eficiencia y potencia.
¿Los coches de calle usan los mismos combustibles que los de F1?
No, en absoluto. Aunque comparten principios básicos, los combustibles de competición son formulaciones a medida, extremadamente caras y diseñadas para un único propósito: máximo rendimiento en un motor específico bajo condiciones extremas. La gasolina comercial está diseñada para un equilibrio entre rendimiento, durabilidad del motor, eficiencia de costes y emisiones en una amplia variedad de vehículos y condiciones.
¿Qué es un isómero y por qué es tan importante para el combustible?
Un isómero es un compuesto que tiene la misma fórmula molecular que otro (mismo número y tipo de átomos) pero una estructura diferente. Como vimos en la tabla, el n-octano, el 2-metilheptano y el iso-octano son todos C8H18. Sin embargo, su diferente disposición estructural les confiere propiedades físicas y químicas drásticamente distintas, especialmente en lo que respecta a su resistencia a la detonación. La capacidad de crear y mezclar isómeros específicos es la base de la formulación de combustibles de alto octanaje.
¿El 2-metilheptano es el único compuesto importante en la gasolina de competición?
Definitivamente no. Es un ejemplo de un tipo de componente valioso (alcano ramificado), pero un combustible de competición puede contener cientos de compuestos diferentes. La magia reside en la mezcla precisa y sinérgica de alcanos, alquenos, compuestos aromáticos y aditivos para lograr las características deseadas de octanaje, velocidad de llama, densidad energética y limpieza.
En conclusión, la próxima vez que veas un monoplaza de F1 o un coche de rally surcando el asfalto o la tierra, recuerda que su increíble rendimiento no solo se debe a la ingeniería mecánica, sino también a la sangre que corre por sus venas: un combustible de diseño, una obra maestra de la química donde moléculas como el 2-metilheptano juegan un papel silencioso pero absolutamente heroico en la búsqueda de la gloria.
Si quieres conocer otros artículos parecidos a La Química Secreta del Combustible de Carreras puedes visitar la categoría Automovilismo.

