28/08/2019
En el vertiginoso mundo del automovilismo deportivo, a menudo centramos nuestra atención en la aerodinámica, la potencia del motor o la habilidad del piloto. Sin embargo, detrás de cada récord de vuelta y cada victoria aplastante, existe una ciencia invisible pero fundamental: la química. Compuestos que parecen pertenecer exclusivamente a un laboratorio desempeñan un papel crucial en la búsqueda de la máxima performance. Hoy nos sumergiremos en el corazón de esta ciencia para desvelar cómo una simple fórmula, AlCl₃, y el elemento que la origina, el aluminio, son pilares inesperados en la construcción y el funcionamiento de los coches de carreras más avanzados del planeta.

Entendiendo los Fundamentos: El Baile de Electrones del Aluminio y el Cloro
Para comprender el impacto del Cloruro de Aluminio, primero debemos entender a sus componentes por separado. Todo comienza en la tabla periódica, donde cada elemento tiene una configuración electrónica que define su comportamiento y su deseo de reaccionar con otros.

El Aluminio (Al): Un Donante Generoso
El Aluminio es un metal con número atómico 13. Esto significa que un átomo neutro de aluminio tiene 13 protones en su núcleo y 13 electrones orbitando a su alrededor. Su configuración electrónica en estado fundamental es 1s² 2s² 2p⁶ 3s² 3p¹. Los electrones más importantes para las reacciones químicas son los que se encuentran en la capa más externa, en este caso, los tres electrones en la tercera capa (3s² 3p¹). La naturaleza tiende a la estabilidad, y para los átomos, esto a menudo significa tener su capa de electrones externa completa, similar a la de un gas noble. Para el aluminio, es mucho más fácil perder esos 3 electrones externos que ganar 5 para completar la capa. Al perder tres electrones, se convierte en un ion con carga positiva, el catión Aluminio (Al³⁺). Su nueva configuración electrónica es 1s² 2s² 2p⁶, que es idéntica a la del gas noble Neón, alcanzando así un estado de gran estabilidad. Ahora, con 13 protones y solo 10 electrones, su carga neta es +3.
El Cloro (Cl): Un Receptor Ansioso
Por otro lado, tenemos el Cloro, un no metal con número atómico 17. Su configuración electrónica es 1s² 2s² 2p⁶ 3s² 3p⁵. A su capa externa le falta un solo electrón para estar completa y asemejarse a la del gas noble Argón. Por lo tanto, el Cloro tiene una fuerte tendencia a capturar un electrón para lograr esa estabilidad. Cuando lo hace, se convierte en un ion con carga negativa, el anión Cloruro (Cl⁻). Con 17 protones y 18 electrones, su carga neta es -1 y su configuración electrónica (1s² 2s² 2p⁶ 3s² 3p⁶) es ahora la del Argón.
La Fórmula de la Unión Perfecta: Nace el Cloruro de Aluminio (AlCl₃)
En la química, como en la vida, los opuestos se atraen. El catión Al³⁺ con su carga positiva y el anión Cl⁻ con su carga negativa sienten una fuerte atracción electrostática. Sin embargo, para formar un compuesto iónico neutro, las cargas deben equilibrarse perfectamente. Un solo ion de Aluminio tiene una carga de +3, mientras que un ion de Cloruro tiene una carga de -1. Para que la suma total sea cero, necesitamos tres iones de Cloruro por cada ion de Aluminio (+3 + (3 x -1) = 0). De esta necesidad de equilibrio nace la fórmula química del compuesto: Cloruro de Aluminio, o AlCl₃. Este mismo principio se aplica a otros elementos con comportamientos similares, como el Galio (Ga), que también forma el ion Ga³⁺ y se combina con el cloro para crear Cloruro de Galio (GaCl₃).

Del Laboratorio a la Pista: El Rol Crítico del AlCl₃ en el Motorsport
Aquí es donde la química abstracta se encuentra con el asfalto. El Cloruro de Aluminio no es un material que encontremos en el chasis o el motor de un coche de F1, pero su papel como catalizador es fundamental en la producción de dos componentes vitales para el alto rendimiento: el combustible y los lubricantes.
Fabricando Combustible de Alto Octanaje
Los motores de competición, especialmente los de Fórmula 1 o WRC, operan bajo compresiones y temperaturas extremas. Para evitar la detonación prematura (conocida como 'picado' o 'knocking'), que puede destruir un motor en segundos, se requiere combustible con un altísimo índice de octanaje. El AlCl₃ es un catalizador ácido de Lewis extremadamente potente utilizado en un proceso petroquímico llamado alquilación de Friedel-Crafts. En términos sencillos, este proceso permite combinar moléculas de hidrocarburos más pequeñas y de bajo octanaje para crear moléculas más grandes y ramificadas, como el iso-octano, que es el estándar de referencia para la resistencia a la detonación. Gracias a catalizadores como el AlCl₃, las refinerías pueden producir los componentes de alta calidad que, mezclados en proporciones precisas, dan vida a los combustibles de competición que permiten a los motores entregar su máxima potencia de forma segura y eficiente.
Síntesis de Lubricantes y Polímeros
El Cloruro de Aluminio también actúa como catalizador en la polimerización y la isomerización de hidrocarburos, procesos clave para la creación de aceites lubricantes sintéticos de alto rendimiento. Estos lubricantes son esenciales para reducir la fricción entre las piezas móviles del motor, disipar el calor y garantizar la fiabilidad durante una carrera entera. Sin la química catalítica, donde el AlCl₃ es un protagonista, sería imposible formular los fluidos que soportan las brutales condiciones dentro de un motor de competición.
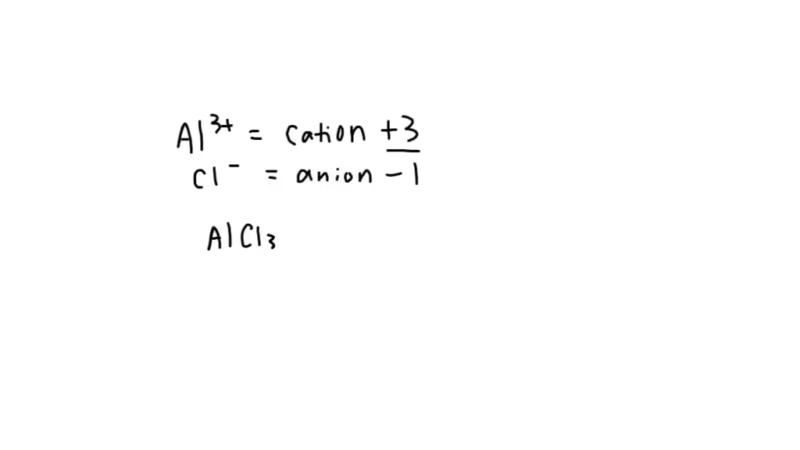
El Aluminio: El Metal Rey de la Pista
Si bien el Cloruro de Aluminio trabaja tras bambalinas, el elemento aluminio es una estrella en el escenario principal del motorsport. Sus propiedades lo convierten en un material casi perfecto para la construcción de coches de carreras.
- Baja Densidad: Es significativamente más ligero que el acero, lo que es crucial en un deporte donde cada gramo cuenta. Menos peso significa mejor aceleración, frenada y agilidad en las curvas.
- Alta Relación Resistencia-Peso: A pesar de su ligereza, ciertas aleaciones de aluminio ofrecen una resistencia estructural impresionante, ideal para componentes del chasis, suspensiones y llantas.
- Excelente Conductividad Térmica: Esta propiedad lo hace el material ideal para radiadores, intercoolers y pinzas de freno, ya que puede disipar el calor de manera muy eficiente, evitando el sobrecalentamiento.
Tabla Comparativa de Materiales en Motorsport
| Material | Densidad (g/cm³) | Ventajas Clave | Aplicaciones Comunes |
|---|---|---|---|
| Aleaciones de Aluminio | ~2.7 | Ligereza, conductividad térmica, buena resistencia, coste moderado. | Bloques de motor, pistones, llantas, radiadores, alerones. |
| Acero | ~7.8 | Alta resistencia, durabilidad, bajo coste. | Engranajes, cigüeñales, jaulas antivuelco (en algunas categorías). |
| Fibra de Carbono | ~1.6 | Relación resistencia-peso extrema, rigidez, moldeabilidad. | Chasis monocasco, carrocería, elementos aerodinámicos, suspensiones. |
| Titanio | ~4.5 | Resistencia similar al acero con 45% menos peso, resistencia a la corrosión. | Tornillería crítica, componentes de escape, piezas internas del motor. |
Preguntas Frecuentes (FAQ)
¿Por qué la fórmula es AlCl₃ y no simplemente AlCl?
La fórmula se debe a la necesidad de neutralidad eléctrica. El ion de aluminio (Al³⁺) tiene una carga de +3, mientras que el ion cloruro (Cl⁻) tiene una carga de -1. Se necesitan tres iones de cloruro para equilibrar la carga positiva de un solo ion de aluminio, resultando en la fórmula AlCl₃.
¿Entonces los coches de carreras llevan Cloruro de Aluminio en su interior?
No directamente. El AlCl₃ no es un componente del coche. Su función es la de ser un catalizador durante el proceso de fabricación de componentes esenciales, principalmente el combustible de alto octanaje y los lubricantes sintéticos que el coche sí utiliza.

¿Qué ventajas aporta el aluminio frente a la fibra de carbono?
Aunque la fibra de carbono tiene una relación resistencia-peso superior, el aluminio sigue siendo indispensable. Es mucho mejor conductor del calor, lo que lo hace ideal para sistemas de refrigeración. Además, su coste es inferior y su comportamiento ante impactos es diferente (se deforma, mientras que el carbono se fractura), siendo útil en ciertas estructuras de absorción de energía.
¿Por qué es importante para un ion como el Al³⁺ alcanzar la configuración de un gas noble?
Alcanzar la configuración electrónica de un gas noble (como el Neón para el Al³⁺) representa un estado de máxima estabilidad energética para un átomo. Los átomos reaccionan (pierden, ganan o comparten electrones) precisamente para alcanzar este estado estable, lo que dicta toda la química de formación de compuestos.
En conclusión, la próxima vez que veamos un monoplaza de F1 o un coche de rally devorando el asfalto, recordemos que su rendimiento no solo depende de la ingeniería visible. En su corazón late una compleja sinfonía de ciencia, donde la química de compuestos como el Cloruro de Aluminio juega una melodía silenciosa pero indispensable para alcanzar la máxima velocidad y fiabilidad.
Si quieres conocer otros artículos parecidos a Química de la Velocidad: El Secreto del AlCl₃ puedes visitar la categoría Automovilismo.
