07/03/2020
La herrumbre es un fenómeno tan común que a menudo pasamos por alto la compleja y fascinante química que ocurre en su formación. Desde una vieja herramienta en el garaje hasta componentes críticos en un coche de carreras, el óxido de hierro es una constante en nuestro mundo metálico. Pero, ¿qué sucede realmente a nivel molecular? La clave para entenderlo todo reside en dos términos que pueden sonar crípticos: Fe2 y Fe3. Estos no son compuestos, sino la representación de los dos principales estados de oxidación del hierro, los cuales dictan el tipo de óxido que se formará, su color, y sus propiedades. Acompáñanos en este profundo análisis para desentrañar los misterios de la oxidación y comprender de una vez por todas el proceso que transforma el brillante hierro en un polvo rojizo.

¿Qué Significan Realmente Fe2 y Fe3? Los Estados de Oxidación
Antes de sumergirnos en las complejas reacciones, es fundamental aclarar la base de todo: el significado de Fe2 y Fe3. En química, estos términos se refieren a los iones de hierro, es decir, átomos de hierro que han perdido electrones. El número indica cuántos electrones ha cedido el átomo.
- Fe2 (Hierro II): También conocido como ion ferroso (Fe²⁺), es un átomo de hierro que ha perdido dos electrones. Esto le confiere un estado de oxidación de +2. Los compuestos formados con este ion se denominan compuestos ferrosos.
- Fe3 (Hierro III): Conocido como ion férrico (Fe³⁺), es un átomo de hierro que ha perdido tres electrones, dándole un estado de oxidación de +3. Los compuestos que lo contienen se denominan compuestos férricos.
Esta diferencia, que parece tan pequeña como un solo electrón, es la responsable de la existencia de distintos tipos de óxidos de hierro, cada uno con características únicas. La herrumbre común que todos conocemos está predominantemente compuesta por óxido de hierro (III).
El Proceso de Oxidación: ¿Cómo Nace la Herrumbre?
La formación de la herrumbre es un proceso electroquímico que requiere de tres elementos indispensables: hierro (Fe), oxígeno (O₂) y agua (H₂O). Sin la presencia de agua o humedad en el aire, el proceso de oxidación del hierro es extremadamente lento. El agua actúa como un catalizador, un electrolito que facilita el movimiento de los electrones desde el hierro hacia el oxígeno.
El proceso se puede simplificar en una reacción general, pero en realidad es una serie de pasos. Cuando una gota de agua entra en contacto con una superficie de hierro, se crea una pequeña celda electroquímica. Una parte del hierro (el ánodo) comienza a disolverse, liberando electrones y formando iones Fe²⁺.

Estos electrones viajan a través del metal hacia otra zona de la superficie (el cátodo), donde reaccionan con el oxígeno disuelto en el agua para formar iones hidroxilo (OH⁻). Finalmente, los iones de hierro (Fe²⁺) reaccionan con los iones hidroxilo (OH⁻) para formar hidróxido de hierro (II), Fe(OH)₂. Este compuesto es rápidamente oxidado por más oxígeno para formar hidróxido de hierro (III), Fe(OH)₃, que es la sustancia inestable que, al perder agua, se convierte en el óxido de hierro (III) hidratado (Fe₂O₃·xH₂O), la sustancia que conocemos como herrumbre.
Existen ciertos factores que pueden acelerar drásticamente este proceso, como la presencia de sales (por eso los coches se oxidan más rápido en zonas costeras o donde se usa sal en las carreteras en invierno), la exposición a ácidos (lluvia ácida) o el contacto con metales menos activos.
La Ecuación Química de la Herrumbre Desglosada
Aunque el proceso es complejo, la reacción global de la formación de herrumbre se puede simplificar en la siguiente ecuación química:
4Fe + 3O₂ + 6H₂O → 4Fe(OH)₃
Esta fórmula nos dice que cuatro átomos de hierro reaccionan con tres moléculas de oxígeno y seis moléculas de agua para producir cuatro moléculas de hidróxido de hierro (III). Este hidróxido de hierro (III) es el precursor directo de la herrumbre. A medida que se deshidrata, se convierte en óxido férrico (Fe₂O₃), la capa porosa y rojiza que vemos en las superficies metálicas.
Óxido Ferroso vs. Óxido Férrico: Diferencias Clave
Como hemos visto, los estados de oxidación Fe2 y Fe3 dan lugar a dos óxidos de hierro principales con propiedades muy diferentes. Comprender sus distinciones es clave para entender la química del hierro.

| Característica | Óxido de Hierro (II) | Óxido de Hierro (III) |
|---|---|---|
| Nombre Común | Óxido ferroso | Óxido férrico, herrumbre |
| Fórmula Química | FeO | Fe₂O₃ |
| Estado de Oxidación del Hierro | +2 (Fe2) | +3 (Fe3) |
| Apariencia / Color | Polvo negro | Polvo rojizo-marrón |
| Estabilidad | Inestable por debajo de 575 °C | Estable, es el producto final de la corrosión |
Un Vistazo Profundo al Óxido Ferroso (FeO)
Aunque el óxido férrico es más conocido por ser el componente de la herrumbre, el óxido ferroso (FeO) también tiene un papel y unas características muy interesantes. A diferencia del óxido férrico, el FeO no se forma comúnmente por exposición al aire y al agua.
Preparación y Estructura
El óxido ferroso se puede preparar en laboratorio mediante la descomposición térmica del oxalato de hierro (II) en una atmósfera inerte para evitar su oxidación a óxido férrico. La reacción es la siguiente:
FeC₂O₄ → FeO + CO₂ + CO
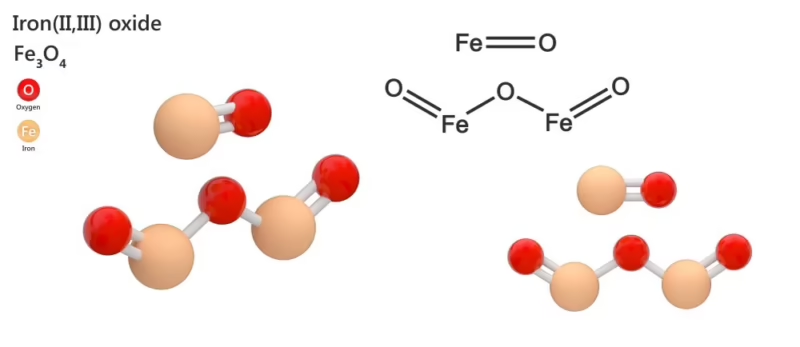
Estructuralmente, el FeO adopta una estructura cúbica similar a la sal de roca. Sin embargo, es termodinámicamente inestable por debajo de los 575 °C, tendiendo a descomponerse en hierro metálico y magnetita (Fe₃O₄), otro óxido de hierro que contiene tanto Fe²⁺ como Fe³⁺.
Usos y Ocurrencia Natural
A pesar de su inestabilidad, el óxido ferroso tiene aplicaciones prácticas. Es ampliamente utilizado como pigmento. De hecho, está aprobado por la FDA para su uso en cosméticos y también se emplea en algunas tintas para tatuajes. Otro uso interesante es como eliminador de fosfatos en acuarios domésticos, ayudando a mantener el agua limpia.
Sorprendentemente, el óxido ferroso constituye aproximadamente el 9% del manto terrestre. Se cree que su posible conductividad eléctrica dentro del manto podría explicar ciertas perturbaciones en la rotación de la Tierra que los modelos actuales no logran justificar por completo.
Preguntas Frecuentes (FAQ)
¿Es posible revertir el proceso de oxidación para recuperar el hierro puro?
No, al menos no mediante un proceso físico simple. La formación de herrumbre es un cambio químico. Si bien es posible reducir químicamente el óxido de hierro para obtener hierro metálico (un proceso fundamental en la siderurgia, utilizando altos hornos), no se puede simplemente "revertir" la reacción eliminando el agua o el oxígeno. El material original ya ha cambiado su composición química.
¿Qué factores aceleran la formación de herrumbre?
Varios factores pueden acelerar la corrosión del hierro. Los principales son la presencia de agua y oxígeno, pero el proceso se ve potenciado por la presencia de electrolitos como sales y ácidos. Además, las tensiones en el metal, las impurezas o el contacto con metales menos reactivos (más nobles) también crean las condiciones ideales para una oxidación más rápida.
¿Todo el óxido de hierro es de color rojizo-marrón?
No. El color rojizo-marrón es característico del óxido de hierro (III) o herrumbre. Sin embargo, como hemos visto, el óxido de hierro (II) o FeO es un polvo de color negro. Existe también la magnetita (Fe₃O₄), que es de color negro y es magnética. El color del óxido depende del estado de oxidación del hierro y de la estructura cristalina del compuesto.
Si quieres conocer otros artículos parecidos a Óxido de Hierro: El Secreto de Fe2 y Fe3 puedes visitar la categoría Automovilismo.
