03/01/2021
El rugido ensordecedor de un V8 de NASCAR, la sinfonía aguda de un motor de Fórmula 1 al límite de revoluciones o el brutal petardeo de un coche del WRC devorando un tramo de tierra. Todos estos sonidos, que son música para los oídos de cualquier aficionado al motorsport, tienen un origen común: una combustión controlada, violenta y extraordinariamente precisa. Pero, ¿qué hay detrás de esa explosión que genera la potencia? No es simple gasolina. Es un cóctel químico diseñado al milímetro, donde compuestos con nombres tan complejos como 2,3-dimetilpentano o 2,3-dimetil-2-buteno no son meras curiosidades de laboratorio, sino los verdaderos protagonistas silenciosos en la búsqueda de la victoria. En este artículo, nos sumergiremos en los tanques de combustible de la alta competición para desvelar la ciencia que se esconde detrás del líquido que lo es todo.

¿Qué es el octanaje y por qué es la clave de todo?
Para entender el combustible de competición, primero debemos comprender un concepto fundamental: el octanaje. Contrario a la creencia popular, un mayor octanaje no significa que la gasolina tenga "más potencia" por sí misma. En realidad, el índice de octano mide la capacidad de un combustible para resistir la compresión antes de detonar. ¿Y qué es la detonación? Es el enemigo número uno de un motor de alto rendimiento.
En un motor, la mezcla de aire y combustible es comprimida por el pistón hasta un punto crítico, y justo en ese momento, la bujía genera una chispa que inicia una combustión controlada, empujando el pistón hacia abajo. La detonación, también conocida como "picado de bielas" o "knocking", ocurre cuando la mezcla se autoenciende por la presión y el calor antes de que salte la chispa, o cuando se producen frentes de llama descontrolados. Este fenómeno genera ondas de choque brutales dentro del cilindro que pueden destruir pistones, bielas y válvulas en cuestión de segundos.
Los motores de competición trabajan con relaciones de compresión altísimas, temperaturas extremas y regímenes de giro infernales para extraer cada caballo de fuerza posible. Estas condiciones son el caldo de cultivo perfecto para la detonación. Por ello, necesitan combustibles con un índice de octano muy elevado (a menudo por encima de 100 o incluso 110 RON), que aguanten esa compresión extrema sin autoencenderse, permitiendo a los ingenieros programar el encendido en el punto exacto para una máxima eficiencia y potencia.
La estructura molecular importa: El rol de los isómeros como el 2,3-Dimetilpentano
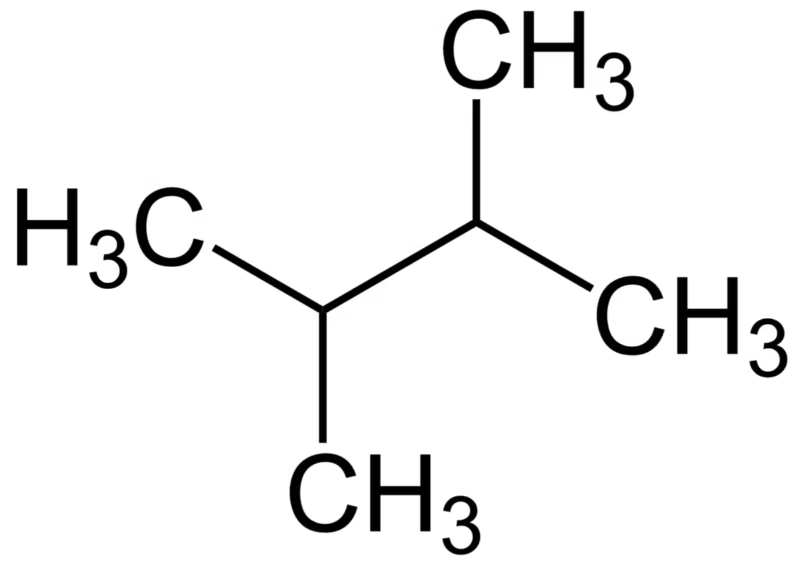
Aquí es donde entra en juego la química orgánica. No todos los hidrocarburos son iguales. La fórmula molecular nos dice cuántos átomos hay, pero la estructura, cómo están organizados, lo cambia todo. Tomemos como ejemplo el compuesto que mencionas, el 2,3-Dimetilpentano. Su fórmula es C7H16. El heptano normal (n-heptano), que también tiene la fórmula C7H16, es una cadena lineal de siete carbonos. El n-heptano es terrible en términos de antidetonación; de hecho, es el punto de referencia '0' en la escala de octanaje.
Sin embargo, el 2,3-Dimetilpentano es un isómero del heptano. Tiene los mismos átomos, pero su estructura es una cadena principal de cinco carbonos (pentano) con dos ramificaciones (grupos metilo) en los carbonos 2 y 3. Esta estructura ramificada es mucho más estable y resistente a la compresión. Las moléculas ramificadas tienden a formar radicales libres más estables durante la pre-combustión, ralentizando las reacciones en cadena que llevan a la detonación. Por lo tanto, el 2,3-Dimetilpentano tiene un índice de octano significativamente más alto que el n-heptano.
Los químicos que diseñan combustibles de competición son maestros en la selección de estos isómeros. Buscan moléculas altamente ramificadas como los diversos isooctanos y otros alcanos ramificados para construir una base de combustible que sea inherentemente resistente a la detonación. Lo mismo ocurre con alquenos (hidrocarburos con dobles enlaces) como el 2,3-dimetil-2-buteno, cuyas estructuras también pueden contribuir a elevar el octanaje y a modificar las propiedades de la combustión.
Más allá de la base: El cóctel de aditivos de competición
Un combustible de F1, IndyCar o WRC es mucho más que una simple mezcla de hidrocarburos de alto octanaje. Es una fórmula compleja que puede contener cientos de componentes, cada uno con una función específica:
- Oxigenantes: Compuestos como el etanol (usado en IndyCar y NASCAR), el metanol o el MTBE contienen átomos de oxígeno en su molécula. Esto ayuda a que la combustión sea más completa y eficiente, lo que puede traducirse en un ligero aumento de potencia. Sin embargo, su uso está estrictamente regulado por cada categoría.
- Detergentes: Aditivos de alta tecnología que mantienen limpios los inyectores, las válvulas y la cámara de combustión. En un motor que gira a 15,000 RPM, cualquier mínimo depósito de carbonilla puede afectar el flujo de la mezcla y robar preciosas milésimas de segundo.
- Modificadores de fricción: Ayudan a reducir la fricción interna entre piezas como los anillos del pistón y las paredes del cilindro, liberando algo más de potencia.
- Antioxidantes y estabilizadores: El combustible de competición puede ser inestable. Estos aditivos previenen su degradación con el tiempo o bajo condiciones de alta temperatura.
La mezcla final es un secreto guardado bajo llave por cada equipo y su proveedor de combustible (como Shell para Ferrari, Petronas para Mercedes o ExxonMobil para Red Bull Racing). Un pequeño cambio en la proporción de un componente puede requerir un ajuste completo en el mapeo del motor para extraer su máximo potencial.
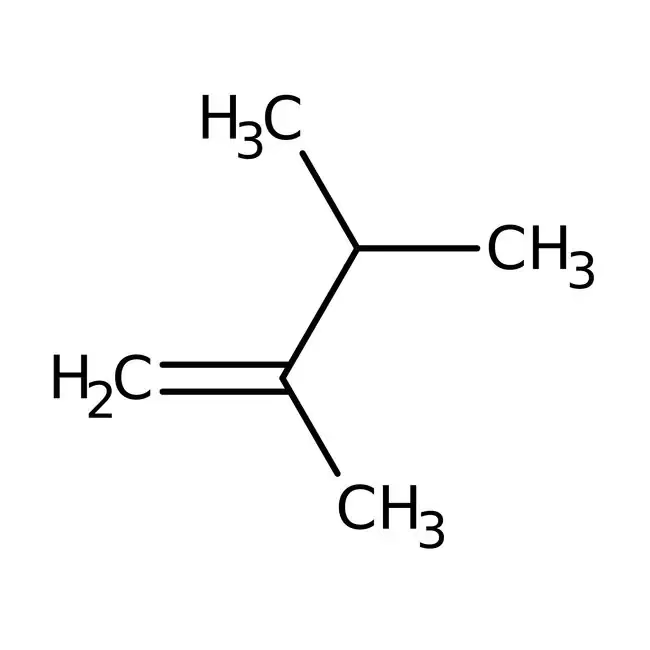
Tabla Comparativa: Combustible de Calle vs. Combustible de Competición
| Característica | Combustible de Calle (Premium) | Combustible de Competición (Ej. F1) |
|---|---|---|
| Octanaje (RON) | 95 - 98 | ~102 (limitado por regulación) |
| Composición Principal | Mezcla amplia de hidrocarburos | Mezcla precisa de isómeros y compuestos sintéticos |
| Contenido de Oxígeno | Regulado, a menudo con etanol (hasta 10%) | Estrictamente limitado por la FIA (Ej: 3.7% por masa) |
| Regulación | Normas gubernamentales (Euro, EPA) | Reglamento técnico de la FIA o del campeonato específico |
| Velocidad de Llama | Estándar | Optimizada para altas RPM |
| Costo | Moderado | Extremadamente alto (decenas de euros por litro) |
El Futuro: Combustibles Sostenibles y E-Fuels
El mundo del motorsport está en plena transición energética. La Fórmula 1, por ejemplo, ya utiliza combustible E10 (10% de etanol sostenible) y tiene el ambicioso objetivo de pasar a usar combustibles sintéticos 100% sostenibles para 2026. Estos e-fuels se fabrican capturando dióxido de carbono (CO2) de la atmósfera y combinándolo con hidrógeno verde (producido a partir de electrólisis del agua con energías renovables). El resultado es un hidrocarburo químicamente idéntico a la gasolina convencional, pero con una huella de carbono neta cercana a cero.
Esta transición no solo busca hacer el deporte más ecológico, sino que también lo posiciona como un laboratorio de pruebas para tecnologías que podrían, en el futuro, alimentar nuestros coches de calle sin depender de los combustibles fósiles. Categorías como el WRC ya están utilizando combustibles sostenibles, demostrando que el rendimiento y la responsabilidad medioambiental pueden ir de la mano.
Preguntas Frecuentes (FAQ)
¿Podría un coche de calle usar combustible de Fórmula 1?
Técnicamente podría funcionar, pero sería una muy mala idea. El combustible de F1 está diseñado para condiciones de operación extremas que un motor de calle nunca alcanza. Su alta resistencia a la detonación y su rápida velocidad de combustión no serían aprovechadas y, peor aún, sus aditivos agresivos podrían dañar los componentes del sistema de combustible y el motor de un vehículo convencional a largo plazo. Además de ser ilegal para uso en la vía pública, su costo es prohibitivo.
¿Por qué los equipos de F1 analizan el combustible de sus rivales?
La FIA (Federación Internacional del Automóvil) permite a los equipos tomar muestras de combustible de otros coches después de una carrera o clasificación. Lo hacen para asegurarse de que todos cumplen con el estricto reglamento. Cualquier desviación en la composición química, por mínima que sea, puede ser motivo de una descalificación inmediata, ya que podría indicar un intento de obtener una ventaja ilegal.
¿El combustible cambia según el circuito?
Sí. Los equipos y sus socios petroleros pueden desarrollar diferentes formulaciones de combustible para adaptarse a las características de cada circuito. Por ejemplo, en un circuito a gran altitud como el de México, donde el aire es menos denso, se podría usar una mezcla que optimice la combustión en condiciones de poco oxígeno. En circuitos de alta velocidad como Monza, se buscaría una fórmula que maximice la potencia pura.
En conclusión, el líquido que llena los tanques de los coches de carreras es mucho más que simple combustible. Es una obra de ingeniería química, un arma estratégica y un componente tan vital como el motor o la aerodinámica. La próxima vez que veas una carrera, recuerda que en cada aceleración, en cada adelantamiento, hay una batalla invisible que se libra a nivel molecular, donde compuestos como el 2,3-dimetilpentano son los héroes anónimos que hacen posible el espectáculo.
Si quieres conocer otros artículos parecidos a La Química de la Victoria: El Combustible puedes visitar la categoría Automovilismo.

