08/12/2019
En el vertiginoso universo del automovilismo, nuestra atención se centra casi siempre en la aerodinámica, la potencia del motor, las estrategias de neumáticos y la destreza de los pilotos. Hablamos de milisegundos, de puntos de frenada y del diseño de un alerón. Sin embargo, detrás de cada coche de Fórmula 1, de cada bestia del Dakar o de cada stock car de NASCAR, existe un mundo invisible pero fundamental: el de la ciencia de materiales. Y en el corazón de muchos de estos materiales de alto rendimiento se encuentran unos compuestos químicos llamados óxidos. Hoy, nos bajamos del coche y entramos al laboratorio para entender qué son, cómo se formulan y por qué son cruciales para alcanzar la gloria en la pista.

¿Qué Son los Óxidos y Por Qué Nos Importan en las Carreras?
En términos simples, un óxido es el resultado de la combinación química de un elemento, ya sea metálico o no metálico, con el oxígeno. Esta reacción, llamada oxidación, es una de las más comunes en la naturaleza. Cuando pensamos en óxido, a menudo nos viene a la mente la herrumbre en un trozo de metal viejo, pero su universo es infinitamente más amplio y sofisticado. Dependiendo del elemento que se combine con el oxígeno, el óxido resultante puede ser básico (si es un metal) o ácido (si es un no metal).
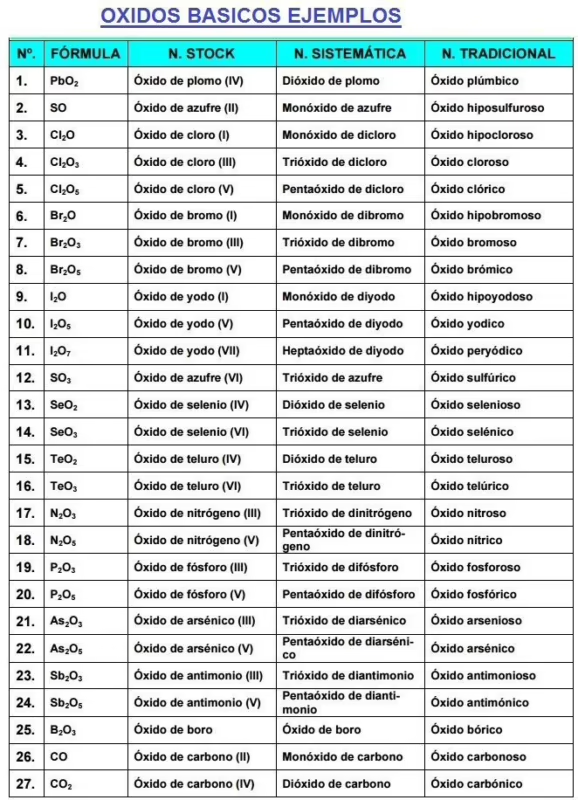
Esta distinción es clave, ya que determina sus propiedades y, por tanto, sus aplicaciones. En el motorsport, estas aplicaciones son vitales:
- Cerámicas avanzadas: Materiales como el óxido de aluminio (Al₂O₃) o el dióxido de titanio (TiO₂) son la base de componentes que necesitan resistir temperaturas y desgastes extremos, como los aislantes de las bujías o partes de los sistemas de frenos carbono-cerámicos.
- Pigmentos para pinturas: La icónica pintura roja de un Ferrari o el vibrante azul de un Alpine deben su color y durabilidad a óxidos metálicos que actúan como pigmentos. El dióxido de titanio, por ejemplo, es la base de casi todas las pinturas blancas.
- Componentes electrónicos: Los complejos sistemas electrónicos y sensores que monitorizan cada aspecto de un monoplaza moderno utilizan óxidos semiconductores para funcionar.
- Tratamiento de metales: Muchos chasis y componentes de motor están hechos de aleaciones metálicas que se tratan para crear una capa de óxido superficial (pasivación) que los protege de la corrosión sin añadir peso significativo.
La Fórmula de la Victoria: Entendiendo los Óxidos Básicos
Los óxidos básicos, también conocidos como óxidos metálicos, son aquellos que unen el oxígeno con un elemento metálico. La fórmula general que los representa es XO, donde 'X' es el símbolo del elemento metálico y 'O' es el del oxígeno. A menudo, estos símbolos van acompañados de subíndices numéricos (como en Fe₂O₃) que indican cuántos átomos de cada elemento hay en la molécula. Estos subíndices surgen del intercambio de las "valencias" o estados de oxidación de los elementos. El oxígeno, en los óxidos, casi siempre actúa con una valencia de -2, mientras que los metales pueden tener una o varias valencias positivas. Este enlace, entre un metal electropositivo y el oxígeno electronegativo, es de tipo iónico, lo que generalmente les confiere una gran dureza y altos puntos de fusión, propiedades muy deseadas en competición.
El Lenguaje de los Boxes: La Nomenclatura de los Óxidos
Para poder hablar de estos compuestos, los ingenieros y químicos utilizan sistemas de nomenclatura estandarizados. Conocerlos nos permite entender exactamente de qué material están hablando cuando se refieren, por ejemplo, al componente de un escape. Existen tres sistemas principales.
1. Nomenclatura Tradicional
Es el sistema más antiguo y se basa en el uso de prefijos y sufijos que dependen del número de valencias que tenga el metal.
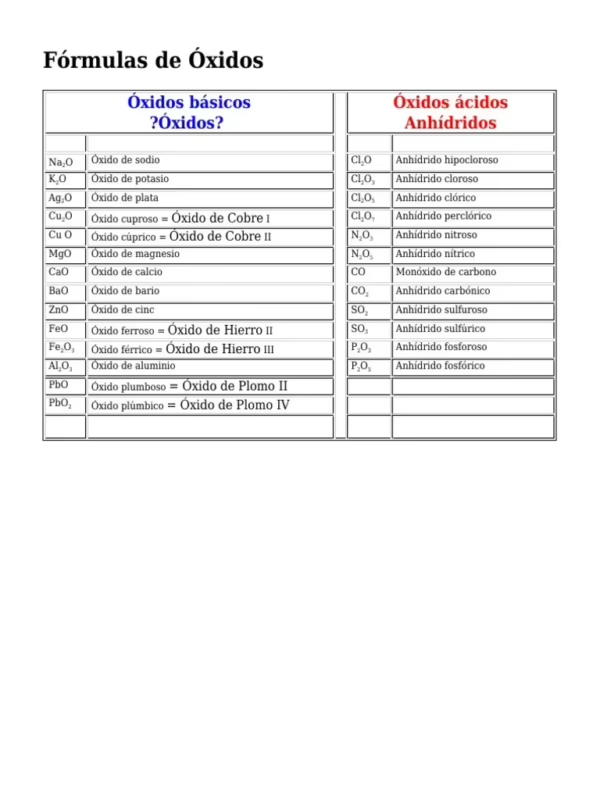
- Una valencia: Se usa la terminación "-ico". Ejemplo: Óxido sódico (Na₂O).
- Dos valencias: Se usa "-oso" para la menor y "-ico" para la mayor. Ejemplo: Óxido ferroso (FeO, con hierro valencia 2+) y óxido férrico (Fe₂O₃, con hierro valencia 3+).
- Tres valencias: Se usa "hipo-...-oso" (menor), "-oso" (intermedia) y "-ico" (mayor). Ejemplo: Óxido hipocromoso (CrO), óxido cromoso (Cr₂O₃) y óxido crómico (CrO₃).
- Cuatro valencias: Se añade el prefijo "per-" a la valencia más alta. Ejemplo: Óxido hipomanganoso (MnO), óxido manganoso (Mn₂O₃), óxido mangánico (MnO₂) y óxido permangánico (Mn₂O₇).
2. Nomenclatura de Stock
Este sistema es más directo y menos propenso a la ambigüedad. Se nombra el compuesto como "óxido de [nombre del metal]" y se indica la valencia del metal con números romanos entre paréntesis. Si el metal solo tiene una valencia, no es necesario indicarla. Es un sistema muy utilizado en la comunicación técnica por su claridad.
- Ejemplo 1: NiO es el óxido de níquel (II).
- Ejemplo 2: Ni₂O₃ es el óxido de níquel (III).
- Ejemplo 3: MgO es simplemente óxido de magnesio, ya que el magnesio solo tiene valencia 2+.
3. Nomenclatura Sistemática (IUPAC)
Es la nomenclatura recomendada actualmente por la Unión Internacional de Química Pura y Aplicada (IUPAC). Utiliza prefijos griegos (mono-, di-, tri-, tetra-, penta-, etc.) para indicar el número de átomos de cada elemento en la molécula. Es el sistema más preciso y descriptivo.
- Ejemplo 1: Fe₂O₃ se nombra como trióxido de dihierro.
- Ejemplo 2: Na₂O se nombra como monóxido de disodio.
- Ejemplo 3: CrO₃ se nombra como trióxido de cromo.
Tabla Comparativa de Nomenclaturas
| Fórmula | Nomenclatura Tradicional | Nomenclatura de Stock | Nomenclatura Sistemática |
|---|---|---|---|
| Fe₂O₃ | Óxido férrico | Óxido de hierro (III) | Trióxido de dihierro |
| CuO | Óxido cúprico | Óxido de cobre (II) | Monóxido de cobre |
| Al₂O₃ | Óxido alumínico | Óxido de aluminio | Trióxido de dialuminio |
| SnO₂ | Óxido estánnico | Óxido de estaño (IV) | Dióxido de estaño |
Un Caso Especial: El Trióxido de Difósforo (P₂O₃)
No todos los óxidos importantes involucran metales. El fósforo es un no metal, y su combinación con el oxígeno da lugar a óxidos ácidos. Un ejemplo es el trióxido de difósforo (P₂O₃), también conocido como anhídrido fosforoso. Aunque su fórmula más simple es P₂O₃, en la naturaleza se presenta de una forma más compleja, como P₄O₆ (hexaóxido de tetrafósforo). Su estructura es un tetraedro de átomos de fósforo, con los átomos de oxígeno uniendo sus aristas. Este tipo de compuestos son fundamentales en la industria química para la creación de otros productos, y aunque su aplicación directa en un coche de carreras no sea tan evidente como la del óxido de aluminio, ejemplifica la increíble diversidad estructural y química que el oxígeno puede generar, abriendo la puerta a la investigación de nuevos materiales con propiedades inesperadas.
Preguntas Frecuentes (FAQ)
¿Por qué es importante la química en un deporte de motor?
La química es fundamental. Define las propiedades de los combustibles, los lubricantes, los compuestos de los neumáticos, los materiales del chasis y del motor, las pinturas y los fluidos hidráulicos. Sin un profundo conocimiento de la química, sería imposible alcanzar los niveles de rendimiento y seguridad que vemos hoy en día.

¿El óxido común (herrumbre) es el mismo tipo de compuesto que se usa en alta tecnología?
Químicamente, sí. La herrumbre es principalmente óxido de hierro (III) hidratado (Fe₂O₃·nH₂O). Es el mismo óxido que, en forma pura y controlada, se usa como pigmento rojo. La diferencia radica en el proceso de formación: la herrumbre es una corrosión descontrolada, mientras que en aplicaciones tecnológicas, el óxido se crea y procesa de forma deliberada para obtener propiedades específicas de dureza, color o reactividad.
¿Qué nomenclatura se usa más en los laboratorios de los equipos de competición?
En entornos técnicos y de investigación, como los que rodean a equipos como Ferrari o Red Bull Racing, se prefiere la nomenclatura de Stock y la Sistemática (IUPAC) por su precisión y falta de ambigüedad. La tradicional se sigue usando por costumbre en algunos contextos, pero para la comunicación científica rigurosa, la IUPAC es el estándar de oro.
La próxima vez que veas un monoplaza trazando una curva a más de 300 km/h o un coche de rally levantando polvo en un tramo de montaña, recuerda que parte de esa increíble hazaña de ingeniería es posible gracias a la química. Los óxidos, esos compuestos aparentemente simples de un elemento y oxígeno, son los héroes anónimos que proporcionan la resistencia, el color y la funcionalidad que definen a las máquinas de carreras más avanzadas del planeta.
Si quieres conocer otros artículos parecidos a Óxidos: La Química Oculta del Automovilismo puedes visitar la categoría Automovilismo.
