12/11/2020
En el mundo del automovilismo, cada detalle cuenta. Desde la aerodinámica más refinada hasta la estrategia de neumáticos, cada variable es optimizada en busca de la milésima de segundo que separa la gloria del segundo lugar. Sin embargo, hay un componente fundamental, a menudo subestimado por el aficionado, que es el verdadero corazón de la potencia: el combustible. No hablamos de la gasolina que se encuentra en cualquier estación de servicio, sino de un cóctel químico diseñado con precisión molecular para liberar la máxima energía. Para entender su importancia, debemos sumergirnos en el fascinante mundo de la química orgánica y conocer a los héroes anónimos de la combustión, moléculas como el buteno y el butino, cuyos secretos estructurales definen el rendimiento de un motor de competición.

Los Hidrocarburos: El ADN de la Potencia
El combustible de carreras es, en esencia, una mezcla compleja de hidrocarburos, compuestos formados por átomos de hidrógeno y carbono. La forma en que estos átomos se enlazan y estructuran determina las propiedades del combustible: su densidad energética, su volatilidad y, crucialmente, su resistencia a la detonación (conocida como octanaje). Los ingenieros químicos y los equipos de F1, IndyCar o WRC no eligen simplemente un combustible; lo diseñan. Manipulan estas estructuras moleculares para crear una fórmula que se adapte perfectamente a las exigencias de su motor. Dos familias de moléculas que ilustran perfectamente este principio son los alquenos, como el buteno, y los alquinos, como el butino.

El Buteno (C₄H₈): Un Pilar Versátil de la Energía
El buteno es un alqueno con la fórmula molecular C₄H₈. Su característica principal es la presencia de un doble enlace carbono-carbono, que lo hace más reactivo que los alcanos (con enlaces simples) y una excelente fuente de energía. Lo realmente interesante del buteno es que no es una única molécula, sino que existe en forma de cuatro isómeros: compuestos con la misma fórmula molecular pero con diferentes estructuras. Esta diferencia estructural, aunque sutil, tiene un impacto gigantesco en sus propiedades fisicoquímicas y, por ende, en su comportamiento como componente de un combustible.
Los Cuatro Rostros del Buteno
Los cuatro isómeros del buteno son gases incoloros e inflamables, pero sus diferencias estructurales los hacen únicos:
- 1-Buteno: Una cadena lineal de cuatro carbonos con el doble enlace en el primer carbono.
- cis-2-Buteno: El doble enlace está en el centro, y los grupos metilo a cada lado apuntan en la misma dirección.
- trans-2-Buteno: Similar al cis-2-buteno, pero los grupos metilo apuntan en direcciones opuestas, lo que le confiere mayor estabilidad.
- Isobuteno (2-metilpropeno): Presenta una estructura ramificada, una característica muy deseada en los combustibles de alto rendimiento por su elevado octanaje.
Para un ingeniero de combustibles, controlar la proporción de estos isómeros es clave. Por ejemplo, las estructuras ramificadas como la del isobuteno son más resistentes a la autoignición o "picado" del motor, permitiendo mayores relaciones de compresión y, en consecuencia, más potencia.
Tabla Comparativa de Isómeros del Buteno
| Isómero | Fórmula Estructural | Punto de Ebullición | Relevancia en Competición |
|---|---|---|---|
| 1-Buteno | CH₂=CH–CH₂–CH₃ | -6,3 °C | Componente base para síntesis de otros aditivos. |
| cis-2-Buteno | CH₃–CH=CH–CH₃ (cis) | 3,7 °C | Menos estable que su contraparte trans. |
| trans-2-Buteno | CH₃–CH=CH–CH₃ (trans) | 0,9 °C | Más estable debido a menor impedimento estérico. |
| Isobuteno | H₂C=C(CH₃)₂ | -6,9 °C | Muy valorado por su estructura ramificada que eleva el octanaje. |
El Butino (C₄H₆): Energía Concentrada en el Triple Enlace
Si el doble enlace del buteno ya es una fuente de energía, el triple enlace del butino, un alquino con fórmula C₄H₆, es aún más potente. Este triple enlace almacena una gran cantidad de energía que puede ser liberada durante la combustión. Al igual que el buteno, el butino también tiene isómeros, cuya diferencia principal radica en la posición de este triple enlace.
1-Butino vs. 2-Butino: Una Diferencia Crucial
La posición del triple enlace no es un detalle menor. Define si el alquino es "terminal" o "interno", lo que altera drásticamente su reactividad química.
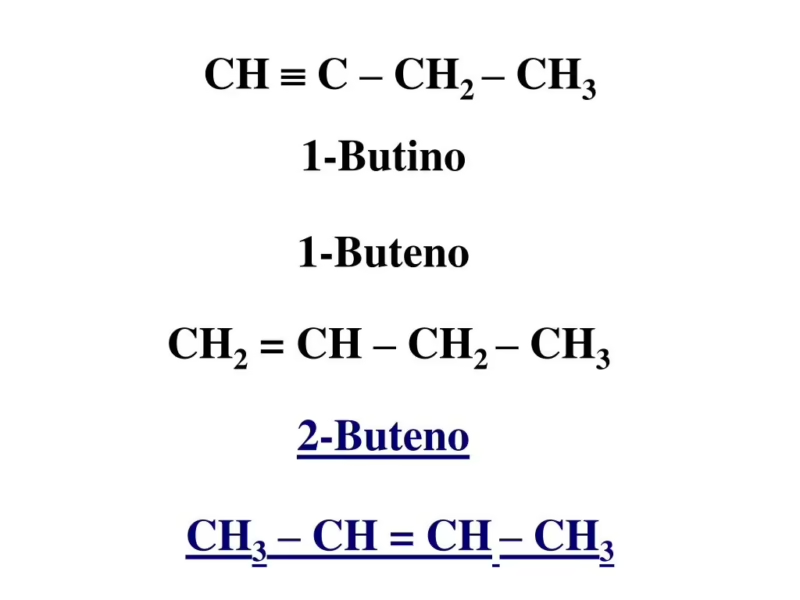
- 1-Butino: Es un alquino terminal, con el triple enlace al final de la cadena. El átomo de carbono en la posición 1 está unido a un átomo de hidrógeno. Este hidrógeno es débilmente ácido, lo que hace que la molécula sea significativamente más reactiva.
- 2-Butino: Es un alquino interno. El triple enlace se encuentra en el medio de la cadena, y los carbonos involucrados no están unidos a hidrógenos, sino a otros grupos de carbono. Esto lo convierte en una molécula mucho más estable que el 1-butino.
En el desarrollo de combustibles, esta diferencia es vital. Una molécula más reactiva como el 1-butino podría ofrecer una liberación de energía más rápida, pero su inestabilidad podría ser perjudicial para el motor. La estabilidad del 2-butino podría ser preferible para una combustión más controlada y predecible. Los químicos pueden incluso diferenciar ambos isómeros en un laboratorio usando el reactivo de Tollen, que reacciona con el hidrógeno ácido del 1-butino para formar un precipitado blanco, mientras que no reacciona con el 2-butino. Este tipo de control de calidad es esencial en la producción de combustibles de élite.
El Arte de la Isomerización: Transformando Moléculas para la Victoria
La genialidad de la química de combustibles no reside solo en seleccionar las moléculas correctas, sino en la capacidad de transformarlas. Un proceso clave es la isomerización, que permite convertir un isómero en otro. Por ejemplo, es posible convertir el más reactivo 1-butino en el más estable 2-butino.
Este proceso se puede lograr calentando el 1-butino en presencia de una base fuerte como el hidróxido de potasio (KOH) en etanol. La base provoca un reordenamiento de los enlaces dentro de la molécula, desplazando el triple enlace desde el extremo hacia el centro de la cadena. Este control a nivel molecular es lo que permite a los ingenieros crear un combustible con las propiedades exactas de estabilidad, energía y combustión que requiere un motor que gira a más de 15,000 RPM. Es, literalmente, construir la victoria átomo por átomo.
Preguntas Frecuentes (FAQ)
¿El combustible de Fórmula 1 es solo gasolina de alto octanaje?
No. Es una mezcla altamente regulada por la FIA, pero dentro de esas regulaciones, los equipos y sus socios petroleros diseñan formulaciones únicas. Son mezclas de cientos de compuestos, donde cada componente está optimizado para la máxima potencia y eficiencia, y se asemeja muy poco a la gasolina comercial.
¿Por qué la estructura de una molécula afecta el octanaje?
El octanaje mide la resistencia de un combustible a detonar prematuramente bajo compresión. Las moléculas con estructuras ramificadas, como el isobuteno o el isooctano, son más estables y compactas, lo que les permite soportar mayores presiones antes de encenderse. Las cadenas lineales son más propensas a la detonación, lo que resulta en un menor octanaje.
¿Se usan butinos y butenos puros en los coches de carreras?
Generalmente no se usan en su forma pura, pero son representativos de los tipos de hidrocarburos y estructuras (dobles enlaces, triples enlaces, ramificaciones) que los químicos buscan y crean para formular los componentes del combustible final. Sirven como bloques de construcción para moléculas más complejas.
¿Cómo influye esta química en la estrategia de carrera?
Un combustible más eficiente energéticamente significa que se necesita menos cantidad para completar una carrera, lo que se traduce en un coche más ligero y paradas en boxes potencialmente más cortas. Un combustible que permite una mayor potencia puede dar una ventaja crucial en las rectas. La formulación del combustible es, por tanto, un factor estratégico clave.
La próxima vez que escuches el rugido de un motor de competición, recuerda que no es solo mecánica y pilotaje. Es también el resultado de una compleja sinfonía química, donde moléculas invisibles como el buteno y el butino son las verdaderas protagonistas, desatando su energía en una danza precisa para impulsar a los campeones hacia la línea de meta.
Si quieres conocer otros artículos parecidos a Combustible: La Química Secreta de la Victoria puedes visitar la categoría Automovilismo.

