17/11/2021
Los compuestos orgánicos más simples de la naturaleza contienen exclusivamente elementos de carbono e hidrógeno; a estos se les denomina hidrocarburos. Aunque su composición parece básica, la diversidad de hidrocarburos es asombrosa. Esto se debe a la increíble capacidad de los átomos de carbono para formar hasta cuatro enlaces fuertes con otros átomos de carbono, creando cadenas y anillos de tamaños, formas y complejidades casi infinitas. Desde el gas natural que calienta nuestros hogares hasta los plásticos que usamos a diario y los combustibles que mueven nuestros vehículos, los hidrocarburos son pilares fundamentales de nuestra vida moderna y de la química orgánica. En este artículo, exploraremos en profundidad su clasificación, propiedades, reacciones características y las innumerables aplicaciones que los convierten en moléculas indispensables.
Clasificación de los Hidrocarburos: Saturados e Insaturados
La principal forma de clasificar los hidrocarburos se basa en el tipo de enlace que une a sus átomos de carbono. Esta diferencia en el enlace no solo cambia su estructura y geometría molecular, sino también su reactividad y sus propiedades físicas. Se dividen en dos grandes grupos: saturados e insaturados.
1. Alcanos: Los Hidrocarburos Saturados
Los alcanos son considerados hidrocarburos saturados porque contienen únicamente enlaces covalentes simples (enlaces sigma, σ) entre sus átomos de carbono. En un alcano, cada átomo de carbono tiene una hibridación sp³ y está enlazado a otros cuatro átomos (ya sea carbono o hidrógeno), adoptando una geometría tetraédrica con ángulos de enlace cercanos a 109,5°. Esta disposición da a las cadenas de alcanos una característica forma de zigzag.
La fórmula general para los alcanos acíclicos (de cadena abierta) es CnH2n+2. El miembro más simple de esta familia es el metano (CH₄), el componente principal del gas natural.
Propiedades Físicas de los Alcanos
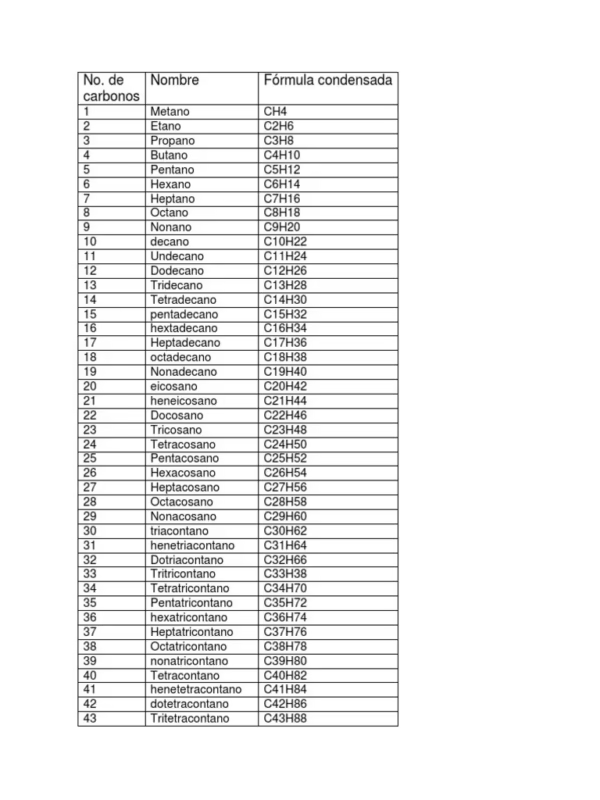
Las propiedades de los alcanos, como sus puntos de fusión y ebullición, varían de manera predecible a medida que aumenta el número de átomos de carbono en la molécula. A mayor longitud de la cadena, mayores son las fuerzas de dispersión intermoleculares, lo que resulta en puntos de ebullición y fusión más altos.

| Alcano | Fórmula Molecular | Punto de Fusión (°C) | Punto de Ebullición (°C) | Fase en STP |
|---|---|---|---|---|
| Metano | CH₄ | -182,5 | -161,5 | Gas |
| Etano | C₂H₆ | -183,3 | -88,6 | Gas |
| Propano | C₃H₈ | -187,7 | -42,1 | Gas |
| Butano | C₄H₁₀ | -138,3 | -0,5 | Gas |
| Pentano | C₅H₁₂ | -129,7 | 36,1 | Líquido |
| Hexano | C₆H₁₄ | -95,3 | 68,7 | Líquido |
| Octano | C₈H₁₈ | -56,8 | 125,7 | Líquido |
| Decano | C₁₀H₂₂ | -29,7 | 174,0 | Líquido |
| Octadecano | C₁₈H₃₈ | 28,2 | 316,1 | Sólido |
Isómeros Estructurales en Alcanos
Los hidrocarburos con la misma fórmula molecular pero diferente disposición de átomos se conocen como isómeros estructurales. Por ejemplo, la fórmula C₄H₁₀ corresponde a dos compuestos diferentes: el n-butano (una cadena lineal) y el 2-metilpropano o isobutano (una cadena ramificada). A medida que aumenta el número de carbonos, la cantidad de posibles isómeros crece exponencialmente.
Reacciones de los Alcanos
Los alcanos son relativamente poco reactivos debido a la fortaleza de sus enlaces C-C y C-H. Sin embargo, participan en dos tipos principales de reacciones:
- Combustión: En presencia de oxígeno, los alcanos arden en una reacción altamente exotérmica que produce dióxido de carbono y agua. Esta es la base de su uso como combustibles. Ejemplo: CH₄(g) + 2O₂(g) → CO₂(g) + 2H₂O(g).
- Sustitución (Halogenación): Bajo la influencia de calor o luz UV, uno o más átomos de hidrógeno de un alcano pueden ser reemplazados por un átomo de halógeno (como cloro o bromo).
2. Alquenos: Dobles Enlaces y Reactividad
Los alquenos son hidrocarburos insaturados que contienen al menos un doble enlace carbono-carbono (C=C). Este doble enlace consta de un enlace sigma (σ) fuerte y un enlace pi (π) más débil y reactivo. Los átomos de carbono involucrados en el doble enlace tienen hibridación sp² y una geometría planar trigonal, con ángulos de enlace de aproximadamente 120°.
El alqueno más simple es el eteno (C₂H₄), comúnmente conocido como etileno. La nomenclatura de los alquenos sigue las reglas de la IUPAC, pero el sufijo -ano se cambia por -eno para indicar la presencia del doble enlace.
Isomería Geométrica (Cis-Trans) en Alquenos
La rigidez del doble enlace C=C impide la libre rotación, lo que da lugar a un tipo especial de isomería llamada isomería geométrica. Por ejemplo, el 2-buteno existe en dos formas: el isómero cis, donde los grupos metilo están en el mismo lado del doble enlace, y el isómero trans, donde están en lados opuestos. Estos isómeros tienen propiedades físicas distintas.
Reacciones de los Alquenos
La presencia del enlace π hace que los alquenos sean mucho más reactivos que los alcanos. Su reacción característica es la reacción de adición, donde el enlace π se rompe y se forman dos nuevos enlaces sigma. Por ejemplo, los halógenos se adicionan fácilmente al doble enlace:
CH₂=CH₂ + Br₂ → CH₂Br-CH₂Br
3. Alquinos: La Linealidad del Triple Enlace
Los alquinos son hidrocarburos insaturados que contienen al menos un triple enlace carbono-carbono (C≡C). Este triple enlace está formado por un enlace sigma y dos enlaces pi. Los carbonos involucrados tienen hibridación sp y una geometría lineal, con un ángulo de enlace de 180°, lo que les da una forma de varilla.

El alquino más simple es el etino (C₂H₂), universalmente conocido como acetileno. La nomenclatura utiliza el sufijo -ino para denotar el triple enlace.
Reacciones de los Alquinos
Químicamente, los alquinos son similares a los alquenos pero aún más reactivos debido a la presencia de dos enlaces π. Pueden someterse a reacciones de adición, reaccionando con el doble de reactivo que un alqueno. El acetileno, por ejemplo, arde con una llama muy caliente, lo que lo hace ideal para sopletes de soldadura.
Tabla Comparativa de Hidrocarburos
| Característica | Alcanos | Alquenos | Alquinos |
|---|---|---|---|
| Tipo de Enlace C-C | Simple (C-C) | Doble (C=C) | Triple (C≡C) |
| Clasificación | Saturado | Insaturado | Insaturado |
| Hibridación del Carbono | sp³ | sp² | sp |
| Geometría | Tetraédrica (109,5°) | Planar Trigonal (120°) | Lineal (180°) |
| Sufijo IUPAC | -ano | -eno | -ino |
| Reacción Característica | Sustitución | Adición | Adición |
Aplicaciones de los Hidrocarburos en la Vida Cotidiana
Los hidrocarburos son mucho más que simples compuestos químicos; son la materia prima de innumerables productos y la fuente de energía que impulsa nuestra civilización.
- Combustibles: Es su uso más conocido. Los primeros cuatro alcanos (metano, etano, propano, butano) son gases usados para calefacción y cocina. Desde el pentano hasta el octano, son líquidos volátiles que componen la gasolina. Hidrocarburos más pesados forman el diésel, el queroseno y los aceites lubricantes.
- Plásticos y Polímeros: El etileno es la materia prima para producir polietileno, uno de los plásticos más comunes del mundo, utilizado en bolsas, envases y películas. Otros hidrocarburos dan lugar al polipropileno, PVC y poliestireno, materiales omnipresentes en nuestra vida.
- Material Sanitario: Muchos medicamentos, como la aspirina o el ibuprofeno, se sintetizan a partir de derivados del petróleo. Además, se utilizan para fabricar jeringuillas, prótesis, guantes desechables y otros equipos médicos.
- Ropa y Textiles: Fibras sintéticas como el nailon, el poliéster y la lycra, presentes en nuestra ropa deportiva, moda y mobiliario, son polímeros derivados de hidrocarburos.
- Cosmética: Productos de maquillaje, cremas, tintes para el cabello y perfumes a menudo contienen aceites minerales y otros compuestos derivados del petróleo.
- Otros Usos: También se encuentran en solventes para pinturas y tintas (como las de libros y periódicos), ceras de parafina para velas, y asfalto para pavimentar carreteras.
Riesgos Asociados a los Hidrocarburos
A pesar de su utilidad, los hidrocarburos no están exentos de riesgos. El metano es un potente gas de efecto invernadero y puede formar mezclas explosivas con el aire. Los alcanos líquidos más ligeros (gasolina, pentano, hexano) son altamente inflamables. Además, la exposición a ciertos hidrocarburos puede ser perjudicial para la salud; por ejemplo, el isómero lineal del hexano es conocido por ser una neurotoxina.
Preguntas Frecuentes (FAQ)
¿Qué son los hidrocarburos y por qué son importantes?
Los hidrocarburos son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno. Son fundamentales porque constituyen la principal fuente de energía del mundo (petróleo, gas natural) y son la materia prima para una vasta gama de productos químicos, incluyendo plásticos, medicamentos, fibras sintéticas y solventes.
¿Cuál es la diferencia entre un hidrocarburo saturado y uno insaturado?
La diferencia radica en los enlaces entre sus átomos de carbono. Un hidrocarburo saturado (alcano) solo tiene enlaces simples C-C, lo que significa que contiene el máximo número posible de átomos de hidrógeno. Un hidrocarburo insaturado (alqueno o alquino) contiene al menos un enlace doble o triple C-C, lo que reduce el número de hidrógenos y crea un sitio reactivo en la molécula.
¿Qué son los isómeros?
Los isómeros son moléculas que tienen la misma fórmula molecular pero diferentes estructuras. Los isómeros estructurales difieren en la forma en que los átomos están conectados (ej., n-butano vs. isobutano). Los isómeros geométricos (como cis-trans en alquenos) tienen la misma conectividad pero difieren en la orientación espacial de los átomos.
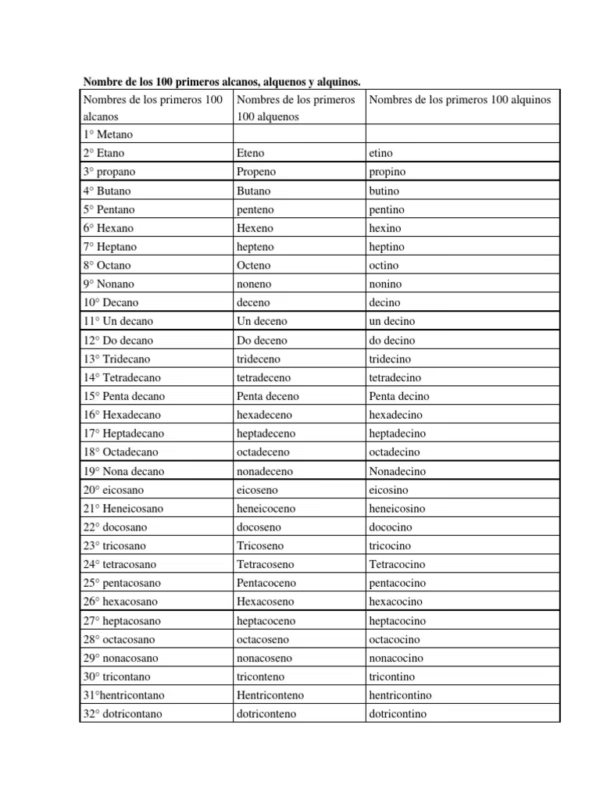
¿Cuáles son los nombres de los primeros diez alcanos de cadena lineal?
Los nombres, según el número de átomos de carbono, son: 1. Metano, 2. Etano, 3. Propano, 4. Butano, 5. Pentano, 6. Hexano, 7. Heptano, 8. Octano, 9. Nonano, 10. Decano.
Si quieres conocer otros artículos parecidos a Hidrocarburos: Guía Completa y Esencial puedes visitar la categoría Automovilismo.

