24/08/2023
En el vertiginoso mundo del automovilismo, donde cada milésima de segundo cuenta, a menudo centramos nuestra atención en la aerodinámica, la potencia del motor y la habilidad del piloto. Sin embargo, detrás de cada victoria, de cada pole position y de cada récord de vuelta, existe un universo invisible pero fundamental: el de la química. Conceptos que pueden parecer lejanos, como la masa molecular, la masa exacta o el número de Avogadro, son en realidad pilares sobre los que se construye el rendimiento de un monoplaza de Fórmula 1, un coche de Rally o un prototipo de resistencia. El peso del combustible, la composición de los neumáticos y la estructura de los materiales exóticos no son magia, son ciencia aplicada al más alto nivel.
https://www.youtube.com/watch?v=0gcJCdgAo7VqN5tD
Comprender cómo se calcula el peso de las moléculas que componen el combustible o los polímeros de las gomas nos permite apreciar la increíble precisión con la que trabajan los ingenieros. No se trata solo de llenar un tanque; se trata de calcular la cantidad exacta de energía, el peso que añadirá al coche y cómo afectará al balance y al desgaste a lo largo de una carrera. Bienvenidos a un viaje al corazón atómico del motorsport, donde la tabla periódica es tan importante como el reglamento técnico de la FIA.

La Masa Molecular: El Peso Secreto de la Velocidad
En su definición más simple, la masa molecular es la suma de las masas atómicas de todos los átomos presentes en una molécula. Se mide en unidades de masa atómica (uma). Para entenderlo, pensemos en el agua (H₂O). El hidrógeno tiene una masa atómica de aproximadamente 1 uma y el oxígeno de 16 uma. Como la molécula de agua tiene dos átomos de hidrógeno y uno de oxígeno, el cálculo es sencillo: (2 x 1 uma) + 16 uma = 18 uma. Este es el peso de una sola molécula de agua.
Ahora, traslademos este concepto al paddock. El combustible de un coche de carreras es una mezcla compleja de hidrocarburos. Tomemos como ejemplo simplificado el octano (C₈H₁₈), un componente clave de la gasolina de alto rendimiento. El carbono tiene una masa atómica de aproximadamente 12 uma y el hidrógeno de 1 uma.
- Masa de los 8 átomos de Carbono: 8 x 12 uma = 96 uma
- Masa de los 18 átomos de Hidrógeno: 18 x 1 uma = 18 uma
- Masa molecular del Octano (C₈H₁₈): 96 uma + 18 uma = 114 uma
¿Por qué es esto tan crucial? Porque la masa está directamente relacionada con el peso. En la Fórmula 1, los coches comienzan la carrera con un máximo de 110 kg de combustible. Los ingenieros saben con precisión la masa molecular de los compuestos de su combustible, lo que les permite calcular la densidad y, por tanto, el volumen exacto que necesitan. Pero más importante aún, les permite predecir cómo cambiará el peso del coche vuelta a vuelta. Un coche más ligero es un coche más rápido: acelera mejor, frena más tarde y es más ágil en las curvas. La gestión del peso del combustible, basada en estos cálculos moleculares, es una de las claves estratégicas de cualquier carrera.
Más Allá del Peso: La Masa Exacta y los Isótopos
Si profundizamos un poco más, nos encontramos con el concepto de "masa exacta" o masa monoisotópica. La masa atómica que usamos comúnmente (como 12 para el carbono) es en realidad un promedio ponderado de todos los isótopos naturales de ese elemento. Los isótopos son átomos de un mismo elemento que tienen un número diferente de neutrones en su núcleo, y por tanto, una masa ligeramente distinta.
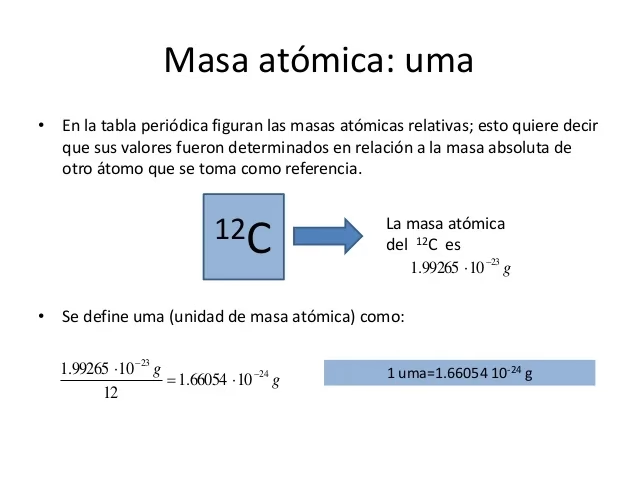
La masa exacta, sin embargo, se calcula utilizando la masa del isótopo más abundante de cada elemento. Por ejemplo, el isótopo más común del carbono es el Carbono-12, cuya masa es exactamente 12.0000 uma. Para el hidrógeno, es el Protio (¹H), con una masa de 1.0078 uma.
Veamos el ejemplo de la teobromina (C₇H₈N₄O₂), una molécula orgánica, para entender la diferencia:
- Masa Molecular (peso molecular promedio): 180.17 uma
- Masa Exacta (monoisotópica): 180.0646 uma
La diferencia puede parecer mínima, pero en el mundo del alto rendimiento y la regulación, es gigantesca. La Federación Internacional del Automóvil (FIA) utiliza técnicas de análisis increíblemente sofisticadas, como la cromatografía de gases acoplada a espectrometría de masas, para verificar que los combustibles y lubricantes cumplen con la estricta normativa. Estos dispositivos no miden el peso promedio; identifican las moléculas por su masa exacta. Esto permite a los comisarios técnicos detectar cualquier compuesto prohibido con una precisión asombrosa, garantizando que nadie obtenga una ventaja ilegal a nivel molecular.
El Mol y el Número de Avogadro: Contando Moléculas en el Paddock
Sabemos cómo pesar una molécula, pero ¿cómo contamos la inmensa cantidad de ellas que hay en un tanque de combustible? Aquí es donde entra en juego uno de los números más importantes de la química: el número de Avogadro, aproximadamente 6.022 x 10²³.
Este número define una unidad de cantidad llamada "mol". Un mol de cualquier sustancia contiene 6.022 x 10²³ partículas (átomos, moléculas, etc.). La genialidad de este concepto es que conecta el mundo microscópico de las 'uma' con el mundo macroscópico de los gramos que podemos pesar en una balanza. La masa de un mol de una sustancia, expresada en gramos, es numéricamente igual a su masa molecular en uma.
- Masa molecular del agua (H₂O) = 18 uma
- Masa de 1 mol de agua = 18 gramos
Para los ingenieros de motores, el mol es una herramienta indispensable. La combustión es una reacción química donde las moléculas de combustible reaccionan con las de oxígeno. La ecuación química de la combustión del octano, por ejemplo, les dice exactamente cuántos moles de oxígeno se necesitan para quemar completamente un mol de octano. Esto les permite calcular la relación estequiométrica aire/combustible perfecta para extraer la máxima energía del motor, optimizando la potencia y la eficiencia. Cada ajuste en la mezcla que se realiza desde el box se basa en estos principios fundamentales.

Tabla Comparativa de Conceptos Químicos en Motorsport
| Concepto | Definición | Aplicación en Motorsport |
|---|---|---|
| Masa Molecular | Suma de las masas atómicas promedio de los átomos de una molécula (en uma). | Calcular el peso del combustible para la estrategia de carrera y la gestión del balance del coche. |
| Masa Exacta | Suma de las masas de los isótopos más abundantes de los átomos de una molécula. | Utilizada en análisis de laboratorio (espectrometría de masas) por la FIA para verificar la legalidad de los combustibles y lubricantes. |
| Mol / Número de Avogadro | Unidad que representa 6.022 x 10²³ partículas. Conecta la masa molecular (uma) con la masa en gramos. | Calcular las relaciones aire/combustible óptimas para la combustión, maximizando la potencia y la eficiencia del motor. |
Preguntas Frecuentes (FAQ)
¿Por qué es tan crítico el peso del combustible en la Fórmula 1?
El peso afecta directamente al rendimiento del coche. Se estima que cada 10 kg de peso extra pueden suponer una pérdida de hasta 0.3 segundos por vuelta, dependiendo del circuito. Por eso, calcular la cantidad exacta de combustible necesario para terminar la carrera, sin un solo gramo de más, es una parte fundamental de la estrategia para ganar.
¿La química también es importante en los neumáticos?
Absolutamente. Los neumáticos de competición son compuestos poliméricos extremadamente complejos. La estructura molecular de estas largas cadenas de polímeros determina su agarre, su ventana de temperatura óptima y su tasa de degradación. Los ingenieros químicos de los fabricantes de neumáticos trabajan constantemente para modificar estas estructuras y encontrar el equilibrio perfecto entre rendimiento y durabilidad.
¿Cómo se aplica esto en otras categorías como el WRC o el Dakar?
Aunque las normativas son diferentes, los principios son los mismos. En el Rally Dakar, la eficiencia del combustible es vital debido a las largas etapas. Un motor que aprovecha mejor cada mol de combustible puede permitir llevar menos peso o tener mayor autonomía. En el WRC, la respuesta del motor es clave, y esta depende directamente de la perfección de la combustión, que se rige por las mismas leyes químicas. En todas las disciplinas, la ciencia de los materiales, basada en la química de sólidos, es crucial para construir coches ligeros y resistentes.
En conclusión, la próxima vez que veas un monoplaza de F1 devorando una recta a más de 350 km/h, recuerda que su velocidad no solo proviene de la fuerza bruta de su motor, sino también de la elegancia y precisión de la ciencia que opera a nivel molecular. Desde el cálculo de la masa de una molécula de combustible hasta la optimización de las reacciones de combustión, la química es la heroína anónima que impulsa la pasión del automovilismo deportivo.
Si quieres conocer otros artículos parecidos a La Química Secreta de la F1: Masa y Moles puedes visitar la categoría Automovilismo.
