03/11/2025
El óxido de plata (I), cuya fórmula química es Ag₂O, es un compuesto inorgánico que juega un papel crucial en diversas áreas de la química y la tecnología. A simple vista, se presenta como un fino polvo de color negro o marrón oscuro, una apariencia que desmiente la complejidad de su estructura y la versatilidad de sus aplicaciones. Este compuesto binario, formado por dos átomos de plata y uno de oxígeno, es un pilar en la preparación de otros compuestos de plata y un reactivo valioso en la síntesis orgánica. A lo largo de este artículo, exploraremos en profundidad sus propiedades, métodos de preparación, reacciones características y su fascinante estructura electrónica a través del diagrama de Lewis.

Propiedades Físicas y Químicas del Óxido de Plata (I)
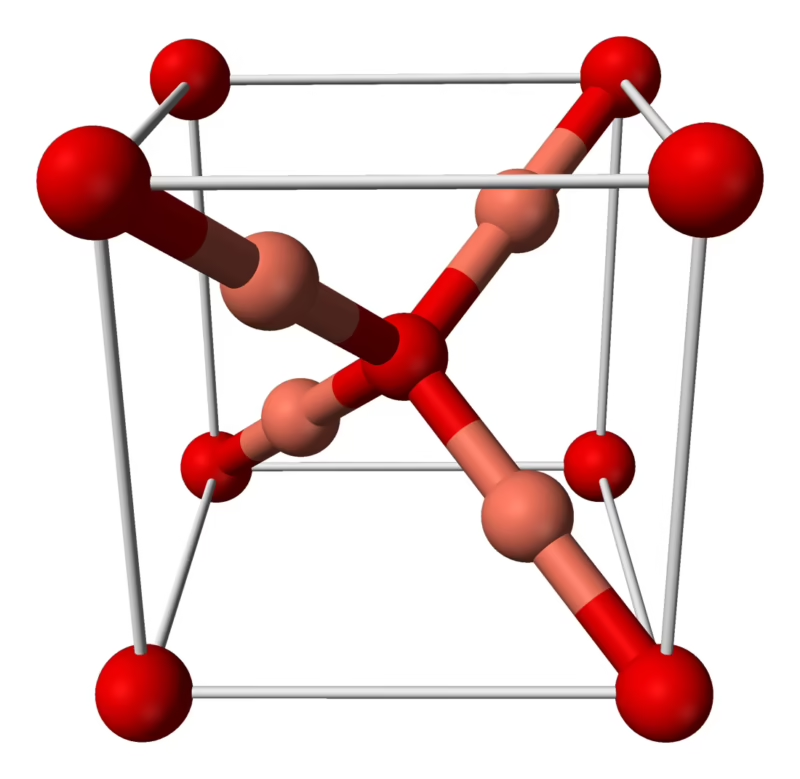
Para comprender verdaderamente el Ag₂O, es fundamental analizar su estructura y comportamiento. A diferencia de compuestos iónicos simples, el óxido de plata es un polímero tridimensional en el que los enlaces entre el metal (plata) y el oxígeno tienen un carácter predominantemente covalente. Su estructura cristalina es isoestructural con la del óxido de cobre (I) (Cu₂O), lo que significa que ambos comparten la misma disposición atómica en el espacio, formando una red cúbica. Esta naturaleza polimérica explica en gran medida su comportamiento frente a los solventes.
Generalmente, el Ag₂O es insoluble en la mayoría de los solventes comunes, incluyendo el agua. Sin embargo, su interacción con el agua no es nula; puede reaccionar en un grado limitado para formar el ion complejo Ag(OH)₂⁻, lo que le confiere una ligera solubilidad en soluciones acuosas. Donde realmente muestra una solubilidad notable es en soluciones de hidróxido de amonio, donde se disuelve para formar derivados solubles complejos de amina-plata. Esta propiedad es ampliamente utilizada en laboratorios para trabajar con compuestos de plata en disolución.
Desde el punto de vista térmico, el óxido de plata es relativamente estable, pero se descompone al ser sometido a altas temperaturas. Al calentarse por encima de los 280 °C, se descompone en sus elementos constituyentes: plata metálica y oxígeno gaseoso, según la reacción: 2 Ag₂O(s) → 4 Ag(s) + O₂(g).
Síntesis y Reacciones Notables
La preparación del óxido de plata en un laboratorio es un proceso relativamente sencillo y directo. El método más común consiste en combinar una disolución acuosa de una sal de plata soluble, como el nitrato de plata (AgNO₃), con una disolución de un hidróxido alcalino, como el hidróxido de sodio (NaOH) o el hidróxido de potasio (KOH). La reacción de precipitación produce el óxido de plata sólido, que puede ser separado por filtración.

Un detalle interesante de esta reacción es que no se forma una cantidad apreciable de hidróxido de plata (AgOH) como intermediario. Esto se debe a que la formación del óxido es energéticamente mucho más favorable, provocando la deshidratación inmediata de cualquier hidróxido de plata que pudiera formarse: 2 AgOH → Ag₂O + H₂O.
El óxido de plata es una base y, como tal, reacciona vigorosamente con ácidos. Por ejemplo, al reaccionar con un ácido halohídrico (HX, donde X es un halógeno como Cl, Br, I), se produce la sal de haluro de plata correspondiente y agua. La ecuación general para esta reacción es:
Ag₂O + 2 HX → 2 AgX + H₂O
Esta reacción es fundamental en muchos procesos de síntesis orgánica y análisis químico.
La Estructura de Lewis del Óxido de Plata (Ag₂O)
La Estructura de Lewis es una representación visual que nos ayuda a entender cómo se distribuyen los electrones de valencia en una molécula. Para dibujar la estructura de Lewis del Ag₂O, seguimos una serie de pasos lógicos:
- Contar los electrones de valencia totales: La plata (Ag) es un metal de transición, pero para estos fines, consideramos que aporta 1 electrón de valencia. El oxígeno (O), al estar en el grupo 16, tiene 6 electrones de valencia. Por lo tanto, el total es: (2 átomos de Ag × 1 e⁻) + (1 átomo de O × 6 e⁻) = 8 electrones de valencia.
- Dibujar la estructura esquelética: El oxígeno es el átomo central, ya que es el más electronegativo y puede formar dos enlaces. La estructura básica será Ag-O-Ag. Esto utiliza 2 enlaces simples, lo que equivale a 4 electrones.
- Distribuir los electrones restantes: Nos quedan 8 - 4 = 4 electrones por distribuir. Estos se colocan como pares solitarios en el átomo más electronegativo, el oxígeno, para completar su octeto. Al añadir dos pares solitarios (4 electrones) al oxígeno, este ahora tiene 2 pares de enlace y 2 pares solitarios, cumpliendo la regla del octeto.
- Verificar octetos y cargas formales: El oxígeno tiene su octeto completo. La plata, como muchos metales de transición, no necesita cumplir la regla del octeto. Ahora calculamos las cargas formales para cada átomo con la fórmula: (electrones de valencia) - (electrones no enlazantes) - (1/2 electrones enlazantes).
- Para cada Ag: 1 - 0 - (1/2 * 2) = 0
- Para O: 6 - 4 - (1/2 * 4) = 0
La estructura final muestra al oxígeno en el centro con dos pares de electrones no enlazantes, unido por enlaces simples a dos átomos de plata. Dado que todas las cargas formales son cero, esta es la estructura de Lewis más estable y representativa para el Ag₂O.
Aplicaciones Industriales y Biomédicas
Las propiedades únicas del óxido de plata le confieren un amplio rango de aplicaciones prácticas:
- Baterías: Es un componente clave en las baterías de óxido de plata (a menudo llamadas baterías de plata-zinc o de botón), que son conocidas por su larga vida útil y su alta relación energía-peso. Se utilizan comúnmente en relojes, calculadoras y otros dispositivos electrónicos pequeños.
- Catálisis: Actúa como un agente oxidante suave en diversas reacciones de síntesis orgánica.
- Nanotecnología: Se utiliza para la producción de nanopartículas de plata, que tienen aplicaciones en electrónica, óptica y medicina.
- Propiedades antimicrobianas: El óxido de plata posee potentes propiedades antimicrobianas. Esta capacidad para inhibir el crecimiento de bacterias, virus y hongos lo hace valioso en aplicaciones médicas, como en recubrimientos para dispositivos médicos, vendajes para heridas y en ciertos productos desinfectantes.
- Materiales fotográficos: Históricamente, los compuestos de plata han sido la base de la fotografía, y el Ag₂O sigue siendo relevante en la fabricación de ciertos materiales fotosensibles.
Tabla Comparativa: Óxidos del Grupo 11
| Propiedad | Óxido de Plata (I) (Ag₂O) | Óxido de Cobre (I) (Cu₂O) |
|---|---|---|
| Fórmula Química | Ag₂O | Cu₂O |
| Apariencia | Polvo negro o marrón oscuro | Polvo rojo o marrón rojizo |
| Estructura Cristalina | Cúbica (Isoestructural con Cu₂O) | Cúbica (Isoestructural con Ag₂O) |
| Uso Principal | Baterías, agente antimicrobiano | Pigmento, fungicida, semiconductor |
Preguntas Frecuentes (FAQ)
¿Cuál es el número CAS del óxido de plata?
El número CAS (Chemical Abstracts Service) que identifica de manera única al óxido de plata (I) es el 20667-12-3. Este identificador es crucial para su seguimiento en bases de datos químicas y para la gestión de seguridad.
¿Es peligroso manipular el óxido de plata?
Sí, se deben tomar precauciones. El Ag₂O puede ser perjudicial si se ingiere o se inhala. El contacto prolongado con la piel puede causar argiria, una coloración grisácea de la piel. Es imprescindible utilizar equipo de protección personal adecuado, como guantes y gafas de seguridad, al manipular este compuesto.
¿El óxido de plata es soluble en agua?
Es considerado insoluble en agua pura. Sin embargo, puede reaccionar con el agua en una pequeña medida para formar iones complejos solubles. Su solubilidad aumenta significativamente en soluciones amoniacales o en presencia de otros agentes complejantes.
¿Por qué se usa en baterías?
Se utiliza en baterías por su excelente estabilidad y su alta densidad de energía. Las baterías de óxido de plata pueden proporcionar un voltaje muy estable durante casi toda su vida útil, lo que las hace ideales para dispositivos que requieren una fuente de alimentación constante y fiable.
Si quieres conocer otros artículos parecidos a Óxido de Plata (Ag₂O): Guía Completa puedes visitar la categoría Automovilismo.
