20/03/2023
El mundo de la química está lleno de compuestos fascinantes que son fundamentales para la industria, la agricultura y hasta la medicina. Uno de estos compuestos es el óxido de potasio (K₂O), una sustancia iónica con propiedades únicas. Para comprender verdaderamente cómo interactúa este y otros compuestos, es esencial dominar una habilidad clave: el balanceo de ecuaciones químicas. Este proceso no es solo un ejercicio académico; es la aplicación directa de uno de los principios más importantes de la ciencia, la Ley de la Conservación de la Materia. En este artículo, exploraremos a fondo el óxido de potasio, desde su estructura hasta sus aplicaciones, y utilizaremos sus reacciones como ejemplo práctico para aprender a realizar un balanceo de ecuaciones de manera correcta y sistemática.

¿Qué es el Óxido de Potasio (K₂O)?
El óxido de potasio es un compuesto iónico que se forma a partir de la combinación de dos elementos: potasio (K) y oxígeno (O). Su fórmula química es K₂O. El potasio es un metal alcalino extremadamente reactivo, por lo que no se encuentra en estado libre en la naturaleza. Posee una valencia de +1 y se combina fácilmente con los átomos de oxígeno. Este óxido, K₂O, se obtiene como una sustancia cristalina de color gris o amarillo pálido cuando el potasio se oxida, generalmente quemándolo en presencia de un exceso de oxígeno. Cuando se disuelve en agua, el óxido de potasio forma un álcali fuertemente corrosivo conocido como hidróxido de potasio.

También es conocido por otros nombres, como monóxido de potasio, hidróxido de dipotasio u óxido de Kalium (del nombre latino del potasio).
Propiedades Físicas y Químicas del Óxido de Potasio
Para entender el comportamiento de este compuesto, es crucial conocer sus propiedades. A continuación, se detallan las más importantes en una tabla comparativa.
| Propiedad | Valor |
|---|---|
| Fórmula Química | K₂O |
| Masa Molar / Peso Molecular | 94.2 g/mol |
| Apariencia | Sólido de color amarillo pálido |
| Olor | Inodoro |
| Densidad | 2.35 g/cm³ |
| Punto de Fusión | 740 °C |
| Solubilidad | Soluble en EtOH (etanol) y éter. Reacciona violentamente con el agua. |
| Carácter | Óxido básico |
En cuanto a sus propiedades químicas, el óxido de potasio es un óxido básico, lo que significa que reacciona con ácidos para formar sal y agua, y con agua para formar una base (hidróxido). Dos de sus reacciones más características son:
- Reacción con agua: Al tratar el óxido de potasio con agua (H₂O), se produce una reacción exotérmica que forma hidróxido de potasio (KOH), una base fuerte. La ecuación es: K₂O + H₂O → 2KOH
- Reacción con ácido clorhídrico: El óxido de potasio reacciona con el ácido clorhídrico (HCl) para formar cloruro de potasio (KCl) y agua. La ecuación es: K₂O + 2HCl → 2KCl + H₂O
El Arte del Balanceo de Ecuaciones Químicas
Las reacciones anteriores nos muestran una transformación, pero para que sean científicamente correctas, deben estar balanceadas. El balanceo de ecuaciones consiste en igualar el número de átomos de cada elemento tanto en los reactivos (las sustancias que inician la reacción, a la izquierda de la flecha) como en los productos (las sustancias que resultan, a la derecha de la flecha). Este procedimiento es fundamental porque verifica la Ley de la Conservación de la Materia, que establece que la materia no se crea ni se destruye, solo se transforma. En una reacción química, los átomos simplemente se reorganizan para formar nuevas moléculas, pero su cantidad total debe permanecer constante.
Guía Paso a Paso para un Balanceo Correcto
Para escribir y balancear una ecuación química de manera efectiva, es necesario seguir un método ordenado. A continuación, se presentan las recomendaciones y pasos a seguir:
- Revisar la Ecuación: Asegúrate de que la ecuación química esté completa y correctamente escrita. Verifica que las fórmulas de todos los compuestos (reactivos y productos) sean las correctas. Un error en una fórmula hará imposible el balanceo.
- Inspección Inicial: Observa si la ecuación ya se encuentra balanceada. Haz un conteo rápido de los átomos de cada elemento a ambos lados de la flecha.
- Priorizar el Orden de Balanceo: Para simplificar el proceso, sigue un orden específico. Balancea primero los metales, luego los no metales, y deja para el final los elementos que suelen aparecer en múltiples compuestos, como el oxígeno y el hidrógeno.
- Uso de Coeficientes: Escribe los números requeridos, llamados coeficientes, al inicio de cada compuesto. Es importante recordar que NUNCA debes cambiar los subíndices de las fórmulas (los números pequeños dentro de la fórmula), ya que eso cambiaría la identidad del compuesto.
- Contar los Átomos: Multiplica el coeficiente de cada compuesto por los subíndices de cada elemento dentro de ese compuesto para obtener el número total de átomos. Si un elemento aparece en más de un compuesto del mismo lado de la ecuación, suma los totales.
- Verificación Final: Una vez que creas que la ecuación está balanceada, realiza un conteo final de todos los elementos para asegurarte de que el número de átomos de cada uno sea idéntico en el lado de los reactivos y en el de los productos. Si no es así, reajusta los coeficientes y repite el proceso.
Ejemplo Práctico: Balanceando las Reacciones del Óxido de Potasio
Apliquemos los pasos anteriores a las reacciones del K₂O que vimos antes.
Reacción con Agua: K₂O + H₂O → KOH
- Revisión: La ecuación está bien escrita.
- Conteo Inicial:
- Reactivos: Potasio (K) = 2, Oxígeno (O) = 1 + 1 = 2, Hidrógeno (H) = 2
- Productos: Potasio (K) = 1, Oxígeno (O) = 1, Hidrógeno (H) = 1
La ecuación no está balanceada.
- Balanceo:
- Metal (K): Hay 2 K en los reactivos y 1 K en los productos. Colocamos un coeficiente de 2 delante del KOH: K₂O + H₂O → 2KOH
- Verificación Final:
- Reactivos: K = 2, O = 2, H = 2
- Productos: K = 1 * 2 = 2, O = 1 * 2 = 2, H = 1 * 2 = 2
¡Perfecto! La ecuación ahora está balanceada: K₂O + H₂O → 2KOH.
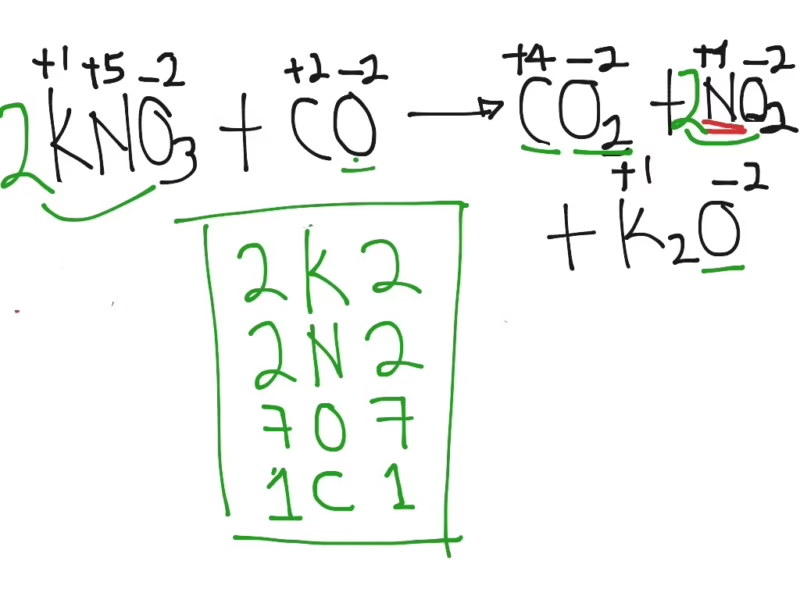
Escribir los números requeridos como coeficiente al inicio de cada compuesto. Contar el número de átomos multiplicando el coeficiente con los respectivos subíndices de las fórmulas y sumar los átomos que estén de un mismo lado de la ecuación. Verificar el balanceo final y reajustar si es necesario.
Reacción con Ácido Clorhídrico: K₂O + HCl → KCl + H₂O
- Revisión: La ecuación está bien escrita.
- Conteo Inicial:
- Reactivos: K = 2, O = 1, H = 1, Cloro (Cl) = 1
- Productos: K = 1, Cl = 1, H = 2, O = 1
La ecuación no está balanceada.
- Balanceo:
- Metal (K): Hay 2 K en los reactivos y 1 K en los productos. Colocamos un 2 delante del KCl: K₂O + HCl → 2KCl + H₂O
- No Metal (Cl): Ahora tenemos 2 Cl en los productos y 1 Cl en los reactivos. Colocamos un 2 delante del HCl: K₂O + 2HCl → 2KCl + H₂O
- Verificación Final:
- Reactivos: K = 2, O = 1, H = 1 * 2 = 2, Cl = 1 * 2 = 2
- Productos: K = 1 * 2 = 2, Cl = 1 * 2 = 2, H = 2, O = 1
La ecuación está completamente balanceada: K₂O + 2HCl → 2KCl + H₂O.
Usos y Aplicaciones del Óxido de Potasio
El óxido de potasio, a menudo denominado "potasa pura", es un estándar comercial en diversas industrias. Sus aplicaciones son variadas y de gran importancia:
- Fertilizantes: Su uso más extendido es en la agricultura. El potasio es uno de los tres macronutrientes esenciales para el crecimiento de las plantas (junto con el nitrógeno y el fósforo). El contenido de potasio en los fertilizantes se expresa comúnmente en términos de su equivalente en K₂O.
- Industria del Vidrio y Jabón: Se utiliza en la fabricación de ciertos tipos de vidrio para mejorar su durabilidad y resistencia. También es un componente en la producción de jabones blandos y líquidos.
- Aplicaciones Médicas: En pequeñas cantidades y en formulaciones específicas, el potasio tiene usos médicos. Históricamente, compuestos de potasio se han empleado en el tratamiento de enfermedades granulomatosas fúngicas, actinomicosis en ganado y otras infecciones.
Preguntas Frecuentes
¿Para qué se utiliza el óxido de potasio?
Es ampliamente utilizado en la industria agrícola como fertilizante. También se emplea en la fabricación de jabones y vidrio. Ciertos procesos médicos también pueden involucrar compuestos derivados del óxido de potasio.
¿El óxido de potasio es ácido o básico?
El óxido de potasio es un óxido básico. Al reaccionar con agua forma una base fuerte (hidróxido de potasio). Otros ejemplos importantes de óxidos básicos incluyen el óxido de hierro (FeO) y el óxido de calcio (CaO).
¿Cómo se produce el óxido de potasio?
Se puede producir mediante la reacción de potasio con oxígeno. Un método común implica tratar el peróxido de potasio (K₂O₂) resultante con potasio metálico adicional para reducirlo a óxido de potasio. La ecuación para esta reacción es: 2K + K₂O₂ → 2K₂O.
Si quieres conocer otros artículos parecidos a Óxido de Potasio: Propiedades y Balanceo Químico puedes visitar la categoría Automovilismo.
