04/08/2021
En el universo del automovilismo deportivo, cada componente, cada material y cada gota de fluido es analizado en busca de la máxima performance. Hablamos de aleaciones ligeras, de aerodinámica de vanguardia y de unidades de potencia híbridas increíblemente complejas. Pero, ¿alguna vez nos hemos detenido a pensar en la química fundamental que subyace en muchas de estas tecnologías? Hoy nos adentraremos en un campo fascinante y poco explorado en nuestras conversaciones de paddock: el mundo de los percloratos. A primera vista, un compuesto químico podría parecer ajeno a la emoción de una carrera, pero como veremos, los principios de su enorme energía y sus aplicaciones industriales tocan de cerca la tecnología que impulsa a nuestros bólidos favoritos.

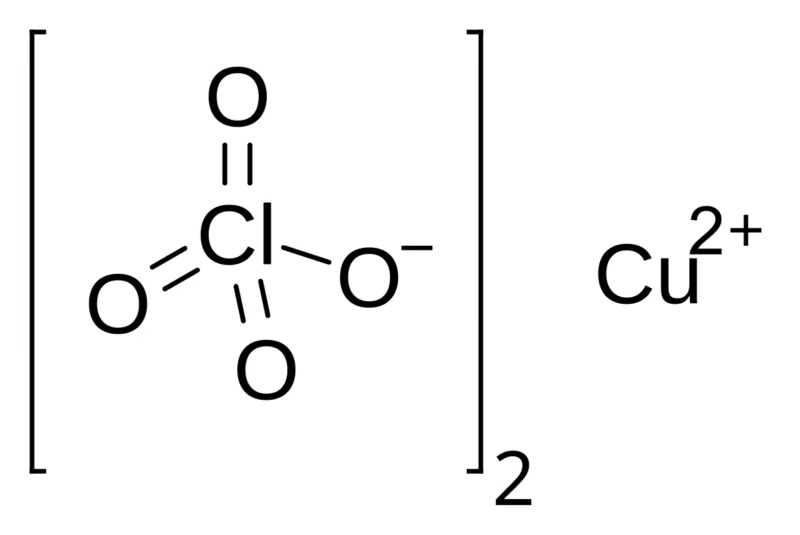
La pregunta inicial que nos trae aquí es específica: ¿cuál es la fórmula del perclorato de cobre (I)? La respuesta es CuClO₄. Esta fórmula se deriva de la unión del ion cobre (I), con una carga positiva (Cu⁺), y el anión perclorato, un grupo de átomos con una carga negativa (ClO₄⁻). Es en este anión, el perclorato, donde reside la clave de una química tan potente como delicada, utilizada en aplicaciones que van desde la exploración espacial hasta elementos de seguridad cruciales en nuestros coches.

- ¿Qué son los Percloratos? La Anatomía de un Compuesto Explosivo
- Del Espacio Exterior a la Pista de Carreras: Aplicaciones de Alto Rendimiento
- El Impacto Ambiental y la Salud: La Responsabilidad Detrás del Poder
- Regulaciones y Seguridad: Estableciendo Límites, como en la Pista
- Preguntas Frecuentes (FAQ)
- Conclusión: La Ciencia Invisible de la Competición
¿Qué son los Percloratos? La Anatomía de un Compuesto Explosivo
Para entender su relevancia, primero debemos desglosar qué es un perclorato. Se trata de un anión, es decir, un ion con carga negativa, cuya fórmula es ClO₄⁻. Consiste en un átomo de cloro central unido a cuatro átomos de oxígeno. Estos aniones no existen de forma aislada en la naturaleza; se unen a iones con carga positiva (cationes) como el amonio, el potasio o el sodio para formar sales estables, conocidas como sales de perclorato. Estos compuestos son generalmente sólidos incoloros y sin olor a temperatura ambiente.
La característica que los hace tan especiales y, a la vez, tan peligrosos, es su comportamiento al ser calentados. Aunque son estables a temperaturas normales, al someterlos a altas temperaturas, inician una reacción que libera una cantidad inmensa de calor. Este calor acelera la reacción del material restante, creando un ciclo de retroalimentación que culmina en una liberación de energía masiva, es decir, una explosión. Esta propiedad es la razón por la que los percloratos son un ingrediente fundamental en propulsores de cohetes, fuegos artificiales, explosivos y bengalas de señalización. La energía contenida en sus enlaces químicos es liberada de forma rápida y violenta, un principio que, en esencia, es lo que busca un motor de combustión: convertir energía química en energía mecánica de la forma más eficiente posible.
Del Espacio Exterior a la Pista de Carreras: Aplicaciones de Alto Rendimiento
El ejemplo más emblemático del poder de los percloratos es el perclorato de amonio. Este compuesto constituía casi el 70% del combustible sólido de los propulsores del transbordador espacial de la NASA. Su capacidad para generar un empuje masivo y sostenido fue clave para poner en órbita toneladas de material. Esta búsqueda de la máxima densidad energética es un eco directo de los desafíos que enfrentan los ingenieros en categorías como la Fórmula 1 o el WEC.
Si bien los percloratos no se utilizan como combustibles directos en los coches de carreras, su presencia se encuentra en tecnologías periféricas pero vitales:
- Airbags: Los sistemas de bolsas de aire en los vehículos, tanto de calle como de competición, dependen de una reacción química extremadamente rápida para inflarse en milisegundos durante un impacto. Algunos de estos sistemas utilizan compuestos que, al igual que los percloratos, generan una gran cantidad de gas de forma casi instantánea tras una ignición. La seguridad del piloto es primordial, y esta tecnología de despliegue rápido es un pilar fundamental.
- Baterías: Algunos tipos de baterías de litio utilizan sales de perclorato en sus electrolitos para facilitar el movimiento de iones. En el contexto del motorsport moderno, con la F1 utilizando sistemas híbridos (ERS) y la Fórmula E basándose completamente en la energía eléctrica, la eficiencia y la seguridad de las baterías son campos de desarrollo críticos.
- Pegamentos y Selladores: Ciertas formulaciones industriales que requieren una alta resistencia y estabilidad utilizan derivados de estos compuestos, cruciales para mantener la integridad estructural de componentes sometidos a vibraciones y fuerzas extremas.
El Impacto Ambiental y la Salud: La Responsabilidad Detrás del Poder
Toda gran potencia conlleva una gran responsabilidad. Debido a su alta solubilidad en agua y su estabilidad a temperaturas normales, los percloratos, si no se gestionan adecuadamente, pueden convertirse en un contaminante ambiental persistente. Históricamente, las instalaciones de fabricación y desmantelamiento de cohetes y material militar han sido fuentes de contaminación del suelo y las aguas subterráneas. Una vez en el ambiente, pueden permanecer durante años, siendo absorbidos por plantas e ingresando en la cadena alimenticia.
El principal efecto de los percloratos en la salud humana es su interferencia con la glándula tiroides. El perclorato inhibe la capacidad de la tiroides para absorber yodo, un elemento esencial para producir hormonas tiroideas. Estas hormonas son cruciales para regular el metabolismo y, especialmente en niños y fetos, para el correcto desarrollo neurológico y físico. Una exposición prolongada a niveles altos de perclorato podría, teóricamente, llevar a hipotiroidismo. Sin embargo, los estudios citados en la documentación de la Agencia de Protección Ambiental (EPA) de EE. UU. indican que los niveles de exposición típicos a través del agua y los alimentos para la población general no parecen causar efectos adversos, especialmente si la ingesta de yodo en la dieta es adecuada.
Tabla Comparativa: Propiedades y Consideraciones de los Percloratos
| Aspecto | Descripción |
|---|---|
| Naturaleza Química | Anión (ClO₄⁻) que forma sales con cationes como amonio, potasio o sodio. |
| Propiedad Clave | Potente agente oxidante; libera gran cantidad de energía al calentarse. |
| Usos de Alto Rendimiento | Propulsores de cohetes, explosivos, pirotecnia, airbags, baterías. |
| Riesgo para la Salud | Interfiere con la absorción de yodo por la glándula tiroides. |
| Impacto Ambiental | Muy soluble en agua, puede contaminar fuentes hídricas y persistir en el ambiente. |
| Regulación | Monitorizado por agencias como la EPA para su control en agua potable y sitios contaminados. |
Regulaciones y Seguridad: Estableciendo Límites, como en la Pista
El mundo de la competición automovilística se rige por un estricto reglamento técnico y deportivo impuesto por organismos como la FIA. Cada aspecto del coche está medido y controlado para garantizar la seguridad y la equidad. De manera similar, el uso y la gestión de sustancias químicas potentes como los percloratos están sujetos a rigurosas regulaciones por parte de agencias gubernamentales.
La EPA, por ejemplo, ha establecido una Dosis de Referencia (RfD) de 0.0007 mg/kg/día para el perclorato. Esta es la ingesta diaria que se estima segura para toda la vida sin riesgo apreciable para la salud, incluso para los grupos más sensibles de la población. A partir de esta dosis, se establecen niveles guía para la concentración en agua potable, que sirven como objetivos para la limpieza de sitios contaminados. Este enfoque basado en datos científicos y márgenes de seguridad es análogo a cómo se definen las estructuras de impacto en un monoplaza o los límites de la pista en un circuito: se establecen para minimizar el riesgo y proteger la integridad de todos los involucrados.
Preguntas Frecuentes (FAQ)
¿Cuál es la fórmula del perclorato de cobre (I)?
La fórmula química del perclorato de cobre (I) es CuClO₄. Se compone de un ion de cobre con estado de oxidación +1 y un anión perclorato.
¿Se usan los percloratos directamente en los motores de Fórmula 1?
No, los percloratos no se utilizan como combustible en los motores de F1. Las unidades de potencia actuales utilizan una gasolina de competición altamente regulada y un sistema de recuperación de energía híbrido. Sin embargo, la química de alta energía de los percloratos es relevante para tecnologías auxiliares como los sistemas de seguridad (airbags) y la electroquímica de las baterías.
¿Son peligrosos los percloratos para el público en general?
El principal riesgo para la salud está asociado a la exposición crónica a niveles elevados, principalmente a través de agua potable contaminada, debido a su efecto sobre la glándula tiroides. Las agencias de salud pública establecen niveles seguros en el agua y los alimentos para proteger a la población. Para la mayoría de las personas, la exposición diaria a través de la dieta y el agua está dentro de los márgenes de seguridad, especialmente con una ingesta adecuada de yodo.
¿Cómo se puede reducir la exposición a los percloratos?
Para la población general, no es necesario tomar medidas especiales más allá de consumir una dieta equilibrada rica en yodo. En áreas con contaminación conocida del agua potable, las autoridades locales suelen emitir avisos y pueden recomendar el uso de agua embotellada o sistemas de filtración. Es fundamental seguir las indicaciones de las agencias de salud locales.
Conclusión: La Ciencia Invisible de la Competición
Desde la fórmula del perclorato de cobre (I) hasta su uso en los confines del espacio, hemos viajado por la ciencia de un compuesto fascinante. Aunque su nombre no resuene en las gradas de Spa o Monza, el perclorato es un recordatorio de que el automovilismo de élite es la suma de innumerables campos del conocimiento. La búsqueda de la liberación controlada de energía, la gestión de materiales potentes y la aplicación de tecnologías de vanguardia bajo un estricto paraguas de seguridad son principios que conectan la química más fundamental con la emoción de la bandera a cuadros. La próxima vez que veamos los fuegos artificiales celebrando a un campeón, quizás recordemos la increíble ciencia que se esconde detrás de esa explosión de luz y color.
Si quieres conocer otros artículos parecidos a Percloratos: El Químico Oculto de la Velocidad puedes visitar la categoría Automovilismo.
