04/04/2020
En el vasto y fascinante universo de la química orgánica, existe una familia de compuestos que juega un papel fundamental tanto en los procesos biológicos como en innumerables aplicaciones industriales: los aldehídos. Desde el aroma de la vainilla hasta la fabricación de plásticos resistentes, estos compuestos están presentes en nuestra vida cotidiana de formas que a menudo pasamos por alto. Su estructura única, caracterizada por un grupo funcional carbonilo, les confiere una reactividad especial que los convierte en piezas clave para la síntesis de una enorme variedad de otros compuestos. Acompáñenos en este recorrido detallado para desentrañar qué son los aldehídos, cómo se forman, cuáles son sus propiedades y por qué son tan importantes en el mundo moderno.

¿Qué son Exactamente los Aldehídos?
Los aldehídos son compuestos orgánicos cuya seña de identidad es la presencia del grupo funcional -CHO, también conocido como grupo formilo. Este grupo está compuesto por un átomo de carbono unido a un átomo de oxígeno mediante un doble enlace (C=O), y a su vez, este mismo carbono está enlazado a un átomo de hidrógeno. La fórmula general que representa a un aldehído es R-CHO.
En esta fórmula:
- R: Representa un radical que puede ser un simple átomo de hidrógeno (en el caso del formaldehído, el aldehído más simple) o una cadena de carbono e hidrógeno, que puede ser alifática (lineal o ramificada) o aromática (conteniendo un anillo de benceno, por ejemplo).
- -CHO: Es el grupo funcional aldehído, donde el grupo carbonilo (C=O) se encuentra en el extremo de la cadena de carbono.
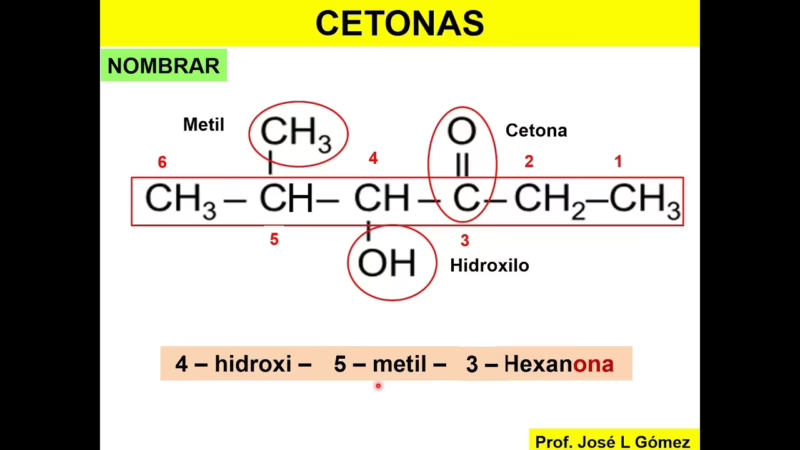
Esta ubicación terminal del grupo carbonilo es lo que distingue fundamentalmente a un aldehído de una cetona, otro compuesto que también posee el grupo C=O. En las cetonas, el carbono del carbonilo está unido a otras dos cadenas de carbono (R-CO-R'), por lo que nunca se encuentra en un extremo.
La presencia del doble enlace carbono-oxígeno introduce una polaridad significativa en la molécula. El oxígeno es más electronegativo que el carbono, lo que significa que atrae con más fuerza a los electrones del enlace. Esto genera una densidad de carga negativa parcial sobre el oxígeno (δ-) y una densidad de carga positiva parcial sobre el carbono (δ+). Esta polaridad es la responsable de muchas de las propiedades físicas y de la reactividad química de los aldehídos.
Obtención y Síntesis de Aldehídos
Los aldehídos pueden obtenerse a través de diversos métodos en el laboratorio, siendo el más común la oxidación controlada o suave de los alcoholes primarios. Un alcohol primario es aquel en el que el grupo hidroxilo (-OH) está unido a un carbono que, a su vez, solo está unido a otro átomo de carbono (o a ninguno, en el caso del metanol).
El proceso de oxidación implica la eliminación de dos átomos de hidrógeno: uno del grupo -OH y otro del carbono al que está unido. Para que la reacción se detenga en la etapa de aldehído y no continúe hasta formar un ácido carboxílico (producto de una oxidación más fuerte), se deben utilizar agentes oxidantes suaves y controlar las condiciones de la reacción. Esquemáticamente:
R-CH₂OH (Alcohol primario) + [O] (Oxidante suave) → R-CHO (Aldehído) + H₂O
Algunos de los métodos y reactivos utilizados para esta transformación son:
- Dicromato de Potasio (K₂Cr₂O₇) en medio ácido: Calentar el alcohol en una disolución ácida de dicromato de potasio es un método clásico. El ión dicromato (Cr₂O₇²⁻, de color naranja) se reduce a ión cromo (III) (Cr³⁺, de color verde), indicando que la oxidación ha tenido lugar. Es crucial destilar el aldehído a medida que se forma para evitar su posterior oxidación a ácido carboxílico.
- Oxidación de Swern: Un método más moderno y suave que utiliza sulfóxido de dimetilo (DMSO), dicloruro de oxalilo y una base (como la trietilamina). Es muy eficaz para obtener aldehídos sin riesgo de sobreoxidación.
Propiedades Físicas Clave de los Aldehídos
Las propiedades físicas de los aldehídos, como sus puntos de ebullición, fusión y solubilidad, están directamente influenciadas por la polaridad del grupo carbonilo y el tamaño de la cadena R.
- Puntos de Ebullición: Los aldehídos tienen puntos de ebullición más altos que los alcanos de peso molecular similar debido a las interacciones dipolo-dipolo causadas por el grupo carbonilo polar. Sin embargo, sus puntos de ebullición son significativamente más bajos que los de los alcoholes correspondientes. Esto se debe a que, a diferencia de los alcoholes, las moléculas de aldehído no pueden formar puentes de hidrógeno entre sí, que son fuerzas intermoleculares mucho más fuertes.
- Solubilidad en Agua: Los aldehídos de cadena corta (hasta cuatro o cinco carbonos) son solubles en agua. Esto es posible porque el átomo de oxígeno del grupo carbonilo puede formar puentes de hidrógeno con las moléculas de agua. A medida que la longitud de la cadena de carbono (la parte no polar 'R') aumenta, la solubilidad en agua disminuye drásticamente, ya que la parte hidrofóbica de la molécula comienza a dominar.
- Olor: Muchos aldehídos tienen olores característicos. Los de bajo peso molecular, como el formaldehído y el acetaldehído, tienen olores penetrantes e irritantes. Sin embargo, a medida que aumenta el tamaño de la molécula, los olores pueden volverse mucho más agradables, a menudo frutales o florales. Por esta razón, muchos aldehídos se utilizan en la industria de los perfumes y saborizantes.
Tabla Comparativa de Aldehídos Comunes
| Nombre Común (Trivial) | Nombre IUPAC | Fórmula | Punto de Fusión (°C) | Punto de Ebullición (°C) |
|---|---|---|---|---|
| Formaldehído | Metanal | HCHO | -92 | -21 |
| Acetaldehído | Etanal | CH₃CHO | -121 | 20 |
| Propionaldehído | Propanal | CH₃CH₂CHO | -81 | 49 |
| Butiraldehído | Butanal | CH₃(CH₂)₂CHO | -99 | 76 |
| Valeraldehído | Pentanal | CH₃(CH₂)₃CHO | -91 | 103 |
| Benzaldehído | Bencenocarbaldehído | C₆H₅CHO | -26 | 178 |
Nomenclatura: ¿Cómo Nombrar un Aldehído?
Existen dos sistemas principales para nombrar a los aldehídos: el sistema IUPAC (Unión Internacional de Química Pura y Aplicada) y la nomenclatura trivial o común.
Sistema IUPAC
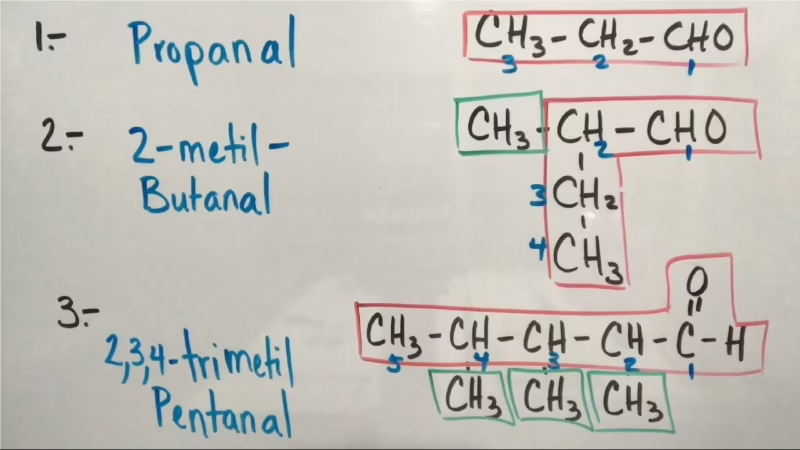
- Se identifica la cadena de carbono continua más larga que contenga al grupo -CHO. El carbono del grupo aldehído siempre es el carbono número 1.
- Se nombra la cadena principal reemplazando la terminación "-o" del alcano correspondiente por el sufijo "-al".
- Se nombran y numeran los sustituyentes (radicales) como en cualquier otro compuesto orgánico, indicando su posición en la cadena.
Ejemplo: CH₃-CH(CH₃)-CH₂-CHO se nombra como 3-metilbutanal.
Sistema Trivial
Los nombres triviales a menudo derivan del nombre del ácido carboxílico correspondiente que se forma por su oxidación. Se utilizan prefijos específicos para el número de carbonos:
- 1 Carbono: Form- (del ácido fórmico)
- 2 Carbonos: Acet- (del ácido acético)
- 3 Carbonos: Propion- (del ácido propiónico)
- 4 Carbonos: Butir- (del ácido butírico)
- 5 Carbonos: Valer- (del ácido valérico)
A estos prefijos se les añade la terminación "aldehído".
Ejemplo: CH₃CH₂CH₂CHO (butanal en IUPAC) se nombra comúnmente como butiraldehído.
Los Aldehídos en Nuestra Vida Cotidiana y en la Industria
La importancia de los aldehídos radica en su amplia gama de aplicaciones y su presencia en la naturaleza.
- Industria Química: Son intermediarios valiosos. El formaldehído (metanal) es uno de los productos químicos más producidos a nivel mundial. Se utiliza para fabricar resinas termoestables como la baquelita (fenol-formaldehído) y la melamina, usadas en adhesivos, tableros de aglomerado y revestimientos.
- Plásticos y Solventes: Sirven como materia prima para la producción de plásticos, solventes y pinturas. Por ejemplo, son precursores de los alcoholes oxo, que se emplean en la fabricación de detergentes.
- Perfumería y Alimentos: Muchos aldehídos aromáticos tienen olores agradables. El benzaldehído huele a almendras amargas, el cinamaldehído es el responsable del olor y sabor de la canela, y la vainillina es el componente principal del extracto de vainilla.
- Biología: Los aldehídos son cruciales en procesos biológicos. La glucosa, un azúcar fundamental para la vida, existe en una forma de cadena abierta que contiene un grupo aldehído. El acetaldehído (etanal) es un producto intermedio en el metabolismo del etanol en el hígado y se considera uno de los principales responsables de los síntomas de la resaca.
- Desinfección y Conservación: El formaldehído en disolución acuosa (formol) se ha utilizado históricamente como conservante de muestras biológicas y como desinfectante. El glutaraldehído es un potente desinfectante en frío utilizado en entornos médicos y para el curtido de pieles.
Preguntas Frecuentes (FAQ) sobre Aldehídos
¿Cuál es la diferencia principal entre un aldehído y una cetona?
La diferencia clave es la posición del grupo carbonilo (C=O). En un aldehído, el grupo carbonilo está en un carbono terminal (al final de la cadena), por lo que está unido a al menos un átomo de hidrógeno (R-CHO). En una cetona, el grupo carbonilo está en un carbono interno, unido a otras dos cadenas de carbono (R-CO-R').

¿Por qué los aldehídos se oxidan fácilmente?
El átomo de hidrógeno unido directamente al carbono del grupo carbonilo es susceptible a la oxidación. Agentes oxidantes, incluso suaves, pueden convertir fácilmente el grupo aldehído (-CHO) en un grupo carboxilo (-COOH), formando un ácido carboxílico. Esta facilidad de oxidación es una de sus propiedades químicas más características.
¿Son peligrosos los aldehídos?
Como con muchos productos químicos, su peligrosidad depende del compuesto específico y de la exposición. El formaldehído es clasificado como un probable carcinógeno humano y es un irritante potente. El acetaldehído es tóxico y contribuye a los efectos dañinos del consumo excesivo de alcohol. El glutaraldehído puede causar dermatitis alérgica. Es fundamental manejarlos con las precauciones de seguridad adecuadas.
¿Qué es la vainillina?
La vainillina (4-hidroxi-3-metoxibenzaldehído) es un aldehído aromático que constituye el principal componente químico del extracto de la vaina de vainilla. Es ampliamente utilizado como agente saborizante en alimentos, bebidas y productos farmacéuticos, así como en la industria de la perfumería por su agradable y característico aroma.
Si quieres conocer otros artículos parecidos a Aldehídos: Estructura, Usos y Propiedades puedes visitar la categoría Automovilismo.
