24/08/2021
En el vertiginoso mundo de la Fórmula 1, cada milisegundo cuenta. Hablamos de aerodinámica, de potencia del motor, de la estrategia en el muro de pits y del talento innato de los pilotos. Pero, ¿alguna vez nos hemos detenido a pensar en la química que une a un equipo campeón? No me refiero únicamente a la química entre piloto e ingeniero, sino a una estructura mucho más profunda y fundamental, una que, curiosamente, encuentra su mejor analogía en los diagramas que estudiábamos en la escuela: la estructura de Lewis. A primera vista, comparar una molécula de Cloro (Cl₂) o Nitrógeno (N₂) con una organización como Red Bull Racing o Ferrari puede parecer una locura, pero los principios de enlace, estabilidad y estructura son universalmente aplicables y nos ofrecen una perspectiva única para entender qué hace que un equipo no solo compita, sino que domine.

La Estructura de Lewis: El Plano de un Equipo Ganador
En química, la estructura de Lewis es un diagrama que muestra los enlaces entre los átomos de una molécula y los pares de electrones solitarios que puedan existir. Es, en esencia, el plano de cómo los componentes básicos se unen para formar algo más grande y estable. Ahora, traslademos esto al paddock. Un equipo de Fórmula 1 está compuesto por cientos de "átomos": pilotos, ingenieros, mecánicos, estrategas, personal de marketing, directivos. Cada uno posee sus propias "valencias", sus habilidades y conocimientos.
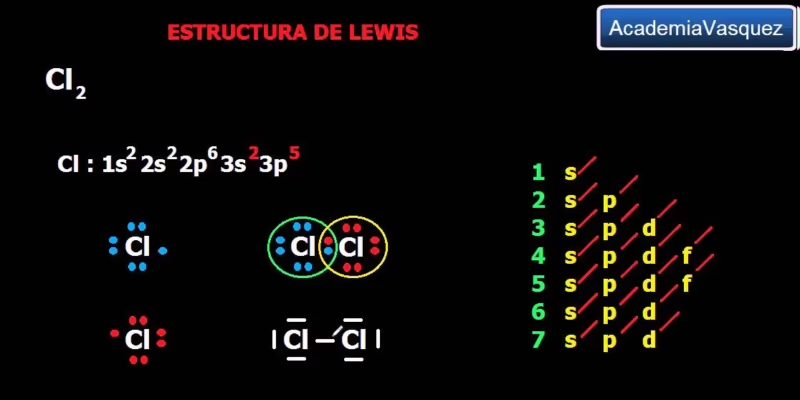
Tomemos como ejemplo la molécula de Cloro (Cl₂), mencionada en la información de base. Se trata de dos átomos de cloro unidos por un enlace simple. Cada átomo comparte un electrón con el otro, formando un par enlazante que los mantiene unidos. Además, cada átomo de cloro conserva tres pares de electrones para sí mismo, los llamados pares solitarios. En nuestra analogía, este enlace simple podría representar la conexión fundamental entre los dos pilotos de un equipo. Comparten un objetivo común (el par enlazante): el éxito del equipo. Sin embargo, cada uno mantiene sus propios secretos de puesta a punto, su telemetría y su equipo de ingenieros (los pares solitarios), que son cruciales para su estabilidad y rendimiento individual, pero que no se comparten directamente.
El Enlace Triple del Nitrógeno: La Cohesión Total
Si el Cl₂ representa una colaboración funcional, la molécula de Nitrógeno (N₂) es el ideal al que todo equipo aspira. La estructura de Lewis del N₂ nos muestra dos átomos de nitrógeno unidos por un enlace triple. Esto significa que comparten tres pares de electrones, creando uno de los enlaces covalentes más fuertes y estables que existen en la naturaleza. La energía necesaria para romper este enlace es inmensa, lo que hace al N₂ una molécula relativamente inerte y muy estable.
¿No es esa la descripción perfecta de un equipo en su era de dominio? Pensemos en la relación entre Max Verstappen y su ingeniero Gianpiero Lambiase en Red Bull, o la histórica dupla de Michael Schumacher y Ross Brawn en Ferrari. Esa es una conexión que va más allá de un simple intercambio de información; es un enlace triple. Comparten una comprensión casi telepática (múltiples pares de electrones compartidos) que los hace increíblemente eficientes y resistentes a la presión externa. La estabilidad de esta unión es la que permite al resto de la "molécula" del equipo funcionar a la perfección. Cada átomo de nitrógeno, al formar este enlace, cumple la regla del octeto, alcanzando una configuración electrónica estable. De igual manera, cuando las piezas clave de un equipo logran esta sinergia, todo el conjunto alcanza su máxima estabilidad y potencial de rendimiento.
Enlaces Iónicos vs. Covalentes: Dinámicas de Equipo en la Parrilla
La química nos ofrece más modelos para analizar las dinámicas de equipo. No todas las uniones son iguales. Consideremos el Cloruro de Bario (BaCl₂), un compuesto iónico. Aquí no se comparten electrones, sino que hay una transferencia. El Bario (un metal) cede electrones y se convierte en un ion positivo, mientras que el Cloro (un no-metal) los acepta y se convierte en un ion negativo. La atracción electrostática entre estas cargas opuestas crea una red cristalina muy fuerte y ordenada.
Esta dinámica de "enlace iónico" puede verse en equipos con una estructura muy jerárquica y tradicional. Pensemos en una escudería con un director de equipo autoritario y carismático (el ion metálico que "cede" la dirección y la visión) y departamentos altamente especializados que "aceptan" y ejecutan esas directivas sin cuestionarlas (los iones no metálicos). Esta estructura puede ser increíblemente fuerte y exitosa, como lo fue Mercedes-AMG Petronas durante su racha de campeonatos, donde la visión clara desde la cúpula generó una máquina de ganar casi perfecta. La estructura es rígida, pero inmensamente poderosa.
Por otro lado, el "enlace covalente" (como en el N₂ y Cl₂) representa un modelo más colaborativo. Equipos como McLaren en su reciente reconstrucción parecen operar más bajo este paradigma. Se fomenta el "compartir" ideas y recursos entre departamentos para alcanzar un objetivo común. No hay una transferencia unidireccional de directivas, sino una puesta en común de "electrones" (conocimiento, datos, innovación) para fortalecer el conjunto. Ambos modelos pueden llevar al éxito, pero la estabilidad y la resiliencia a largo plazo a menudo provienen de los enlaces más fuertes y compartidos.
Tabla Comparativa: Química y Fórmula 1
| Concepto Químico | Descripción Breve | Analogía en Fórmula 1 |
|---|---|---|
| Estructura de Lewis | Diagrama de enlaces y electrones en una molécula. | El organigrama y las líneas de comunicación de un equipo. |
| Enlace Covalente Simple (Cl₂) | Dos átomos comparten un par de electrones. | La relación profesional entre compañeros de equipo. |
| Enlace Covalente Triple (N₂) | Dos átomos comparten tres pares de electrones. Muy estable. | La sinergia total entre un piloto y su ingeniero de carrera. |
| Enlace Iónico (BaCl₂) | Transferencia de electrones y atracción de cargas opuestas. | Una estructura de equipo jerárquica con un liderazgo fuerte. |
| Pares Solitarios | Electrones no compartidos que pertenecen a un solo átomo. | Conocimientos y habilidades individuales de cada miembro del equipo. |
Preguntas Frecuentes (FAQ)
¿Es esta analogía solo una metáfora o la química real importa en la F1?
Aunque la comparación con las estructuras de equipo es una metáfora para entender la dinámica, la química real es absolutamente fundamental en la Fórmula 1. La composición del combustible, la degradación de los neumáticos, la ciencia de los materiales del chasis de fibra de carbono y la lubricación del motor son campos donde la química y la ingeniería química deciden campeonatos.
¿Qué tipo de "enlace" es más exitoso en un equipo de F1, iónico o covalente?
No hay una respuesta única. Ambos modelos han demostrado ser exitosos. El modelo "iónico" o jerárquico puede producir resultados rápidos y dominantes bajo un liderazgo visionario. Sin embargo, el modelo "covalente" o colaborativo puede ser más resiliente y adaptable a los cambios de reglamento, fomentando la innovación desde todas las áreas del equipo. Los equipos más exitosos suelen tener una combinación de ambos.
¿Por qué es tan estable la molécula de N₂ mencionada en el artículo?
La estabilidad del Nitrógeno molecular (N₂) proviene de la enorme energía de su enlace triple. Se necesitan 226 kilocalorías por mol para romperlo, una cifra altísima. Esta fuerza hace que la molécula no reaccione fácilmente con otras sustancias en condiciones normales, lo que se define como inercia química. En nuestra analogía, esta es la "inercia" al caos y la presión externa que define a los grandes equipos.
En conclusión, la próxima vez que veamos un monoplaza de Fórmula 1 cruzar la línea de meta en primer lugar, recordemos que detrás de esa proeza de ingeniería y pilotaje, existe una estructura invisible. Una red de enlaces humanos, tan complejos y vitales como los enlaces atómicos que gobiernan el universo. El éxito no es solo una suma de partes; es el resultado de una estructura perfectamente enlazada, una molécula de campeonato que ha alcanzado su estado más estable y energético.
Si quieres conocer otros artículos parecidos a F1: La Química Invisible del Éxito puedes visitar la categoría Automovilismo.